
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Хххххххх
|
|
Хлор қышқылының формуласын көрсетiңiз.
А) HCl В) HclO С) HclO2 D) HclO3 Е) HclO4
№ 107. Хлордың қайсы қосылысы тек тотықтырғыш қасиет көрсетедi?
KCl NaClO HClO4 Ca(ClO3)2 KClO2
№ 212. Хлордың ең жоғарғы тотығу дәрежесiн көрсетiңiз.
№ 215. Хром (24Cr) атомында, қалыпты жағдайда неше тақ электрон болады?
№ 231. Хлордың 17Cl …3s23p5 (максималлды) ең жоғары тотығу дәрежесiн көрсетiңiз.
№ 234. Хром катионындағы Сr3+ электрондар санын көрсетiңiз. Хром атомы (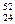 Сr).
Сr).
№ 13
00 С газдың көлемі1 м3 . Егер қысым тұрақты болса, қандай температурада газдың көлемі екі еселенеді?
№15
70 С 100 кПа қысымдағы газдың көлемі 600 м3. –130С 80 кпа – дағы газдың көлемі:
44,5 г AlCl3 –тегі хлор атомының саны неге тең?
90,3 % кремний мен 9,7 % сутегінен тұратын қосылыстың буының тығыздығы сутекпен салыстырғанда 31,9. Осы қосылыстың формуласы қандай?
№ 25
00С 101,3 кПа 200 л хлордың массасы:
№ 31. 0,25М NaOH ерiтiндiсiнiң титрiн анықтаныз.
№ 38. 20 %-тiк ерiтiндi дайындау үшiн 400 г суда NaNO3-тiң қандай мөлшерiн ерiту керек?
№ 40. 100 мл ерiтiндiде 49 г H2SO4 бар болса, осы ерiтiндiнiң нормалдығы қандай?
№ 44. 100 мл ерiтiндiде 3,4 г AgNO3 болса, осы ерiтiндiнiң нормалдығы қандай?
№ 46. 30 г бейэлектролит (электролит емес) 500 г суда ерiтiлген. КН2О=1,860С. Ерiтiндi –1,860С-та қатады. Ерiтiлген заттың молекулалық массасын анықтаңыз
№ 53. 160 г суда 40 г тұз ерiтiлген. Ерiтiндiдегi заттың массалық үлесi қандай?
№ 54. 250 мл ерiтiндiдегi 10,5 г натрий фторидiнiң нормалдық концентрациясы неге
тең? MNaF=42 г/моль.
H2CO3 H3PO4 NaNO3 Cu(OH)2 H2S
№ 56. 400 г 50 % H2SO4 ерiтiндiсiнен (массасы бойынша) буландырып 100 г суды бөлiп алдық. Қалған ерiтiндiдегi H2SO4 массалық үлесi (%) неге тең?
№ 57. 500 мл 0,25Н Na2CO3 ерiтiндiсiнде қанша Na2CO3 (г) ерiтiлген?
№ 59. 180С температурада Mg(OH)2 –магний гидроксидiнiң суда ерiгiштiгi 1,7*10-4 моль/л. Осы температурадағы Mg(OH)2-ерiгiштiк көбейтiндiсiн анықта (молл/л).
№ 60. 250 г суға 54 г глюкоза (C6H12O6) ерiтiлген. Осы ерiтiндi қандай температурада (0С) кристалданады?
№ 61. 1 литр құрамында 49 г H2SO4 бар. Осы ерiтiндiнiң нормальдық концентрациясы неге тең? Mr(H2SO4)=98 г/моль.
№ 64. 250 мл сулы ерiтiндiде 10,5 г натрий фторидi ерiтiлген. (Мr(NaF)=42). Ерiтiндiнiң нормальдық концентрациясын анықта.
№ 115. 0,01М ZnSO4 тұзы ерiтiндiсiндегi мырыштың электрод потенциалын
есептеңiз: E0Zn2+/zn=-0,76B.
№ 120. 0,01М CuSO4 ерiтiндiсiндегi мыстың электродтық потенциалын (В) анықтаңыз: E0Cu2+/Cu=+0.34B.
№ 125. 2 моль су мөлшерiн 2А ток күшiмен ыдыратуға қанша уақыт (сағ-мөлшерiмен) қажет?
№ 137. 0,5 моль сутегiнiң (қ.ж.) көлемiн анықтаңыз.
№ 138. 11,2 л көмiртегi (IV) оксидiнiң қалыпты жағдайдағы мөлшерi нешеге тең?
№ 139. 2 моль хлордың (Cl2) қалыпты жағдайдағы көлемi қандай?
№ 141. 5,6 л азот оксидiнiң (NO) қ.ж. мөлшерiн (n) табыңыз?
№ 151. 2 моль темiр сульфидiнiң (FeS) массасын көрсетiңiз.
№ 155. 56 г азоттың (N2) қ.ж. моль санын көрсетiңiз.
№ 160. 0,5 моль күкiрт қышқылының массасы (г) қандай? M(H2SO4)=98 г/моль
№ 161. 34 г аммиак (NH3) қалыпты жағдайда қандай көлем (л) алады?
№ 162. 5 л газдың қалыпты жағдайдағы массасы 7,15 г. Осы газдың азотпен
№ 257. 5,6 г күкiрт темiрмен қосылғанда 17,59 кДж жылу бөлiнген. Темiр сульфидiнiң түзiлу жылуын есептеңiз, мына реакция бойынша: Fe+S=FeS
№ 277. 2,5 А токты қалайы хлоридiнен SnCl2 30 мин өткiзгенде 2,77 г қалайы бөлiндi. Қалайының эквивалентiн тап.
№ 293. 1 сағ бойы AlCl3 балқымасынан 13,4 А. ток жiбергенде бөлiнетiн алюминийдiң массасы:
№ 294. 15 минут 5 А. токты күмiс нитраты ерiтiндiсiнен өткiзгенде 5,04 г күмiс бөлiндi. Ток шығымы қандай?
№ 317. 100 г ерітіндіде 5 г Ca(OH)2Бар. Гидроксид кальцийдің массалық үлесін w, % табыңдар.
№ 352. 5 л 1Н Na2SO4 ерiтiндiсiн дайындау үшiн қанша грамм Na2SO4 өлшеп алу керек?
№ 353. 1 литр ерiтiндiде 98 г H2SO4 болса (MH2SO4=98 г/моль) осы ерiтiндiнiң молярлық концентрациясы қандай?
№ 354. 100 мл ерiтiндiде 3,4 г AgNO3 ерiтiлген. Ерiтiндiнiң нормалдығы қандай?
M(AgNO3 )=170 г/моль).
№ 356. 80 г электролит емес зат 2 кг суда (Н2О) ерiтiлген. Бұл заттың молярлық массасы 80 г/моль. KH2O=1,860. Ерiтiндiнiң қату температурасын анықтаңыз (Dt).
№ 357. 0,01М HNO3 ерiтiндiсiнiң рОН мәнiн есептеңiз.
№ 358. 0,01М КОН ерiтiндiсiнiң рН мәнiн есептеңiз.
$$$ 368
90,3 % кремний 9,7 % сутегінен тұратын қосылыстың буының сутегімен салыстырғандағы тығыздығы 31,9. Қосылыстың формуласы:
$$$ 392
15 минут 5 А. Токты күмiс нитраты ерiтiндiсiнен өткiзгенде 5,04 г күмiс бөлiндi.
Ток шығымы қандай?
Zn/Zn2+ (0,01 моль/л) // Cd2+ (0,01 моль/л)/Cd гальваникалық элементiнiң E0Cd2+/Cd=-0,43 B; E0Zn2+/Zn=-0,76 B болса, онда ЭҚК неге тең?
1 сағ бойы AlCl3 балқымасынан 13,4 А. ток жiбергенде бөлiнетiн алюминийдiң массасы:
Date: 2015-09-22; view: 887; Нарушение авторских прав