
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Характеристика щелочных металлов
|
|
Общие свойства металлов
76. В свободном виде в природе встречаются:
а) цинк, магний;
б) натрий, калий;
в) серебро, медь;
г) железо, алюминий.
77. Какая реакция является примером алюмотермии?
а) Al + HCl =...;
б) Al2О3 + HNO3 =...;
в) Al + Cl2 =...;
г) Al + MnO2 =....
78. Какой металл нельзя получить электролизом раствора его хлорида?
а) Никель;
б) медь;
в) калий;
г) серебро.
79. Из какого оксида можно получить металл восстановлением водородом?
a) СuO;
б) K2O;
в) Al2O3;
г) ZnO.
80. Имеется смесь хлоридов меди(II), цинка, серебра. В какой последовательности будут восстанавливаться эти металлы на катоде?
а) Cu, Zn, Ag;
б) Ag, Cu, Zn;
в) Zn, Ag, Cu;
г) Zn, Cu, Ag.
81. Какой из приведенных ниже металлов самый мягкий?
а) Серебро;
б) никель;
в) калий;
г) железо.
82. Металлы с какой плотностью считаются тяжелыми?
а) Около 1 г/см3;
б) более 10 г/см3;
в) около 3 г/см3;
г) более 5 г/см3.
83. Какая из перечисленных ниже реакций не протекает?
а) Ca + Cl2 =...;
б) Ag + N2 =...;
в) Na + S =...;
г) К + О2 =....
84. Какой из перечисленных ниже металлов является легким?
а) Алюминий;
б) цинк;
в) медь;
г) серебро.
85. Какая из перечисленных ниже реакций может протекать?
а) MgCl2 + Cu =...;
б) NaCl + Fe =...;
в) СuCl2 + Zn =...;
г) Al2(SO4)3 + Ni =....
86. С помощью какой реакции нельзя получить водород?
а) Cu + HNO3 =...;
б) Mg + H2SO4 (р-р) =...;
в) Fe + HCl =...;
г) Al + HCl =....
87. В контакте находятся два металла – свинец и цинк. Коррозия какого металла будет протекать вначале?
а) Свинца;
б) цинка;
в) корродировать будут оба металла;
г) коррозия не пойдет.
88. Никелирование – это процесс покрытия металлов или сплавов:
а) оксидом никеля;
б) никелем;
в) гидроксидом никеля;
г) хромом.
Характеристика щелочных металлов
89. Электронная конфигурация катиона калия:
а) 1 s 22 s 22 p 4;
б) 1 s 22 s 22 p 63 s 23 p 64 s 0;
в) 1 s 22 s 22 p 63 s 2;
г) 1 s 22 s 22 p 63 s 23 p 4.
90. Взаимодействие большинства щелочных металлов с кислородом приводит к образованию:
а) пероксидов;
б) оксидов;
в) гидридов;
г) гидроксидов.
91. С помощью какой реакции можно получить кислород?
а) К + H2O =...;
б) Na2O2 + CO2 =...;
в) K2O + CO2 =...;
г) Mg + H2SO4 =....
92. Степень окисления кислорода в пероксиде натрия Na2O2 равна:
а) +1;
б) 0;
в) +2;
г) –1.
93. Примером щелочи служит:
а) Cu(OH)2;
б) Mg(OH)2;
в) KOH;
г) CaO.
94. Формула известковой воды:
а) Na2CO3;
б) NaHCO3;
в) K2CO3;
г) Ca(OH)2.
95. Формула питьевой соды:
а) NaCl;
б) NaHCO3;
в) Na2SO4;
г) K2CO3.
96. Амальгама – это сплав любого металла с:
а) серебром;
б) алюминием;
в) ртутью;
г) железом.
97. Какая реакция характеризует гидроксид алюминия как амфотерное основание?

Железо
98. Формула магнетита:
а) FeO;
б) Fe3O4;
в) Fe2O3;
г) Fe.
99. Реагентом на соли трехвалентного железа является:
а) серная кислота;
б) КОН;
в) K2CO3;
г) роданид калия.
100. Какая из приведенных ниже реакций не протекает?

101. Содержание углерода в стали:
а) 5%;
б) 0,02%;
в) от 0,1 до 2%;
г) свыше 10%.
102. Какая из приведенных ниже реакций не протекает?
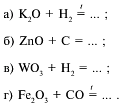
ЧАСТЬ A. Тестовые задания c выбором ответа
1 (1 балл) Распределение электронов по энергетическим уровням в атоме магния:
A. 2е, 2е. Б. 2е, 4е B.2е, 3е. Г. 2е, 8е, 2е.
2 (1 балл) Число электронов на внешнем электронном слое y атомов щелочных металлов:
А.1. Б.2. В.3. Г.4.
3 (1балл). Тип химической связи в простом веществе литии:
A. Ионная. Б. Ковалентная полярная.
B. Ковалентная неполярная. Г. Металлическая.
4 (1 балл). Простое вещество c наиболее ярко выраженными металлическими свойствами:
A. Бериллий. B. Магний.
Б. Кальций. Г. Стронций.
5 (1 балл). Радиус атомов элементов 3-го периода c увеличением заряда ядра от щелочного металла к галогену:
A. Изменяется периодически. Б. Не изменяется.
B. Увеличивается. Г. Уменьшается.

|
6 (1 балл). Атом алюминия отличается от иона алюминия:
А. 3арядом ядра. В. Числом протонов.
Б. Радиусом частицы. Г. Числом нейтронов.
7 (1 балл). Наиболее энергично реагирует с водой:
А. Калий Б. Кальций В. Скандий Г. Магний.
8 (1балл). С разбавленной серной кислотой не взаимодействует:
А. Железо Б. Никель В. Платина Г. Цинк
9 (1 балл). Гидроксид алюминия взаимодействует с веществом, формула которого:
А. КОН (р-р). В. КNОз (р-р).
Б. NaC1 (Р-Р). Г. BaSO4.
10 (1балл). Ряд, в котором все вещества реагируют с железом:
А. HC1, О2, H2SO4. В. КОН, HgO, Н3РО4.
Б. СаО, НСl, НNОз. Г. Н2, О2, СО2.
ЧАСТЬ Б. 3адания со свободным ответом
11 (6 баллов). Составьте уравнения химических реакций, необходимых для осуществления превращений. В первой реакции укажите окислитель и восстановитель, для третьей составьте полное и сокращенное ионное уравнение.
Al→ Al2О3 → AlCL3 → Al(ОН)3 → Al(NОз)3
12 (3балла).Задача на примеси. Определите массу алюминия, который выделится при взаимодействии водорода с 200г оксида алюминия, содержащего 49% примесей.
| <== предыдущая | | | следующая ==> |
| Рекомендации для бросающих курить постепенно | | | Введение. Институт высокоточных систем им |
Date: 2015-09-22; view: 402; Нарушение авторских прав