
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Реакции аминогруппы
|
|
2.1.1. Основность.
Анилин значительно более слабое основание, чем амины жирного ряда и чем аммиак, т.к. неподелённая пара электронов атома азота участвует в сопряжении с π-системой бензольного кольца, и присоединение протона к ней затруднено. При замене атомов водорода в аминогруппе на алкильные радикалы основность N-алкилзамещённых анилина несколько возрастает.
Растворы анилина не обнаруживают по лакмусу щелочной реакции и не окрашивают фенолфталеин.
Анилин образует соли только с сильными кислотами:
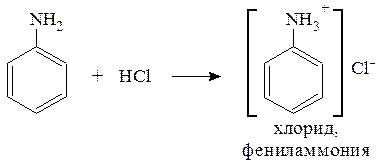
Вторичные и третичные амины, содержащие только ароматичес-кие заместители, например, дифениламин и трифениламин являются очень слабыми основаниями:
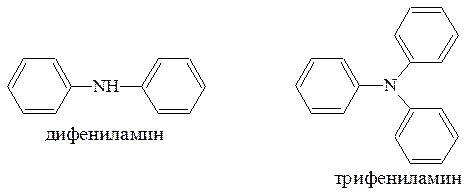
Трифениламин солей не образует даже с сильными кислотами.
2.1.2. Алкилирование анилина - реакция аналогична алкилирова-нию аминов жирного ряда.
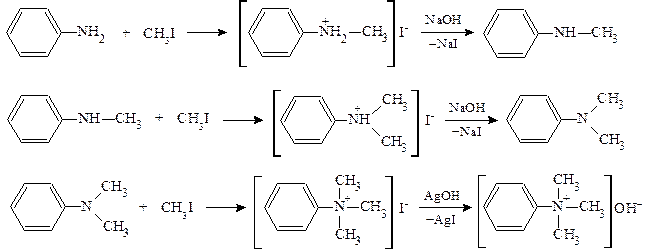
2.1.3. Образование вторичных и третичных аминов, содержащих только ароматические радикалы.
а) Получение вторичных аминов:
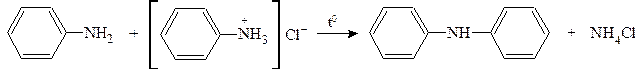
б) Третичные амины получают нагреванием вторичных аминов с иодбензолом в присутствии сухого поташа и порошкообразной меди:
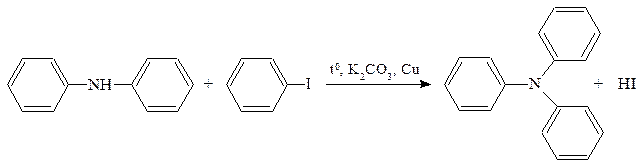
2.1.4. Получение анилидов.
Так, ацетанилиды можно получать ацилированием аминов при помощи карбоновых кислот, а также их ангидридов и хлорангидридов:
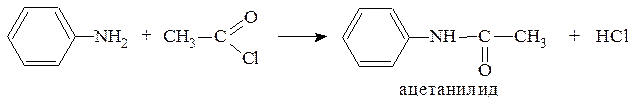
Ацетанилид нашёл некоторое применение в медицине под названием «антифебрин». Это первый синтетический жаропонижаю-щий препарат был синтезирован в 1886 г. В промышленности ацетанилид применяется в качестве промежуточного продукта при синтезе ряда лекарственных веществ и красителей. Интерес для медицины представляет производное ацетанилида, содержащее этоксигруппу в пара-положении бензольного кольца:
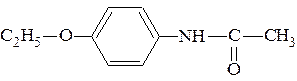
пара-этоксиацетанилид, известен как
жаропонижающий препарат - фенацетин.
2.1.5. Действие азотистой кислоты.
Как и в ряду аминов жирного ряда, эта реакция протекает по-разному для первичных, вторичных и третичных аминов.
а) В случае первичного амина происходит замена аминогруппы на гидроксил:
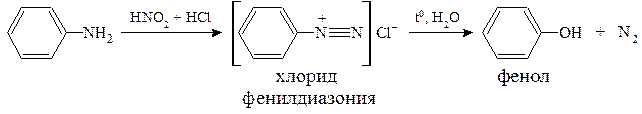
б) Вторичные жирно-ароматические амины, реагируя с азотистой кислотой, образуют N-нитрозо-N-алкиланилин:

В кислой среде происходит перегруппировка: нитрозогруппа перемещается в пара-положение бензольного кольца.
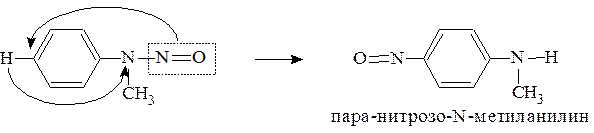
в) Третичные жирно-ароматические амины легко реагируют с азотистой кислотой. Нитрозогруппа сразу вступает вместо атома водорода в пара-положение кольца. Это реакция электрофильного замещения, в которой электрофилом является частица NO+:
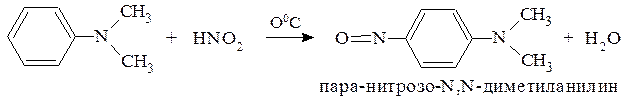
При нагревании со щелочами нитрозодиметиланилин обменивает группу -N(CH3)2 на гидроксильную группу, образуя пара-нитрозофенол и вторичный амин:
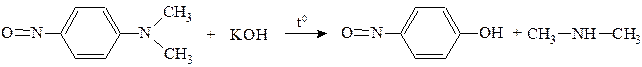
2.1.6. Восстановление.
Анилин восстанавливается с трудом. Однако при действии водорода под давлением над Ni катализатором образуется циклогексиламин:
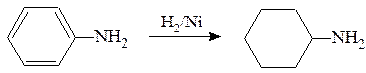
2.1.6. Окисление.
Анилин легко окисляется. При этом образуется смесь хинонов и их производных.
Date: 2015-09-25; view: 1713; Нарушение авторских прав