
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Краткие теоретические сведения
|
|
Под микроанализом понимают изучение строения (структуры) металлов и сплавов с помощью металлографического микроскопа. Под структурой понимают такие особенности материалов, которые обусловлены размером, формой и взаимным расположением кристаллов или зерен, их количественным соотношением. В зависимости от размеров структурных составляющих и применяемых методов их выявления используют следующие понятия: макроструктура, микроструктура и тонкая структура.
Изучая строение кристаллов невооруженным глазом или при небольших увеличениях с помощью лупы, выявляют макроструктуру материала. Большинство материалов состоит из мелких кристалликов (зерен). Наблюдать такие мелкие структурные составляющие – микроструктуру возможно с помощью оптического (размером до 10-7 м) или электронного (размером до 2·10-10 м) микроскопа. Микроскопические методы дают возможность определить размеры и форму кристаллов, наличие различных по своей форме кристаллов, их распределение и относительные объемные количества, форму инородных включений и микропустот и др. Величина зерна поликристаллических материалов является одной из важных характеристик структуры и определяет большинство физико-механических свойств материалов. Тонкая структура описывает расположение элементарных частиц в кристалле и электронов в атоме. Изучается она дифракционными методами (рентгенография, электронография, нейтронография). Микрошлифом называется образец металла, поверхность которого подготовлена для микроанализа. Место вырезки металлического образца (темплета) зависит от вида изделия и задачи исследования. Его часто определяют после макроструктурного анализа слитков, отливок, а также изделий, подвергнутых деформации, сварке, химико-термической обработки. При вырезке образца должна быть сохранена структура исследуемого металла.
Размеры и форма образца. Удобной является цилиндрическая форма образца диаметром 10–12 мм и высотой 0,7–0,8 диаметра, например диаметром 12 мм и высотой 10 мм (рис. 3.1, а). Удобны также прямоугольные образцы с основанием 12х12 мм и высотой 10 мм (рис. 3.1, б). Образцы небольшого сечения (проволока, листы и т. д.) монтируются в зажиме или заливаются в металлическом кольце с помощью легкоплавких металлических сплавов или пластмасс (рис. 3.1, в, г). Приготовление микрошлифа включает операции шлифовки, полирования и травления.
Приготовление микрошлифа включает операции шлифовки, полирования и травления. Наиболее распространен механический метод шлифования. Поверхность образца выравнивают на абразивном круге или напильником так, чтобы края не сминались, а затем шлифуют вручную на наждачных шкурках (бумагах) различных номеров с постепенным уменьшением крупности абразивных частиц, при этом шкурки кладут на толстое стекло. Неровности поверхности образца постепенно срезаются абразивными частицами. При переходе от одного номера зернистости к другому необходимо очищать образец от абразива, промывая водой и менять направление шлифовки на 90°.
Механическое шлифование может осуществляется на специальных шлифовальных машинах, имеющих несколько кругов диаметром 200–250 мм, приводимых во вращение от электродвигателя. На поверхность кругов надевают или наклеивают шлифовальную шкурку. Методика механического шлифования аналогична методике ручного шлифования. Чтобы получить хорошее качество подготавливаемой поверхности образца, шлифование с самого начала надо вести правильно и аккуратно. Нельзя переходить с крупнозернистой шлифовальной шкурки сразу на мелкозернистую. В этом случае грубые риски полностью не устраняются, промежутки между ними заполняются металлическими опилками, абразивными частицами, и поверхность образца только с виду кажется хорошо подготовленной. После дальнейшей обработки поверхности (полирования, травления) легко растворимые металлические опилки будут удалены, резко выступят грубые риски, которые придется удалять повторным шлифованием.
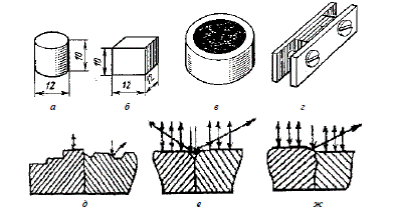
Рис. 3.1. Нормальные размеры металлографических образцов (а и б) и приспособления для монтирования образцов малого размера (в и г). Схема образования контраста в изображении структур: д – формирование контраста; е – граница зерен; ж – избирательное растравливание одной из фаз
Для приготовления шлифов материалов с мягкой основой и твердыми включениями, а также для эффективного удаления деформированного слоя при шлифовке применяют алмазные абразивы. Абразивные частицы одинаково хорошо шлифуют и полируют мягкие и твердые структурные составляющие, поэтому не происходит выкрашивания мелких твердых включений, четко выявляются границы в местах перехода от твердых к мягким слоям.
После окончания шлифования, перед полировкой, образец следует промыть.
Полированием достигается полное удаление рисок и формирование блестящей зеркальной поверхности образца. Полировать можно механическим, химико-механическим и электролитическим способами.
Механическое полирование осуществляют на вращающемся круге диаметром 200–250 мм, обтянутым сукном или фетром. Поверхность круга смачивают полировальным составом. Полировальными составами являются взвешенные в воде мелкие порошки окиси алюминия, окиси хрома, окиси железа и окиси магния. Чаще всего применяют окись хрома или окись алюминия. Чтобы получить хороший результат полирования, не следует сильно прижимать образец к сукну, так как могут произойти деформирование по-
верхностного слоя и искажение структуры, а также быстрое высыхание полировальной жидкости и возможное пригорание поверхности.
Химико-механическое полирование осуществляется с помощью паст, которые наряду с тонкими абразивами содержат вещества, оказывающие химическое воздействие на металл. При этом на поверхности металла образуются тончайшие пленки химических соединений, при шлифовании эти пленки срываются абразивными частицами в первую очередь с выступов. Путем чередования окисления и срыва пленки производится полирование. Для черных сплавов применяют тонкую хромовую пасту ГОИ, в состав которой входят окись хрома, олеиновая кислота, сода, керосин, стеарин и хромоалюми-ниевая паста, содержащая кроме окиси хрома окись алюминия. При полировании пасту наносят на бумагу или сукно. Химико-механическое полирование позволяет получить шлифы лучшего качества, при этом трудоемкость их изготовления снижается.
Электролитическое полирование – это процесс анодного растворения металла в соответствующем электролите. Механически отшлифованный образец в качестве анода помещают в ванну с электролитом напротив катода, которым служит пластина из свинца, нержавеющей стали и т. д. Электролитами являются водные растворы кислот, щелочей, солей.
В результате электрополировки получается блестящая, гладкая, недеформированная поверхность образца. При нарушении режима электрополировки возможно локальное растворение поверхности шлифа или травление без полировки.
После полирования образец промывают водой, полированную поверхность протирают ватой, смоченной спиртом, а затем просушивают прикладыванием фильтровальной бумаги или легким протиранием сухой ватой. Чтобы предохранить полированную поверхность от окисления, образцы хранят в эксикаторе с хлористым кальцием.
Химическое травление – распространенный метод выявления микроструктуры металлов и сплавов. Он основан на различной скорости растворения отдельных участков металлической поверхности, отличающихся по химическому составу или физическому строению. Поверхность шлифа, покрытую травителем, можно рассматривать как гальванический элемент, состоящий из большого числа соединенных между собой микроскопических электродов. Структурные составляющие сплава, имеющие наиболее электроотрицательный потенциал (границы зерен и разных фаз и т. д.), становятся анодами и растворяются в травителе, вызывая потемнение шлифа в этих местах.
Структурные составляющие с более положительным электродным потенциалом являются катодами и при травлении остаются неизменными. После травления гладкая поверхность превращается в совокупность плоскостей и узких впадин между ними, характеризующих микроструктуру сплава.
Угол отражения света, падающего на зеркальную поверхность, равен углу падения. При наличии рельефа на отражающей поверхности (рис. 3.1, д) вместо зеркального отражения происходит рассеивание света. Оптический контраст в изображении структурных составляющих получается за счет того, что в объектив попадает неодинаковое количество света от разных структурных составляющих. Границы между отдельными зернами выявляются в виде тонких темных линий (рис. 3.1, е), образующих сетку. Фазы, имеющие различную скорость растворения, дают контрастную границу за счет избирательного растравливания одной из фаз (рис. 3.1, ж).
Метод химического травления заключается в погружении образца в травитель полированной поверхностью вниз и выдержке оптимальное время. При этом можно совершать покачивания образца, чтобы обеспечить взаимодействие свежего реактива и кислорода воздуха с травимой поверхностью. Если травитель слабо взаимодействует с металлом или образует на поверхности шлифа пленки, препятствующие доступу раствора, применяют метод втирания реактива ватой. Когда полированная поверхность становится слегка матовой, травление считается законченным, и шлиф после травления быстро промывают в проточной воде и просушивают фильтровальной бумагой. В результате травления должно быть четкое выявление микроструктуры. Если структура недостаточно выявлена, следовательно, шлиф недотравлен, и его травят повторно. Если структура получается слишком темная и разъеденная, следовательно, шлиф перетравлен; тогда его нужно снова полировать и травить, уменьшив время выдержки или ослабив травитель. Подготовленный для исследования микроструктуры микрошлиф рассматривают в металлографический микроскоп.
Контрольные вопросы и задания
1. Что такое структура материала?
2. Какие методы исследования используются для изучения макро-, микро- и тонкой структуры материалов?
3. Назовите операции и их последовательность для приготовления микрошлифа.
4. Какие принципы лежат в основе выявления микроструктуры методами травления?
5. Объясните, почему после травления на поверхности микрошлифа возникает система выступов и впадин.
6. Почему границы зерен на микрошлифе выглядят темными полосами?
7. Какими способами осуществляется полирование поверхности микрошлифа?
8. Приведите последовательность механического шлифования стального образца.
9. Какова цель микроанализа?
10. Что позволяет установить микроанализ?
11. Какие элементы структуры позволяет определить микроанализ?
12. Какие особенности строение металла определяют методом микроанализа?
13. Почему при приготовлении шлифов разные участки по-разному травятся?
14. Почему при травлении микрошлифов сначала проявляются границы, а потом и сами зерна?
15. Почему нельзя травить образцы сильной кислотой?
16. Устройство слитков. Что является катодом, а что анодом?
17. К чему может привести сильный перегрев и резкое охлаждение?
18. Чем отличается кристаллическое вещество от аморфного?
19. Чем будут отличаться кривые охлаждения для кристаллического и аморфного вещества?
ЛАБОРАТОРНАЯ РАБОТА №2.
ЧАСТЬ 4. ПОСТРОЕНИЕ ДИАГРАММЫ СОСТОЯНИЯ ОЛОВО–ВИСМУТ. АНАЛИЗ ДИАГРАММ СОСТОЯНИЯ ДВОЙНЫХ СПЛАВОВ
Свойства сплава зависят от многих факторов, но прежде всего они определяются составом фаз и их количественным соотношением. Эти сведения получают из анализа диаграмм состояния. По диаграмме состояния можно представить полную картину формирования структуры, определить оптимальную температуру заливки любого сплава в литейную форму, оценить жидкотекучесть выбранного сплава и возможности получения химической неоднородности, выбрать сплавы и условия для их обработки давлением.
Для построения диаграммы состояния необходимо взять несколько сплавов с разной концентрацией компонентов, а также сами компоненты. Используя метод термического анализа, для каждого компонента и сплава, строятся кривые охлаждения. На них определяются положения критических точек. Зная критические точки большого числа сплавов, приступают к построению диаграммы состояния в координатах температура–
химический состав сплава. Кривые охлаждения для двух компонентов и трех сплавов показаны в левой части рис. 4.1. Техника построения диаграммы состояния сплавов висмут-олово по критическим точкам показана на рис. 4.1.
На горизонтальной оси откладывают концентрацию одного из двух компонентов, образующих сплав. В нашем случае отложена концентрация Sn. В точке, где 0 % Sn, сплав будет однокомпонентным – чистый висмут. Ордината, проведенная через точку 100 % Sn, также отвечает составу чистого компонента – олова.
Затем на оси концентраций находят точки, соответствующие составу каждого сплава. Через эти точки проводят вертикальные прямые, на которых проектируют полученные значения критических температур. На диаграмме эти вертикали обозначены цифрами I, II, III, IV и т. д. Экспериментально построенные диаграммы состояния проверяют по правилу фаз, дающему возможность теоретически обосновать направление процессов превращения для установления равновесного состояния системы. Общие закономерности существования устойчивых фаз, отвечающих условиям равновесия, выражены в математической форме правилом фаз Гиббса. Правило фаз дает возможность предсказать и проверить процессы, происходящие в сплавах при нагреве и охлаждении. Оно показывает, происходит ли процесс кристаллизации при постоянной температуре или в интервале температур и какое число фаз может одновременно существовать в системе.
Диаграммы состояния обычно строят при постоянном атмосферном давлении, и правило фаз выражается уравнением
С = К + 1 – Ф,
где С – число степеней свободы (вариантность) системы, под которым понимают число внешних и внутренних факторов (температура, давление и концентрация), которое можно изменять без изменения числа фаз в системе; К – число компонентов в системе; Ф – число фаз.

Рис. 4.1. Построение диаграммы системы висмут-олово по кривым охлаждения
Проанализируем построенные кривые охлаждения, чтобы установить фазовый состав на отдельных их участках. Кривая охлаждения I относится к чистому висмуту. При температурах выше точки (271 °С) висмут находится в жидком состоянии. На горизонтальном участке кривой 1–1′ идет кристаллизация свинца. Ниже точки 1′(ниже 271 °С) идет охлаждение твердого слитка. Кривая II относится к сплаву с 80 % Bi и 20 % Sn. Кристаллизация начинается в точке 1 (260 °С), из жидкости выделяются кристаллы висмута. Это согласуется с правилом фаз, т. е. число степеней свободы в этом случае равно единице. В данном случае компонентов – два, фазы – две (жидкость и кристаллы висмута). Число степеней свободы в точке 1: С 1 = К – Ф + 1 = 2 – 2 + 1 = 1.
Так как на участке кривой 1–2 из жидкости с понижением температуры выделяются кристаллы висмута, жидкость обогащается оловом. В момент начала выделения кристаллов висмута в точке 1 жидкость сплава содержала 20 % Sn, в точке 2 жидкость уже содержит 57 % Bi и 43 % Sn. Как только достигается это соотношение компонентов, выделение и рост кристаллов висмута прекращаются, а оставшаяся жидкость сплава кристаллизуется в виде смеси мелких кристаллов Bi и α-твердого раствора на основе олова.
Реакция, в результате которой из жидкого сплава при постоянной температуре образуются кристаллы двух фаз, записывается и читается следующим образом: 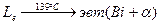 . Жидкая фаза сплава состава точки e при t = 139 °С кристаллизуется в виде смеси кристаллов висмута и альфа-фазы на основе олова – эвтектики. В период эвтектического превращения в равновесии находятся три фазы: жидкая, кристаллы висмута и кристаллы альфа твердого раствора на основе олова, поэтому на участке 2–2′ число степеней свободы
. Жидкая фаза сплава состава точки e при t = 139 °С кристаллизуется в виде смеси кристаллов висмута и альфа-фазы на основе олова – эвтектики. В период эвтектического превращения в равновесии находятся три фазы: жидкая, кристаллы висмута и кристаллы альфа твердого раствора на основе олова, поэтому на участке 2–2′ число степеней свободы
С = К – Ф + 1 = 2 – 3 + 1 = 0.
Система безвариантна (нонвариантна), т. е. температура и число фаз должны оставаться постоянными. Наличие горизонтального участка на кривой охлаждения отражает постоянство температуры. Температура остается постоянной до полного исчезновения одной из фаз – жидкости.
У сплава III, содержащего висмута 57 %, из жидкости при постоянной температуре 139 °С (на участке 1–1′ кривой охлаждения) выделяются два вида кристаллов Bi и α-фаза на основе олова) в виде равномерной смеси. Сплав III называют эвтектическим, он имеет самую низкую температуру кристаллизации (слово эвтектика означает легкоплавкая).
В сплаве с содержанием висмута более 57 % (IV) в точке 1 начинают выделяться кристаллы альфа-фазы на основе олова из жидкости (C = 2 – 2 + 1 = 1), а сплав обогащается висмутом. Когда температура снизится до 139 °С (точка 2), жидкость будет содержать 57 % Bi, и при постоянной температуре образуется эвтектика:
С = К – Ф + 1 = 2 – 3 + 1 = 0.
При температуре ниже эвтектической, состав α-фазы будет изменяться по линии сольвуса, в связи с чем будет избыток кристаллов Bi, который будет выделяться в виде вторичных кристаллов висмута.
Сплав V кристаллизуется по аналогии со сплавом I.
У рассмотренных пяти сплавов значения точек начала и конца кристаллизации наносятся на диаграмму.
Диаграмма состояния представляет собой графическое изображение фазового состава сплавов данной системы в функции температуры и химического состава сплавов.
На диаграмме состояния системы Bi-Sn линия aeb – линия ликвидуса, т. е. геометрическое место всех точек, которые определяют температуру начала кристаллизации сплавов. Линия солидуса cedb соответствует точкам, определяющим температуру конца кристаллизации сплавов.
Сплавы, расположенные левее точки e и имеющие концентрацию висмута менее 57 %, называются доэвтектическими. Процесс их кристаллизации начинается с выделения кристаллов висмута, имеющего избыточную концентрацию по отношению к эвтектике.
Сплавы, содержащие более 57 % висмута и лежащие правее точки e на диаграмме состояния, называются заэвтектическими. Процесс их кристаллизации начинается с выделения сурьмы. У всех сплавов системы Bi-Sn процесс кристаллизации заканчивается при постоянной температуре с образованием эвтектики. Поэтому диаграмма состояния, показанная на рис. 4.1, – одна из простейших для сплавов, образующих эвтектические смеси из чистых компонентов.
Знание диаграмм состояния различных систем, характеризующих превращения в сплавах, и умение анализировать эти превращения позволяют оценить свойства сплавов и в конечном итоге рационально выбрать материал для тех или иных изделий в зависимости от предъявляемых к ним требований.
Диаграммы состояния изображаются в координатах температура–состав компонентов. Линии, соединяющие критические точки аналогичных превращений в системе, разграничивают области существования равновесных фаз. Любая точка на диаграмме определяет фазовый и химическийсоставы сплава, а также его структуру при данной температуре. Вертикальная линия соответствует определенному химическому составу сплава.
В сплаве в процессе кристаллизации могут присутствовать следующие твердые фазы: исходные компоненты; твердые растворы; химические соединения.
Исходные компоненты, образующие сплав, могут не вступать в соединения и химические реакции друг с другом в твердом состоянии. В этом случае каждый компонент после кристаллизации сохраняет свою кристаллическую решетку. Структура сплава представляет собой смесь из зерен отдельных компонентов с пренебрежимо ничтожной взаимной растворимостью.
Твердые растворы – это кристаллы, образовавшиеся в результате распределения атомов одного компонента в кристаллической решетке другого компонента. У твердого раствора кристаллическая решетка одного из компонентов (растворителя) сохраняется, а атомы растворенного компонента располагаются в его решетке, изменяя только ее параметры. Кристаллическая решетка твердых растворов может состоять из атомов двух или нескольких компонентов. Различают твердые растворы замещения, когда атомы растворенного компонента замещают часть атомов растворителя в узлах кристаллической решетки, и твердые растворы внедрения, когда атомы растворенного компонента располагаются в междоузлиях решетки растворителя. Твердые растворы замещения бывают неограниченные и ограниченные, а твердые растворы внедрения, как правило, с ограниченной растворимостью (рис. 4.2).
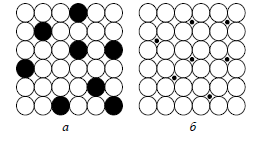
Рис. 4.2. Атомно-кристаллическая структура твердого раствора: а - твердый раствор замещения; б – твердый раствор внедрения
Химические соединения – это соединения, которые имеют:
– свою кристаллическую решетку, отличную от решеток исходных компонентов;
– кратное массовое соотношение элементов, что позволяет выразить их состав формулой А т В п, где А и В – компоненты сплава, а т и п – простые числа;
– постоянную температуру плавления (диссоциации).
В отличие от твердых растворов, химические соединения обычно образуются между компонентами, имеющими большое различие в электронном строении атомов и кристаллических решеток. Если образующиеся в сплавах химические соединения оказываются стойкими веществами, не диссоциирующими при нагреве вплоть до темпера-
туры плавления, то их принято рассматривать в качестве самостоятельных компонентов, способных образовывать сплавы с химическими элементами.
Большое число химических соединений, образующихся в металлических сплавах, отличается по некоторым особенностям от типичных химических соединений, так как не подчиняется законам валентности и не имеет постоянного состава.
В зависимости от того, как взаимодействуют компоненты сплавов между собой в твердом состоянии (обладают различной взаимной растворимостью и образуют твердые растворы, химические соединения, эвтектические смеси), различают несколько типов диаграмм состояния.
ЧАСТЬ 5. МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Краткие теоретические сведения
Механические свойства характеризуют способность материала сопротивляться деформации и разрушению под действием приложенных нагрузок. По характеру изменения во времени действующей нагрузки механические испытания могут быть статическими (на растяжение, сжатие, изгиб, кручение), динамическими (на ударный изгиб) и циклическими (на усталость).
По воздействию температуры на процесс их делят на испытания при комнатной температуре, низкотемпературные и высокотемпературные (на длительную прочность, ползучесть).
Существуют статические испытания, динамические испытания, циклические испытания и испытания на твердость.
Испытания на твердость. Простейшим механическим свойством является твердость. Методы определения твердости в зависимости от скорости приложения нагрузки делятся на статические и динамические, а по способу ее приложения – на методы вдавливания и царапания. Методы определения твердости по Бринеллю, Роквеллу, Виккерсу относятся к статическим методам испытания.
Твердость – это способность материала сопротивляться вдавливанию в него более твердого тела (индентора) под действием внешних сил. При испытании на твердость в поверхность материалов вдавливают пирамиду, конус или шарик (индентор), в связи с чем различают методы испытаний, соответственно, по Виккерсу, Роквеллу и Бринеллю. Кроме того, существуют менее распространенные методы испытания твердости: метод упругого отскока (по Шору), метод сравнительной твердости (Польди) и некоторые другие.
При испытании материалов на твердость не изготавливают стандартных специальных образцов, однако к размерам и поверхности образцов и изделий предъявляются определенные требования.
Твердость по Виккерсу (ГОСТ 2999-75) устанавливают путем вдавливания в металл индентора – алмазной пирамиды с углом при вершине 136о под действием постоянной нагрузки Р: 1; 2; 2,5; 3; 5; 10; 20; 30; 50 или 100 кгс и выдержки под нагрузкой в течение 10–15 с. Для определения твердости черных металлов и сплавов используют нагрузки от 5 до 100 кгс, медных сплавов – от 2,5 до 50 кгс, алюминиевых сплавов – от 1 до 100 кгс. После снятия нагрузки с помощью микроскопа прибора находят длину диагонали отпечатка, а твердость HV рассчитывают по формуле
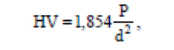
где Р – нагрузка, кгс; d – диагональ отпечатка, мм.
Имеется таблица зависимости твердости от величины нагрузки и длины диагонали. Поэтому на практике вычислений не производят, а пользуются готовой расчетной таблицей. Твердость по Виккерсу HV измеряется в кгс/мм2, Н/мм2 или МПа. Значение твердости по Виккерсу может изменяться от HV 2 060 до HV 5 при нагрузке 1 кгс.
По методу Бринелля вдавливают в образец или изделие стальной закаленный шарик диаметром 10, 5 или 2,5 мм под действием нагрузок 3000, 1 000, 750, 500, 250, 62,5 кгс и др. (ГОСТ 9012-59, рис. 5.1). Полученный круглый отпечаток на образце измеряют под лупой и по таблицам находят величину твердости по Бринеллю, значение которой не превышает 450 НВ. Твердость по Бринеллю почти совпадает со значениями твердости по Виккерсу.
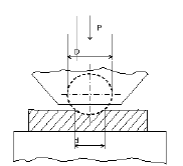
Рис. 5. Схема определения твердости по Бринеллю.
Твердость НВ – это также величина напряжений сопротивления вдавливанию:
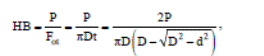
где Р – нагрузка, кгс; Fot – площадь отпечатка, мм2; t – глубина сегмента отпечатка; D – диаметр шарика, мм; d – диаметр отпечатка, мм.
Твердость по Бринеллю НВ (по умолчанию) имеет размерность кгс/мм2, например, твердость алюминиевого сплава равна 70 НВ. При нагрузке, определяемой в ньютонах, твердость по Бринеллю измеряется в МПа. Например, твердость отожженной стали равна 207 НВ при нагрузке 3 000 кгс, диаметре шарика 10 мм, диаметре отпечатка 4,2 мм или, учитывая коэффициент перевода: 1 Н = 9,8 кгс, НВ = 2 028 МПа.
По методу Роквелла (ГОСТ 9013-59) вдавливают алмазный конус с углом при вершине 120о (шкалы А и С) или стальной шарик диаметром 1,5875 мм (шкала В).
При этом определяют твердость, соответственно, HRA, HRC и HRB. В настоящее время измерение твердости по методу Роквелла является наиболее распространенным методом, потому что при использовании твердомеров Роквелла не требуется измерять отпечаток, число твердости считывается со шкалы прибора сразу после снятия основной нагрузки. Метод заключается во вдавливании в испытуемый образец индентора под действием двух последовательно прикладываемых нагрузок – предварительной Р0 и основной P1, которая добавляется к предварительной, так что общая нагрузка Р = Р0 + Р1.
После выдержки в течение нескольких секунд основную нагрузку снимают и измеряют остаточную глубину проникновения индентора, который при этом продолжает находиться под действием предварительной нагрузки. Перемещение основной стрелки индикатора на одно деление шкалы соответствует перемещению индентора на 0,002 мм, которое принимается за единицу твердости.
На рис. 5.2 представлена схема измерения твердости по методу Роквелла алмазным или твердосплавным конусом. При испытаниях измеряют глубину восстановленного отпечатка. Шкалы А и С между собой совпадают, поскольку испытания проводят одним и тем же индентором – алмазным конусом, но при разных нагрузках: 60 и 150 кгс соответственно. Твердость в этом случае определяется как
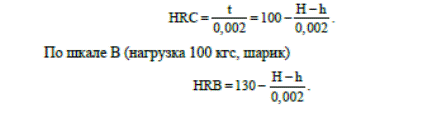
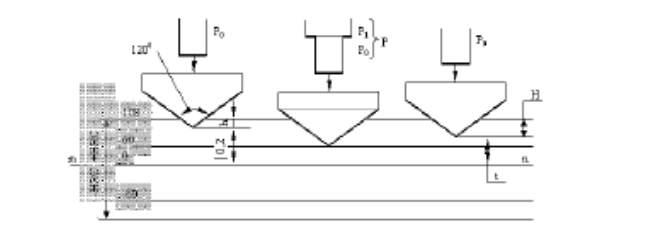
Рис. 5.2. Схема определения твердости по Роквеллу
На практике значения твердости по Роквеллу не рассчитываются по формулам, а считываются с соответствующей (черной или красной) шкалы прибора. Шкалы HRC и HRA используются для высокой твердости, HRB – для низкой. Число твердости по Роквеллу измеряют в условных единицах, оно является мерой глубины вдавливания индентора под определенной нарузкой.
Контрольные вопросы
1. Охарактеризовать типы механических испытаний.
2. Как определить твердость по Бринеллю? Каковы условия испытаний, значения твердости?
3. Как определить твердость по Роквеллу? Каковы условия испытаний, значения твердости?
4. Как определить твердость по Виккерсу? Каковы условия испытаний, значения твердости?
5. Записать единицы измерения твердости по Бринеллю, Роквеллу и Виккерсу.
Date: 2015-09-18; view: 5201; Нарушение авторских прав