
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Химические источники энергии
|
|
711. Гальванические элементы – устройства, преобразующие химическую энергию в электрическую. Простейшим гальваническим элементом является элемент Даниэля-Якоби, разработанного в 1836 году. Элемент Даниэля-Якоби представляет собой медно-цинковый элемент. Медный и цинковый электроды погружены в растворы своих солей и образуют полуэлементы, их разграничивает пористая перегородка, препятствующая смешению растворов, но пропускающая сульфат-анионы.
анод (-) Zn|ZnSO4, H2O||CuSO4 , H2O |Cu(+) катод
(-) Zn – 2e- = Zn2+
(+) Cu2+ + 2e- = Cu
Zn + Cu2+ = Zn2+ + Cu
Источником электрического тока при работе этого элемента является пространственно разделенная окислительно-восстановительная реакция вытеснения более активного металла менее активным из его соли.
712. При работе гальванических элементов стандартными называют условия Т = 298 К, Р = 1.013*105 Па, концентрация катионов соли в растворе – 1 г-ион/л. Элемент Даниэля-Якоби представляет собой медно-цинковый элемент. Медный и цинковый электроды погружены в растворы своих солей и образуют полуэлементы, их разграничивает пористая перегородка, препятствующая смешению растворов, но пропускающая сульфат-анионы.
анод (-) Zn|ZnSO4, H2O||CuSO4 , H2O |Cu(+) катод
(-) Zn – 2e- = Zn2+
(+) Cu2+ + 2e- = Cu
Zn + Cu2+ = Zn2+ + Cu
ЭДС = E0(Cu2+/Cu) - E0(Zn2+/Zn) = 0.34 – (-0.76) = 1.10 В.
713. Электрод – металлическая пластина,контактирующая с электролитом, являющаяся передатчиком электронов от восстановителя к внешнему проводнику и от внешнего проводника к окислителю. Положительно заряжен катод, на котором протекает реакция восстановления (Cu2+ + 2e- = Cu). Отрицательно заряжен анод, на котором протекает реакция окисления (Zn - 2e- = Zn2+).
714. В основу работы гальванического элемента можно положить реакции: Zn + Cu2+ = Zn2+ + Cu, Fe + Pb2+ = Fe2+ + Pb, KMnO4 + FeSO4 + H2SO4 = MnSO4 + Fe2(SO4)3 + K2SO4 + H2O, K2Cr2O7 + K2SO3 + H2SO4 = Cr2(SO4)3 + K2SO4 + H2O.
анод (-) Zn|ZnSO4, H2O||CuSO4 , H2O |Cu(+) катод
(-) Zn – 2e- = Zn2+
(+) Cu2+ + 2e- = Cu
Zn + Cu2+ = Zn2+ + Cu
715. В основе расчета ЭДС лежит термодинамический принцип.
анод (-) Zn|ZnSO4, H2O||CuSO4 , H2O |Cu(+) катод
(-) Zn – 2e- = Zn2+
(+) Cu2+ + 2e- = Cu
Zn + Cu2+ = Zn2+ + Cu
ЭДС = E0(Cu2+/Cu) - E0(Zn2+/Zn) = 0.34 – (-0.76) = 1.10 В.
(-)Zn|ZnSO4||AgNO3|Ag(+)
Cн(ZnSO4)=0.01н., Cн(AgNO3)=0.1н.,T = 27oC =300 K
(-) Zn – 2e- = Zn2+
(+) Ag1+ + 1e- = Ag Zn +2Ag1+ = Zn2+ + Ag
[Zn2+] = Cм(ZnSO4) = Сн/2 = 0.01/2 = 0.005 моль/л
[Ag+] = Cм(AgNO3) = Сн = 0.1 моль/л
ЭДС = E(Ag+/Ag) - E(Zn2+/Zn) = E0(Ag+/Ag) - E0(Zn2+/Zn) + 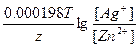 = -0.8 – (-0.76) +
= -0.8 – (-0.76) + 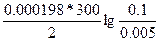 = 1.58B
= 1.58B
716.
| Дано: Cн(ZnSO4)=0.01н. Cн(AgNO3)=0.1н. T = 27oC =300 K ЭДС =?. | (-)Zn|ZnSO4||AgNO3|Ag(+)
(-) Zn – 2e- = Zn2+
(+) Ag1+ + 1e- = Ag Zn +2Ag1+ = Zn2+ + Ag
[Zn2+] = Cм(ZnSO4) = Сн/2 = 0.01/2 = 0.005 моль/л
[Ag+] = Cм(AgNO3) = Сн = 0.1 моль/л
ЭДС = E(Ag+/Ag) - E(Zn2+/Zn) = E0(Ag+/Ag) - E0(Zn2+/Zn) + 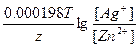 = -0.8 – (-0.76) + = -0.8 – (-0.76) + 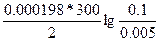 = 1.58B = 1.58B
|
717.
| Дано: Cн(Mg(NO3)2)=0.2н. Cн(SnSO4) = 0.03н. T = 17oC = 290 K ЭДС =?. | (-)Mg|Mg(NO3)2||SnSO4|Sn(+)
(-) Mg – 2e- = Mg2+
(+) Sn2+ + 2e- = Sn Mg + Sn2+ = Mg2+ + Sn
[Mg2+] = Cм(Mg(NO3)2) = Сн/2 = 0.2/2 = 0.1 моль/л
[Sn2+] = Cм(SnSO4) = Сн/2 = 0.03/2 = 0.015 моль/л
ЭДС = E(Sn2+/Sn) - E(Mg2+/Mg) = E0(Sn2+/Sn) - E0(Mg2+/Mg) + 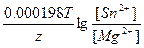 = -0.14 + 2.37 + = -0.14 + 2.37 + 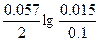 = 2.21 В. = 2.21 В.
|
718.
| Дано: Cн(Fe(NO3)2)=0.03н. Cн(Pb(NO3)2)=0.1н. T = 37oC = 310 K ЭДС =?. | (-)Fe|Fe(NO3)2|| Pb(NO3)2|Pb(+)
(-) Fe – 2e- = Fe2+
(+) Pb2+ + 2e- = Pb Fe + Pb2+ = Fe2+ + Pb
[Fe2+] = Cм(Fe(NO3)2) = Сн/2 = 0.03/2 = 0.015 моль/л
[Pb2+] = Cм(Pb(NO3)2) = Сн/2 = 0.1/2 = 0.05 моль/л
ЭДС = E(Pb2+/Pb) - E(Fe2+/Fe) = E0(Pb2+/Pb) - E0(Fe2+/Fe) + 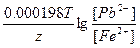 = -0.13 + 0.45 + = -0.13 + 0.45 + 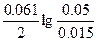 = 0.34 В. = 0.34 В.
|
719.
| Дано: Cн(MnCl2)=0.01н. Cн(CdCl2)= 0.5н. T = 25oC = 298 K ЭДС =?. | (-)Mn|MnCl2||CdCl2|Cd(+)
(-) Mn – 2e- = Mn2+
(+) Cd2+ + 2e- = Cd Mn+ Cd2+=Mn2+ +Sn
[Mn+] = Cм(MnCl2) = Cн/2 = 0.01/2 = 0.005 моль/л
[Cd2+] = Cм(CdСl2) = Сн/2 = 0.05/2 = 0.025 моль/л
ЭДС = E(Cd2+/Cd) - E(Mn2+/Mn) = E0(Cd2+/Cd) - E0(Mn2+/Mn) + 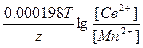 = -0.40 + 1.17 + = -0.40 + 1.17 + 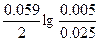 = 0.749 В. = 0.749 В.
|
720.
| Дано: Cн(NiCl2) = 0.04н. Cн(CuCl2)= 0.08н. T = 65oC = 338 K ЭДС =?. | (-)Ni|NiCl2||CuCl2|Cu(+)
(-) Ni – 2e- = Ni2+
(+) Cu2+ + 2e- = Cu Ni + Cu2+ = Ni2+ + Cu
[Ni2+] = Cм(NiCl2) = Сн/2 = 0.04/2 = 0.02 моль/л
[Сu2+] = Cм(CuCl2) = Сн /2= 0.08/2 = 0.04 моль/л
ЭДС = E(Cu2+/Cu) - E(Ni2+/Ni) = E0(Cu2+/Cu) - E0(Ni2+/Ni) + 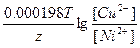 = 0.34 + 0.25 + = 0.34 + 0.25 + 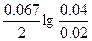 = 0.6 В. = 0.6 В.
|
721.
| Дано: Cн(Cd(NO3)2)=0.06н. Cн(AgNO3) = 0.05н. T = 57oC = 330 K ЭДС =?. | (-)Cd|Cd(NO3)2||AgNO3|Ag(+)
(-) Cd – 2e- = Cd2+
(+) Ag+ + e- = Ag
Cd + 2Ag+ = Cd2+ + 2Ag Cd + 2AgNO3 = Cd(NO3)2 + 2Ag
[Cd2+] = Cм(Cd(NO3)2) = Сн/2 = 0.06/2 = 0.03 моль/л
[Ag+] = Cм(AgNO3) = Сн = 0.05 моль/л
ЭДС = E(Ag+/Ag) - E(Cd2+/Cd) = E0(Ag+/Ag) - E0(Cd2+/Cd) + 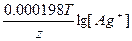 - - 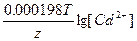 = 0.8 + 0.4 + = 0.8 + 0.4 + 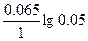 - - 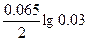 = 1.15 В = 1.15 В
|
722.
| Дано: Cн(Sn(NO3)2)=0.07н. Cн(Hg(NO3)2)=0.09н. T = 23oC = 290 K ЭДС =?. | (-)Sn|Sn(NO3)2||Hg(NO3)2|Hg(+)
(-) Sn – 2e- = Sn2+
(+) Hg2+ + 2e- = Hg
Sn + Hg2+ = Sn2+ + Hg Sn + 2Hg(NO3)2 = Sn(NO3)2 + Hg
[Sn2+]= Cм(Sn(NO3)2) = Сн/2 = 0.07/2 = 0.035 моль/л
[Hg2+]= Cм(Hg(NO3)2) = Сн/2 = 0.09/2 = 0.045 моль/л
ЭДС = E(Hg2+/Hg) - E(Sn2+/Sn) = E0(Hg2+/Hg) - E0(Sn2+/Sn) + 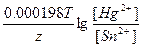 = 0.79 + 0.14 + = 0.79 + 0.14 + 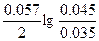 = 0.94 В = 0.94 В
|
723.
| Дано: Cн(Al2(SO4)3)=0.3н. Cн(Bi(NO3)3)=0.3н. T = 33oC = 310 K ЭДС =?. | (-)Al|Al2(SO4)3||Bi(NO3)3|Bi(+)
(-) Al – 3e- = Al3+
(+) Bi3+ + 3e- = Bi
Al + Bi3+ = Al3+ + Bi
[Al3+]= Cм(Al2(SO4)3) = Сн/3 = 0.3/3 = 0.1 моль/л
[Bi3+]= Cм(Bi(NO3)3) = Сн/3 = 0.3/3 = 0.1 моль/л
ЭДС = E(Bi3+/Bi) - E(Al3+/Al) = E0(Bi3+/Bi) - E0(Al3+/Al) + 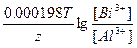 = 0.2 + 1.62 + = 0.2 + 1.62 + 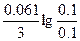 = 1.82 В = 1.82 В
|
724.
| Дано: Cн(CaCl2) = 0.5 н. Cн(H2SO4)=0.02н. T = 20oC = 293 K ЭДС =?. | (-)Ca|CaCl2||H2SO4|H2(Pt)(+)
(-) Сa – 2e- = Ca2+
(+) 2H+ + 2e- = H2
Ca + 2H+ = Ca2+ + H2
[Ca2+] = Cн(CaCl2) = 0.5 н = 0.25 моль/л
[Н+] = 2Cн(H2SO4) = 0.04 н = 0.02 моль/л
ЭДС = E(H+/H2) - E(Ca2+/Ca) = E0(H+/H2) - E0(Ca2+/Ca) + 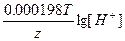 - - 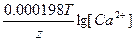 = 0 + 2.87 + = 0 + 2.87 + 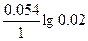 - -  = 2.79 В. = 2.79 В.
|
725.
| Дано: Cн(Li2SO4) = 0.1н Cн(AgNO3) = 0.1н T = 0oC = 273 K ЭДС =?. | (-)Li|Li2SO4||AgNO3|Ag(+)
(-) Li – 1e- = Li+
(+) Ag+ + 1e- = Ag Li + Ag+ = Li+ + Ag
[Li+] = 2Cм(Li2SO4) = Сн = 0.1 моль/л
[Ag+] = Cм(AgNO3) = Сн = 0.1 моль/л
ЭДС = E(Ag+/Ag) - E(Li+/Li) = E0(Ag+/Ag) - E0(Li+/Li) + 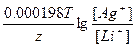 = 0.8 + 3.02 + = 0.8 + 3.02 + 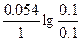 = 3.82 В. = 3.82 В.
|
726. Гальванический элемент с максимальным значением ЭДС: (-)Li|Li2SO4||AuNO3|Au(+) ЭДС = Eo(Au+/Au) - Eo(Li+/Li) = 1.68+3.02 = 4.7 В
727.
| А) Медь – анод. (-)Cu|CuSO4||Ag2SO4|Ag(+) E = E0(Ag+/Ag) - E0(Cu2+/Cu) = 0.8 – 0.34 = 0.46 В. |
| Б) Медь – катод. (-)Fe|FeSO4||СuSO4|Cu(+) E = E0(Cu2+/Cu) - E0(Fe2+/Fe) - = 0.34 + 0.45 = 0.79 В. |
728. KMnO4 + FeSO4 + H2SO4 = MnSO4 + Fe2(SO4)3 + K2SO4 + H2O.
| (-)Fe|Fe2+,Fe3+||MnO4-, Mn2+|Fe(+) |
729. K2Cr2O7 + K2SO3 + H2SO4 = Cr2(SO4)3 + K2SO4 + H2O.
| Cr2O72-,Cr3+:φ0 = 1.33 B, SO32-, SO42-: φ0 = 0.17 B |
| (-)Pt| SO32-, SO42-, H+|| Cr2O72-,Cr3+, H+ |Pt(+) |
730.
| (-)Pt, H2| H+|| H+ | H2, Pt(+) |
| pH1 =4 pH2 = 2 |
pH = -lgC(H+), C1(H+) = 10-2 , C2(H+) = 10-4 . E0 (H2/H+) = 0 B.
E = 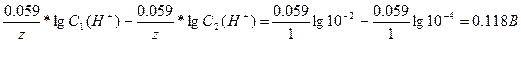
731. Концентрационные элементы – гальванические элементы, образованные одинаковыми электродами, опущенными в растворы своих солей разной концентрации.
| (-)Cu| CuSO4(C1 = 0.1%)|| CuSO4(C2 = 5.0%) | Cu (+) |
| ЭДС = (0.059/z)*lg(C2/C1) = (0.059/2)lg(5/0.1) = 0.05 В. |
732. Топливный элемент – это гальванический элемент, в котором в качестве активного материала отрицательного электрода используются либо природное топливо (природный газ, содержащий углеводород), либо водород, окись углерода и др. восстановители. Активным материалом положительного материала служит кислород. Токообразующая реакция сводится к окислению топлива.
Водород-кислородный ТЭ разделен электродами на три плоскости – водородную, кислородную и промежуточную, заполненную электролитом. Электроды изготовлены из пористого никеля, электролитом является раствор КОН, водород и кислород подаются под давлением 30-75 атм. Элемент работает при Т=2000 С. Схема: (-)Н2| КОН, Н2О| O2(+)
Анод: 2Н2 – 4е- + 4ОН- = 4Н2О, катод: О2 + 4е- + 2Н2О = 4ОН-
Общая реакция: 2Н2 + О2 = 2Н2О.
733. Аккумуляторы – химические источники тока, которые могут быть использованы многократно. Их работоспособность восстанавливается многократно, т.к. в основе их действия лежат химически обратимые процессы. Свинцовый аккумулятор состоит из чередующихся пластин, одна из которых представляет собой PbO2, а вторая – металлический свинец в виде пористой губки. Пластины погружены в 35-40% раствор серной кислоты. Электрохимическая схема заряженного аккумулятора: (+)PbO2|H2SO4,H2O|Pb(-)
При работе (разрядке) протекают реакции: (+)Pb –2e - + SO42- = PbSO4 , (-)PbO2 +2e - + SO42- + 4H+ = PbSO4 + 2H2O.
Электрохимическая схема разряженного аккумулятора: (-)PbSO4|H2SO4,H2O|PbSO4(+)
Протекают процессы: (-)PbSO4+2e - = Pb- + SO42, (+)PbSO4 -2e - + 2H2O.= PbO2+ + SO42- + 4H+
734.
| Дано: E(Zn2+/Zn)=-0.81В C(ZnCl2) = 0.07 м. a(ZnCl2) =?. | E(Zn2+/Zn) = Eo(Zn2+/Zn) + 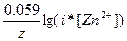 = -0.76 + (0.059/2) * lg(i*0.07) = -0.81, следовательно, i = 1.8. a = (i-1)(m-1) = (1.8-1)/(2-1) = 0.8 = 80%, где m – количество ионов, на которые диссоциирует электролит. = -0.76 + (0.059/2) * lg(i*0.07) = -0.81, следовательно, i = 1.8. a = (i-1)(m-1) = (1.8-1)/(2-1) = 0.8 = 80%, где m – количество ионов, на которые диссоциирует электролит.
|
735.
| Дано: E(Ag+/Ag) = 0.59 В S(Ag2CrO4) =?. | E(Ag+/Ag) = Eo(Ag+/Ag) + 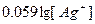 = 0.8 + 0.059*lg[Ag+] = 0.59, следовательно, [Ag+] = 2.8*10-4 м. S = = 0.8 + 0.059*lg[Ag+] = 0.59, следовательно, [Ag+] = 2.8*10-4 м. S = 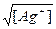 = 1.66*10-2 = 1.66*10-2
|
736.
| Дано: E(Ag+/Ag)=0.51 В ПР(AgСl) =?. | E(Ag+/Ag) = Eo(Ag+/Ag) + 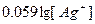 = 0.8 + 0.059*lg[Ag+] = 0.51, следовательно, [Ag+] = S = 1.2*10-5 м. ПР = S2 = 1.47*10-10 (S-растворимость) = 0.8 + 0.059*lg[Ag+] = 0.51, следовательно, [Ag+] = S = 1.2*10-5 м. ПР = S2 = 1.47*10-10 (S-растворимость)
|
737.
| (-)Mg|Mg2+||Ag+|Ag(+) E = E0(Ag+/Ag) - E0(Mg2+/Mg) = 0.8 + 2.37 = 3.17 B ΔG0 = -zFE = -2*96500*3.17 = -611.81 кДж/моль ΔG0 = -RTlnKp = 8.31*298*lnKp = 611.81, следовательно, Кр = 1.28 |
738.
| (-)Fe|Fe2+||Cu2+|Cu(+) E = E0(Cu+2/Cu) - E0(Fe2+/Fe) = 0.34 - (-0.45) = 0.79 B ΔG0 = -zFE = -2*96500*0.79 = -152.5 кДж/моль ΔG0 = -RTlnKp = 8.31*298*lnKp = 152.5, следовательно, Кр = 5.5*1026. |
739.
| Дано: Cм(FeSO4)=1м. ЭДС = 0 В. Cм(CdSO4) =?. | (-)Fe|FeSO4||CdSO4|Cd(+)
ЭДС = E(Fe2+/Fe) - E(Cd2+/Cd) = E0(Fe2+/Fe) - E0(Cd2+/Cd) + 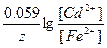 .
0= -0.40 + 0.45 + .
0= -0.40 + 0.45 + 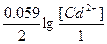 , следовательно, [Cd2+] = Cм(CdSO4) =0.02 м. , следовательно, [Cd2+] = Cм(CdSO4) =0.02 м.
|
Date: 2015-09-18; view: 533; Нарушение авторских прав