
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Испарение жидкостей. Давление насыщенного пара
|
|
Жидкость, налитая в открытый сосуд, испаряется из него. При этом молекулы, оторвавшиеся от поверхности жидкости за счёт конвективных потоков и броуновского движения, уходят в окружающее пространство, а на их место из жидкости вылетают всё новые и новые молекулы. Таким образом, над поверхностью жидкости образуется насыщенный пар и процесс испарения протекает до тех пор, пока вся жидкость не испарится.
Для того чтобы молекула оторвалась от поверхности жидкости, она должна иметь кинетическую энергию примерно в 10 раз большую, чем средняя кинетическая энергия молекул жидкости.
В закрытом сосуде кроме испарения будет протекать процесс конденсации паров. При этом в начальный момент времени скорость испарения будет больше скорости конденсации. Но с увеличением числа молекул в единице объёма скорость испарения уменьшается, а скорость конденсации возрастает. В какой-то момент скорость испарения становится равной скорости конденсации. Такое состояние жидкости и пара называется динамическим равновесием. Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным.
Давление насыщенного пара зависит от природы жидкости и её абсолютной температуры. Зависимость давления пара от температуры можно выразить формулой, вытекающей из уравнения Клаузиса-Клайперона.
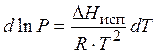 . (53)
. (53)
Если принять в первом приближении, что теплота испарения с изменением температуры остаётся величиной постоянной (что справедливо для области температур, которой отвечают невысокие значения давления пара), то интегрируя уравнение, получим:
 , (54)
, (54)
где С – постоянная интегрирования.
Если же мы будем интегрировать уравнение в пределах от Т 1 до Т 2 и соответственно от Р 1 до Р 2, то получим уравнение вида:
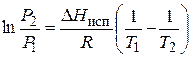 (55)
(55)
или, перейдя к десятичному логарифму, получим:
 . (56)
. (56)
Это уравнение линейное и может быть использовано для определения давления пара данной жидкости при заданной температуре, если известны значение давления пара при другой температуре и мольная теплота испарения.
Из полученных уравнений видно, что с повышением температуры жидкости давление пара увеличивается. С увеличением мольной теплоты испарения давление пара уменьшается, т. к. уменьшается летучесть жидкости.
На практике очень часто приходится иметь дело с различными смесями горючих жидкостей. Различают следующие смеси двух и более жидкостей:
1. смеси жидкостей, хорошо растворимых друг в друге;
2. смеси жидкостей, частично растворимых друг в друге;
3. смеси жидкостей, не растворимых друг в друге.
Давление пара смесей нерастворимых друг в друге жидкостей определяется как сумма давлений компонентов смеси по формуле:
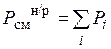 , (57)
, (57)
где  - давление пара смеси не растворимых друг в друге жидкостей,
- давление пара смеси не растворимых друг в друге жидкостей,
Рi – давление пара i- компонента.
Расчёт давления пара смеси жидкостей, растворимых друг в друге, ведётся по формуле:
 , (58)
, (58)
где 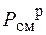 - давление пара смеси жидкостей, растворимых друг в друге;
- давление пара смеси жидкостей, растворимых друг в друге;
ri – мольная доля i компонента, причём  .
.
Мольная доля каждого компонента может быть определена по формуле
 , (59)
, (59)
где g 1, g 2, g 3 …gi – весовой процент каждого компонента в жидкой фазе;
M 1, M 2, M 3 – молекулярные массы компонентов.
ПРИМЕР: Вычислить давление пара толуола при температуре 17°С, если при температуре 30°С давление насыщенных паров его равно 37,2 мм рт. ст. Мольная теплота испарения толуола 32880 Дж/моль.
Решение:
Из уравнения (50) выразим lg P 1
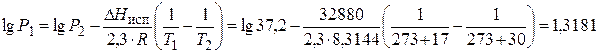 .
.
Отсюда Р 1 = 20,8 мм рт. ст.
Ответ: при температуре 17 °С давление насыщенных паров толуола составит 20,8 мм рт. ст.
Давление насыщенного пара при заданной температуре можно определить по номограмме (рис. 3). В середине номограммы находится шкала давления пара, общая для всех веществ. Справа и слева от неё – шкалы температур. По обе стороны от шкалы давления расположены точки, каждая из которых соответствует определённому веществу. Например, №19 –керосину и декану, №32 – этиленгликолю и т. д. Нахождение давления пара жидкости сводится к тому, что через точку, отвечающую заданному веществу, и точку заданной температуры проводится прямая до пересечения её со шкалой давления пара. Точка пересечения этой прямой со шкалой давления и даст значение давления пара при заданной температуре. Для нахождения точных значений давления насыщенных паров или температурных пределов необходимо уметь находить цену деления в конкретных интервалах давлений насыщенных паров по формуле
 . (60)
. (60)
ПРИМЕР: Определить давление пара воднобензольной эмульсии при температуре 20°С.
Решение:
1. По номограмме № 1 (рис. 3) для определения давления насыщенного пара находим значения давления насыщенных паров бензола и воды при температуре 20 °С.
Давление насыщенных паров бензола при температуре 20 °С составило 9,31 кПа, давление насыщенных паров воды составило 2,39 кПа.
2. Поскольку вода и бензол при смешивании образуют эмульсию, т. е. взаимно нерастворимы, давление насыщенных паров рассчитывается по формуле 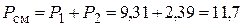 (кПа).
(кПа).
Ответ: давление пара воднобензольной эмульсии при температуре 20 °С составило 11,7 кПа.
ПРИМЕР: О пределить давление насыщенных паров спиртовой смеси при температуре 10 °С. Состав смеси в весовых процентах: этанола – 30 %, метанола – 20 %, пропанола – 50 %.
Решение:
1. Определяем давление насыщенного пара каждого компонента смеси по номограмме:
Р н.п.(СН4О) = 7,315 кПа; Р н.п . (С2Н6О) = 1,995 кПа; Р н.п.(С3Н8О)=0,931 кПа.
2. Определяем молекулярные массы компонентов:
М (СН4О)=32 у. ед.; М (С2Н6О)=46 у. ед.; М (С3Н8О = 60 у. ед.
3. Определяем мольные доли компонентов:
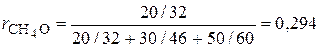 ;
;
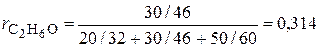 ;
;
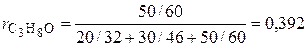 .
.
4. Определяем давление паров смеси растворимых друг в друге жидкостей.
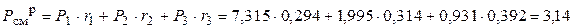 (кПа).
(кПа).
Ответ: давление паров спиртовой смеси при 10°С составило 3,14 кПа.


Рис. 3. Номограмма № 1 для определения давления насыщенного пара жидкостей
ПРИМЕР: определить, будет ли опасной концентрация паров этилового спирта в мернике при температуре 270 К и общем давлении 101,3 кПа.
Решение:
1. Определяем давление паров этилового спирта при температуре 270 К (по номограмме № 1 рис. 3) Р = 13,32 кПа.
2. Определяем фактическую концентрацию паров этилового спирта:
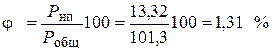 .
.
3. По справочным данным определяем область воспламенения этилового спирта:
jн = 3,28 % jв = 18,95 %.
4. Сравниваем j и jн: j = 1,31 % < jн = 3,28 %, следовательно определяем ПДВК.
ПДВК ≤ Кбез × j н = 0,5 × 3,28 = 1,64 %.
Кбез = 0,5, т.к. мерник – аппарат без источников зажигания.
5. Сравниваем j с ПДВК и делаем вывод: j = 1,31 < ПДВК, следовательно концентрация безопасна.
Ответ: концентрация паров этилового спирта в мернике при температуре 270 К и давлении 101,3 кПа будет безопасной.
Для определения мест расположения устройств вытяжной вентиляции при работе с жидкостями необходимо знать плотность их паров по воздуху, т.е. вес их относительно воздуха.
Плотность пара по воздуху определяется по формуле
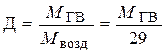 , (61)
, (61)
где М ГВ – молярная масса горючего вещества, кг/кмоль.
Если Д >1, то пары тяжелее воздуха и будут скапливаться в нижней части помещения, вентиляционные устройства следует располагать внизу.
Если Д < 1, то пары легче воздуха и будут скапливаться в верхней части помещения, вентиляционные устройства следует располагать вверху.
ПРИМЕР: Определить место расположения устройств вытяжной вентиляции при работе с бензолом.
Решение:
1. Определяем молярную массу бензола: М (С6Н6) = 6×12 + 6 ×1 = 78 (кг/кмоль).
2. Определяем плотность пара по воздуху:
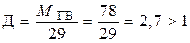 пары тяжелее воздуха и скапливаются в нижней частипомещения.
пары тяжелее воздуха и скапливаются в нижней частипомещения.
Ответ: устройства вытяжной вентиляции при работе с бензолом должны быть расположены в нижней части помещения.
Date: 2015-08-15; view: 7531; Нарушение авторских прав