
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт 1. Влияние среды на окислительно-восстановительные реакции
|
|
В три пробирки налью по 2-3 мл раствора перманганата калия KMnO4. В первую пробирку прилью 1-2 мл разбавленной серной кислоты H2SO4, во вторую 1-2 мл воды, в третью - 1-2 мл концентрированного раствора щелочи (NaOH или KOH).
В каждую пробирку добавлю по 2-3 мл свежеприготовленного раствора сульфита натрия Na2SO3. Отмечу наблюдения. (Учтите, что фиолетовая окраска характерна для ионов MnO4-, бесцветная или слабо-розовая для ионов Mn2+, зеленая - для ионов MnO42-, бурый цвет имеет осадок MnO2).
1. Уравнения реакций взаимодействия KMnO4 с Na2SO3
a) в кислой среде:
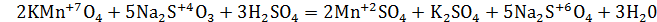
окислитель восстановитель среда
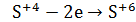 5 - восстановитель
5 - восстановитель
Mn+7 + 5e → Mn+2 2 - окислитель
b) в щелочной среде:

окислитель восстановитель среда
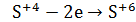 1 - восстановитель
1 - восстановитель
Mn+7 + 1e → Mn+6 2 - окислитель
c) в нейтральной среде:
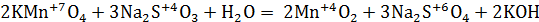
окислитель восстановитель среда
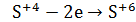 3 - восстановитель
3 - восстановитель
Mn+7 + 3e → Mn+4 2 - окислитель
2. Вывод о характерной степени окисления марганца
· в кислой среде: Mn+7 → Mn+2
· в щелочной среде: Mn+7 → Mn+6
· в нейтральной среде: Mn+7 → Mn+4
Date: 2015-08-15; view: 13692; Нарушение авторских прав