
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Индикаторы комплексонометрии
|
|
В комплексонометрическом титровании конечную точку титрования устанавливают как визуально, так и с использованием инструментальных методов анализа.
При визуальном способе установлении конечной точки применяют металлоиндикаторы (это индикаторы, изменяющие окраску в зависимости от концентрации иона Ме). Металлоиндикаторы – обычно органические соединения, которые с ионами титруемого металла образуют окрашенные комплексы. Их обычно делят на 2 группы:
1) индикаторы, которые сами не имеют окраски, но образуют с ионами Ме окрашенные комплексы (например, при комплексонометрическом титровании Fe(III) в качестве индикатора используют салициловую или сульфосалициловую кислоту, тайрон; при определении Bi(III) – тиомочевину). Комплексы Fe(III) с салициловой кислотой (с молярным соотношением 1:1) окрашены в красный цвет, с тайроном – в зеленый. Тиомочевинные комплексы с Bi (III) окрашены в желтый цвет. Интенсивность окраски образующихся комплексов обычно невысока. Поэтому, чтобы наблюдать окраску комплекса, концентрация индикатора должна быть ≈ в 10 раз больше концентрации титруемого Ме.
2) органические соединения, содержащие в своих молекулах хромофорные группы, следовательно, окрашенные и образующие с ионами Ме внутрикомплексные соединения, по цвету отличающиеся от самих индикаторов. Эти индикаторы называются металлохромные.
Рингбом предложил делить индикаторы на 3 группы:
а) индикаторы, содержащие азогруппу –N=N–. Например, эриохромовый черный Т (при рН 9-10 используется для определения Mg2+, Ba2+, Cd2+, Pb2+, Zn2+, Mn2+, Sr2+); и кислотный хромовый темно-синий (Mn2+, Mg2+, Zn2+, Pb2+, Ca2+);
б) индикаторы, относящиеся к классу трифенилметановых красителей. Например, ксиленоловый оранжевый (при рН 1,5-3: Bi3+, Fe3+; при рН 5-7: Cd2+, Co2+, Cu2+, Hg2+, Zn2+); пирокатехиновый фиолетовый (при рН 2-4:Bi3+, Ti4+; рН 5-6: Cu2+, Fe3+, Pb2+);
в) прочие индикаторы – мурексид (при рН 8-9: Co2+, Ca2+, Zn2+, Ni2+), дитизон, ализарин.
К металлоиндикаторам предъявляется ряд требований:
1 ) должны в выбранной области рН образовывать с ионами Ме достаточно устойчивые комплексы с соотношением Ме:Ind = 1:1. Условные константы устойчивости комплексов MeInd должны быть меньше условных констант устойчивости комплексов данных Ме с ЭДТА, т.е. 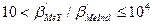 . В свою очередь, достаточно большие значения констант устойчивости комплексов MeInd позволяют использовать небольшие соотношения концентраций индикатора и Ме:
. В свою очередь, достаточно большие значения констант устойчивости комплексов MeInd позволяют использовать небольшие соотношения концентраций индикатора и Ме: 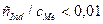 , что соответствует уменьшению погрешности титрования.
, что соответствует уменьшению погрешности титрования.
2) комплекс иона Ме с Ind должен быть кинетически лабильным и быстро разрушаться при добавлении ЭДТА. Считается, что в комплексонометрии можно применять металлоиндикаторы, для которых период полуобмена лигандами в комплексе MeInd равен 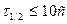 .
.
3) изменение окраски раствора в конечной точке титровании должно быть контрастным. Согласно учению о цвете, предельные цвета, т.е. исходные (окраска чистого МеInd) и конечные (окраска чистого Ind) должны быть по возможности дополнительными – взаимно дополнять друг друга до белого цвета. Дополнительными цветами, например, являются: красный – сине-зеленый; оранжевый – синий; желтый – синий; желто-зеленый – фиолетовый и т.д. Индикатор, окраска которого изменяется от одного дополнительного цвета к другому, в промежуточной точке становится бесцветным (или серым), т.к. цветовые тона взаимно погашают друг друга. Поэтому такую точку особенно легко заметить. Большинство применяемых металлоиндикаторов лишь в редких случаях изменяют свой цвет на дополнительный. Чтобы достичь максимального цветового эффекта, используют смешанные индикаторы, т.е. к металлоиндикатору добавляют индифферентный краситель, создающий цветовой фон, вследствие чего предельные окраски до и после конечной точки титрования становятся дополнительными. Например, для титрования ионов Ca предложена смесь мурексида и нафтолового зеленого В: переход окраски от оливково-зеленой через красновато-серую к чисто синей.
Металлолиганды, как правило, являются многоосновными кислотами и в зависимости от рН могут существовать в виде протонированных и непротонированных форм HIInd, HI-1Ind, …, Ind. Молярную долю любой формы индикатора вычисляют по уравнению:
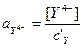 ,
,
где 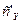 – общая концентрация незакомплексованной ЭДТА, которая равна сумме равновесных концентраций всех форм ЭДТА:
– общая концентрация незакомплексованной ЭДТА, которая равна сумме равновесных концентраций всех форм ЭДТА:

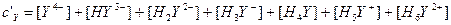 .
.
В большинстве случаев ионы металла и индикатор образуют лишь один комплекс с соотношением 1:1, и тогда условную константу устойчивости этого комплекса с учетом равновесий протонирования индикатора можно записать следующим образом:
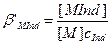
Из этого выражения следует, что
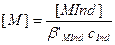
Для ориентировочной оценки интервала изменения цвета индикатора можно принять, что человеческий глаз ощущает переходный цвет в следующем интервале отношении концентраций:
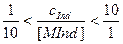
Тогда для границ интервала перехода окраски получаем 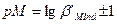 .
.
Таким образом, интервал изменения цвета индикатора на шкале рМ определяется значением условной константы устойчивости комплекса MеInd.
Date: 2015-08-06; view: 1079; Нарушение авторских прав