
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретическое введение. Цель работы: изучение изотопической структуры спектральных линий серии Бальмера в водородном спектре
|
|
ИССЛЕДОВАНИЕ ИЗОТОПНОГО СОСТАВА АТОМАРНОГО ВОДОРОДА
Цель работы: изучение изотопической структуры спектральных линий серии Бальмера в водородном спектре, полученном методом компьютерного моделирования; измерение длин волн изотопических компонентов линий α, β, γ, и δ для трех изотопов водорода (протия, дейтерия и трития); определение значений постоянной Ридберга по данным спектральных измерений, определение минимальной разрешающей способности спектрального прибора, посредством которого представляется возможным анализировать изотопный состав атомарного водорода и однократно ионизированного гелия.
Теоретическое введение
Волновые числа спектральных линий водородоподобных систем определяются в соответствии с эмпирической обобщенной формулой Бальмера
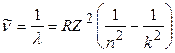 , (1)
, (1)
где R – постоянная Ридберга, экспериментально найденное значение которой для атомов водорода равно 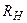 =(109677,576±0,012) см-1.
=(109677,576±0,012) см-1.
В формуле (1) одним из значений 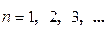 определяются волновые числа конкретной спектральной серии, а одним из возможных значений
определяются волновые числа конкретной спектральной серии, а одним из возможных значений 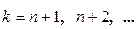 определяется волновое число заданной спектральной линии.
определяется волновое число заданной спектральной линии.
Формула (1) впоследствии была получена теоретически в рамках теории Бора и квантовой механики в предположении, что электрон в водородоподобной системе движется относительно покоящегося ядра, что соответствует допущению о том, что масса ядра бесконечно велика по сравнению с массой электрона. Для постоянной Ридберга при этом было получено выражение
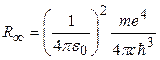 , (2)
, (2)
где m – масса электрона.
Вычисленное в соответствии с формулой (2) значение постоянной Ридберга равно 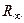 =109737,309 см-1 , что не совпадает с ее экспериментальным значением. Указанное несоответствие устраняется, если рассматривать движение водородоподобной системы, состоящей из ядра и электрона, относительно их центра масс. При этом следует вместо массы электрона
=109737,309 см-1 , что не совпадает с ее экспериментальным значением. Указанное несоответствие устраняется, если рассматривать движение водородоподобной системы, состоящей из ядра и электрона, относительно их центра масс. При этом следует вместо массы электрона 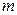 использовать приведенную массу атомной системы
использовать приведенную массу атомной системы 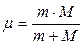 , где
, где 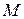 - масса ядра. Следовательно, постоянная Ридберга
- масса ядра. Следовательно, постоянная Ридберга
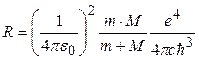 (3)
(3)
и волновые числа спектральных линий, обусловленных идентичными квантовыми переходами (формула (1)) в различных изотопах данного химического элемента характеризуются различными значениями. Это явление названо изотопическим сдвигом.
Из формул (2) и (3) легко получить выражение, посредством которого устанавливается связь
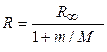 . (4)
. (4)
Химическому элементу водорода соответствуют три изотопа: обычный водород 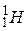 , называемый протием и обозначаемый
, называемый протием и обозначаемый 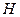 , дейтерий
, дейтерий 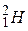 , обозначаемый
, обозначаемый 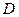 , и тритий
, и тритий 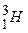 , обозначаемый
, обозначаемый 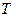 . Ядром атома протия является протон, ядро атома дейтерия состоит из протона и нейтрона, ядро атома трития состоит из протона и двух нейтронов. Наиболее распространенным в природе из изотопов водорода является протий. Относительная концентрация атомов дейтерия и протия в природе составляет ~10-5, а относительная концентрация трития и протия равна ~10-18. Протий и дейтерий являются стабильными изотопами, а тритий подвержен β-распаду. с периодом полураспада 12,26 года. Различием масс ядер изотопов водорода обусловливается различие значений соответствующих постоянных Ридберга
. Ядром атома протия является протон, ядро атома дейтерия состоит из протона и нейтрона, ядро атома трития состоит из протона и двух нейтронов. Наиболее распространенным в природе из изотопов водорода является протий. Относительная концентрация атомов дейтерия и протия в природе составляет ~10-5, а относительная концентрация трития и протия равна ~10-18. Протий и дейтерий являются стабильными изотопами, а тритий подвержен β-распаду. с периодом полураспада 12,26 года. Различием масс ядер изотопов водорода обусловливается различие значений соответствующих постоянных Ридберга
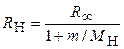 ,
, 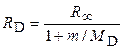 ,
, 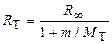 , (5)
, (5)
где 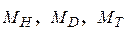 ‒ массы ядер протия, дейтерия и трития.
‒ массы ядер протия, дейтерия и трития.
Длины волн спектральных линий, соответствующих идентичным квантовым переходам в рассматриваемых изотопах, как следует из формул (1) и (5), определяются по формулам
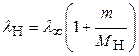 ,
, 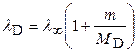 ,
, 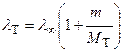 , (6)
, (6)
где 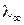 определяется соотношением
определяется соотношением
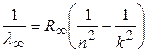 . (7)
. (7)
Из выражений (6) и (7) легко получить формулу для относительной величины изотопического сдвига линий протия и дейтерия
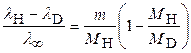 , (8)
, (8)
из которой видно, что относительная величина изотопического сдвига в рассматриваемом случае одинакова для всех спектральных линий и приближенно равна m /(2 m p) ≈ 2,7∙10– 4, где m p ‒ масса протона.
Изотопический сдвиг спектральной линии определенного изотопа относительно ее теоретического значения 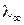 , полученного без учета движения ядра, как следует из выражений (6) и (7), определяется только отношением
, полученного без учета движения ядра, как следует из выражений (6) и (7), определяется только отношением 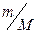 :
:
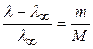 . (9)
. (9)
Date: 2015-07-24; view: 439; Нарушение авторских прав