
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Составление теплового баланса
|
|
Производственные процессы протекают при заданных температурных условиях, причем температура проведения процесса может быть как выше, так и ниже температуры окружающей среды. В основе уравнения теплового баланса любого процесса или аппарата положен закон сохранения энергии, согласно которому количество теплоты ΣQ', поступающей в данный процесс (если в нем нет превращения в другой вид энергии), равно количеству теплоты, выделившейся в процессе ΣQ". Если все тепло или часть его превращается в другой вид энергии, например, в механическую работу или работу электрического тока, то эта работа должна входить в одно из значений ΣQ. В наиболее общем виде уравнение теплового баланса можно представить следующим образом:
Q1 + Q2 + Q3 = Q4 + Q5,
где Q1 - теплота входящих в аппарат веществ, кДж (ккал);
Q2 - теплота физических и химических превращений, протекающих в данном аппарате, кДж (ккал);
Q3 - теплота, необходимая для нагревания аппарата, в котором протекает процесс, кДж (ккал) (сумма этих трех статей теплового баланса составляет приход тепла);
Q4 - теплота выходящих из аппарата продуктов, кДж (ккал);
Q5 - потери тепла в окружающую среду, кДж (ккал) (сумма этих статей дает расход тепла).
Величина Q2 может входить в расход тепла, если она является отрицательной.
Подсчет каждой из указанных величин является одной из главных задач при расчете технологического процесса и аппаратуры.
Теплота входящих в аппарат веществ
Q1 подсчитывается по уравнению:
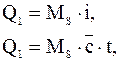
где MS - количество веществ, входящих в аппарат, кг, м3, или моль (берется из данных материального баланса);
i - теплосодержание веществ при данной температуре;
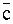 - средняя теплоемкость веществ при температуре их поступления в аппарат;
- средняя теплоемкость веществ при температуре их поступления в аппарат;
t - температура веществ при поступлении их в аппарат.
Величина средней теплоемкости (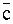 ) должна быть взята или подсчитана в соответствии с величиной MS: если MS взято в килограммах, то
) должна быть взята или подсчитана в соответствии с величиной MS: если MS взято в килограммах, то 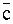 следует взять в кДж/кг (ккал/кг); если MS взято в м3, то
следует взять в кДж/кг (ккал/кг); если MS взято в м3, то 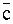 - в Дж/м3 (ккал/м3) и т.д.
- в Дж/м3 (ккал/м3) и т.д.
Значение теплоемкости для большинства веществ зависит от их температуры и давления, а в случае газов оно зависит также и от того, протекает ли данный процесс при постоянном объеме или при постоянном давлении. В большинстве случаев приходится иметь дело не с чистыми веществами, а с их смесями. Теплоемкость и теплосодержание смесей обычно неизвестны, так как в специальных таблицах приводятся теплоемкости и теплосодержание только для чистых веществ. Поэтому в случае подсчета величины Q1 для смесей, состоящих из нескольких компонентов, формула принимает следующий вид:
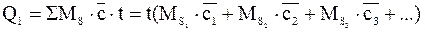
или
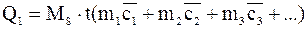
или
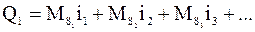
или
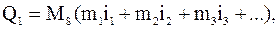
где 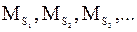 - количество каждого компонента в отдельности;
- количество каждого компонента в отдельности;
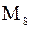 - общее их количество, которое равно:
- общее их количество, которое равно:
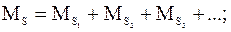
m1, m2, m3,… - доля каждого компонента в единице объема или веса всей их смеси;
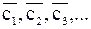 - соответствующие средние теплоемкости;
- соответствующие средние теплоемкости;
i1, i2, i3,… - соответствующие теплосодержания.
Теплота химических и физических превращений
Эта величина включает или теплоту протекающих химических реакций, или теплоту превращения веществ из одного агрегатного состояния в другое (например, из жидкости в пар или твердое тело), или теплоту растворения и т.д., или же и то и другое одновременно. Значения тепловых величин (тепловой эффект реакции, теплоты парообразования и т.д.) всегда берутся из таблиц и диаграмм, где они даются в калориях для определенных условий и отнесены к определенному количеству вещества. Эти табличные данные часто приходится пересчитывать для тех условий работы (температуры и давления), при которых будет работать рассчитываемый аппарат. Величины, входящие в значение Q2, могут быть положительны и отрицательны.
Положительные значения этих величин следует относить к приходу тепла, отрицательные - к расходу.
Теплоту химических реакций, выражающуюся количеством тепла, которое выделяется или поглощается при их протекании, определяют чаще всего с помощью закона Гесса, математическая интерпретация которого приводит к простому равенству:
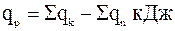
где qp – теплота реакции, кДж/моль (ккал/моль);
Σqk – сумма теплот образования из элементов, образовавшихся в результате химического взаимодействия, кДж/моль;
Σqn – сумма теплот образования из элементов соединений, вступающих в химическое взаимодействие, кДж/моль.
Таким образом, вычисление теплот химических реакций сводится к простым арифметическим действиям, если только известны теплоты образования из элементов соединений, вступающих в реакцию и образующихся в результате ее.
К теплотам физических и физико-химических процессов, с которыми приходится иметь дело при расчетах химической аппаратуры, следует отнести: теплоту испарения, теплоту плавления, теплоту гидратации, теплоту растворения и теплоту разведения (разбавления). Значения величин теплот физических превращений берут, как правило, из справочников. Эти данные для большого числа процессов можно найти в таблицах и номограммах [4].
Теплота, подающаяся к аппарату извне
Эта величина подсчитывается в зависимости от конкретных условий, т.е. от того, что именно и в каком виде является носителем тепловой энергии.
Количество тепла, необходимое для нагревания отдельных частей аппарата, определяется по формуле:
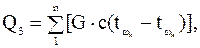
где G – масса отдельных частей аппаратов, кг;
с – теплоемкости отдельных частей аппарата, кДж/кг·К;
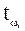 - средняя температура отдельных частей аппарата в конце нагревания, ºС;
- средняя температура отдельных частей аппарата в конце нагревания, ºС;
 - начальная температура отдельных частей аппарата, ºС.
- начальная температура отдельных частей аппарата, ºС.
Теплота уходящих из аппарата продуктов
Подсчитывается совершенно так же, как и количество теплоты Q1.
Тепловые потери в окружающую среду
Вызываются теплопроводностью стенок аппарата, переходом тепловой энергии в лучистую и конвекцией. В основе подсчетов величины Q5 лежат законы теплопередачи. В большинстве случаев основные потери тепла происходят за счет теплопроводности стенок аппарата. Эти потери рассчитываются по уравнению:
- в случае плоских стенок:
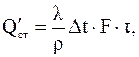
- в случае цилиндрических стенок:
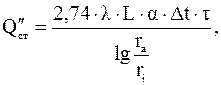
где Δt - разность температур между внутренней t1 и внешней t2 стенками аппарата Δt = t1 – t2;
F - поверхность стенки, м2;
ρ - толщина стенки, м;
L - длина стенки цилиндра, м;
ri - внутренний радиус стенки цилиндра, м;
ra - внешний радиус стенки цилиндра, м;
τ - время, ч;
λ – коэффициент теплопроводности материала стенки, ккал/ч·ºС.
Для твердых тел значение λ берут из таблиц; для жидкостей и газов коэффициент теплопроводности чаще всего рассчитывается по формулам:
- для жидкостей:
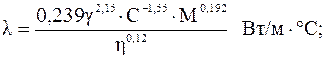
- для газов:
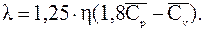
где γ - удельный вес жидкости;
С - средняя удельная теплоемкость жидкости;
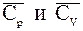 - средние удельные теплоемкости газов при постоянных давлении и объеме;
- средние удельные теплоемкости газов при постоянных давлении и объеме;
М - молекулярный вес жидкости;
η - вязкость жидкости или газа в сантипуазах.
Следует отметить, что при составлении теплового баланса производственных процессов иногда величиной Q5 задаются на основе практических данных или же определяют ее как разность между суммой:
(Q1 + Q2 + Q3) и Q4.
Date: 2015-07-24; view: 668; Нарушение авторских прав