
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Работа 19. Способы получения и физические свойства алкенов
|
|
Задание В
74. Бутен можно получить крекингом:
а) бутана, б) пентана, в) гексана, г) октана.
75. В качестве основного продукта каталитического дегидрирования н-бутана образуется:
а) бутен-1, б) бутен-2,
в) 2-метилпропен, г) 2-метилпропан.
76. Дегидрохлорированием 2-метил-3-хлорбутана можно получить:
а) 2-метилбутен-1, б) 2-метилбутен-2,
в) 3-метилбутен-1, г) бутен-2.
77. Соотнесите:
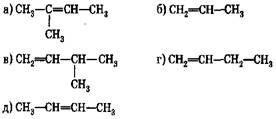
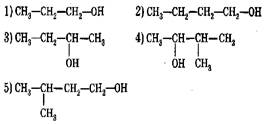 исходный спиртпродукт реакции дегидратации:
исходный спиртпродукт реакции дегидратации:
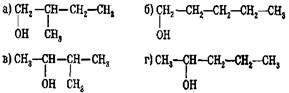
78. Пентен-2 можно получить дегидратацией спирта:
Напишите уравнение реакции, укажите условия ее проведения.
79. Соотнесите:
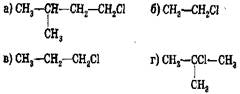 продукт реакции дегидрохлорирования: исходный хлоралкан
продукт реакции дегидрохлорирования: исходный хлоралкан
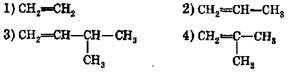
80. Какие признаки характеризуют физические свойства этена:
1) бесцветная жидкость,
2) имеет резкий запах,
3) бесцветный газ,
4) немного легче воздуха,
5) почти без запаха,
6) плохо растворим в воде,
7) не горит,
8) с воздухом образует взрывоопасные смеси?
а) 3,4,5,6,8, б) 1,2,6,7, в) 2,3,4,6,8, г) 3,4,6,8.
81. Какой объем спиртового раствора гидроксида натрия с массовой долей NаОН 8% (плотность 0,96 г/мл) потребуется для дегидрохлорирования 2-хлорпропана массой 7,85 г?
а) 52,1 мл, б) 48,0 мл, в) 46,3 мл, г) 42,1 мл.
82. Плотность паров алкена по воздуху равна 2,41. Молекулярная формула этого углеводорода:
а) С3Н6, б) С4Н8, в) С5Н10, г) С6Н12.
83. Массовая доля водорода в углеводороде нормального строения составляет 14,29%, плотность его паров по водороду равна 21. Это вещество называется:
а) этен, б) пропен, в) бутен, г) пентен.
84. При термическом крекинге декана основными продуктами являются:
а) бутан и пентан, б) пентан и пентен, в) ацетилен и водород, г) децен и водород.
85. В качестве основного продукта каталитического дегидрирования н-пентана образуется:
а) пентен-1, б) пентен-2,
в) 2-метилбутен-1, г) 2-метилбутен-2.
Напишите уравнение соответствующей реакции.
86. Реакцией дегидробромирования 2-метил-4-бромпентана можно получить:
а) 2-метилпентен-2, б) 4-метилпентен-2,
в) 4-метилпентен-1, г) 2-метилпентен-1.
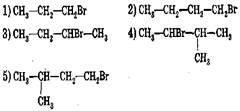
87. Соотнесите:
исходный бромалкан продукт реакции дегидробромирования::
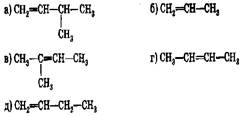
88. 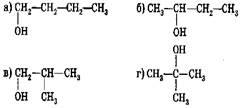 Бутен-2 можно получить дегидратацией спирта:
Бутен-2 можно получить дегидратацией спирта:
Напишите уравнение реакции, укажите
условия ее проведения.
89. Соотнесите:
продукт реакции дегидратации: исходный спирт:

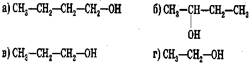
90. Какие признаки характеризуют физические свойства пропена:
1) бесцветный газ,
2) бесцветная жидкость,
3) имеет удушливый запах,
4) смешивается с водой во всех отношениях,
5) горит,
6) плохо растворим в воде,
7) в 21 раз тяжелее водорода,
8) легче воздуха?
а) 1,5,6,7, б) 2,3,4,5, в) 1,3,5,6,8, г) 1,6,7.
91. Какой объем этилена (н. у.) можно получить дегидратацией 100 мл этилового спирта (плотность 0,8 г/мл), массовая доля воды в котором составляет 4%, если выход продукта реакции 85% от теоретического?
а) 31,8 л, б) 33,1 л, в) 34,4 л, г) 44,0 л.
92. Пары алкена в 42 раза тяжелее водорода. Молекулярная формула алкена:
а) С3Н6, б) С4Н8, в) С5Н10, г) С6Н12.
93. Массовая доля углерода в углеводороде равна 85,71%, плотность его паров по воздуху 0,966. Это вещество называется:
а) этен, б) пропен, в) бутен, г) пентен.
Задание С
94. *Для получения алкенов не применяют крекинг:
а) термический, б) каталитический, в) восстановительный.
95. *В качестве основного продукта каталитического дегидрирования 2-метилбутана образуется:
а) 2-метилбутен-1, б) 2-метилбутен-2,
 в) 3-метилбутен-1, г) бутен-2.
в) 3-метилбутен-1, г) бутен-2.
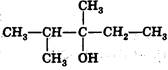
96. *Основной продукт дегидратации спирта с формулой:
Называется:
а) 2,3-диметилпентен-2, б) 3,4-диметилпентен-2,
в) 2-этил-3-метилбутен-1, г) 2,3-диметилпентен-1.
97. *Какой галогеналкан нужно взять в реакцию дегидрохлорирования, чтобы получить 2-метилбутен-2?
а) 2-метил-1-хлорбутан, б) 2-метил-3-хлорбутан,
в) 2-метил-4-хлорбутан, г) 2-метил-2,3-дихлорбутан.
98. *Из каких веществ, и в каких условиях можно получить требуемые алкены?
 целевой алкен: исходное вещество:
целевой алкен: исходное вещество:
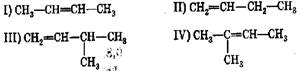
условия реакции:
а) спиртовой раствор NаОН, нагревание,
б) нагревание при 180°С в присутствии Н2SО4(конц.).
99. 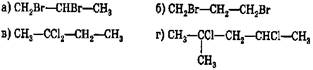 *Какой дигалогеналкан при нагревании с металлическим цинком образует алкен?
*Какой дигалогеналкан при нагревании с металлическим цинком образует алкен?
100. *Какие признаки характеризуют физические свойства пентена-1:
1) бесцветный газ,
2) бесцветная жидкость,
3) растворим в воде,
4) мало растворим в воде,
5) горит,
6) тяжелее воды?
а) 1,4,5, б) 2,3,5,6, в) 2,4,5,6, г) 2,4,5.
101. *При взаимодействии 27,4 г 2-бромбутана с избытком спиртового раствора гидроксида калия при нагревании образовалась смесь бутена-1 и бутена-2 в соотношении 1:4. Объемы этих газов при н. у. равны соответственно:
а) 0,896 и 3,584 л, б) 1,12 и 4,48 л, в) 2,24 и 8,96 л, г) 4,48 и 17,92 л.
102. *Относительная плотность алкена по газу, образующемуся при нагревании нитрита аммония, равна 1. Этот алкен имеет формулу:
а) С2Н4, б) С3Н6, в) С4Н8, г) С5Н10.
103. *При н. у. 10л паров вещества имеют массу 18,75г. Плотность этого углеводорода по воздуху равна:
а) 0,966, б) 1,448, в) 1,931, г) 2,414.
104. **При нагревании 42,8 г бромалкана с избытком спиртового раствора гидроксида калия с выходом 80% получили 5,6л (н.у.) этиленового углеводорода симметричного строения. Исходный галогеналкан называется:
а) бромэтан, б) 1-бромбутан,
в) 2-бромбутан, г) 2,3-диметил-2-бромбутан.
Задание А
105. *На основании электронного строения двойной связи предположите, какие типы реакций наиболее характерны для алкенов.
106. Перечислите основные типы реакций, характерные для этиленовых углеводородов.
107. В какие реакции присоединения вступают алкены? Расшифруйте смысл каждого термина.
108. *Опишите механизм реакции электрофильного присоединения бромоводорода к этену в водном растворе.
109. Многие реакции присоединения к алкенам являются обратными способам их получения.
110. Как называются эти обратные реакции? Сравните условия проведения реакций в том и другом направлении.
111. *Среди реакций присоединения (гидрирование, галогенирование, гидрогалогенирование, гидратация) только гидрирование и гидратацию можно считать обратимыми реакциями. Объясните почему.
112. Сформулируйте правило Марковникова. Приведите по две реакции гидрогалогенирования и гидратации, иллюстрирующие его.
113. *Для 2-метилпропена покажите распределение электронной плотности в молекуле, определяющее направление реакций присоединения. Свяжите правило Марковникова с результатами проведенного анализа.
114. Дайте определения терминов: «мономер», «полимер», «полимеризация», «элементарное звено», «степень полимеризации». Проиллюстрируйте каждый из них на уравнениях реакций полимеризации этена и пропена.
115. *Опишите механизм реакции радикальной полимеризации алкенов.
116. Запишите термохимическое уравнение реакции горения этена, зная, что ее тепловой эффект составляет 1410 кДж\моль.
117. Какие качественные реакции на непредельные соединения (в том числе алкены) вы знаете?
118. Напишите схематическое уравнение реакции окисления пропена водным раствором перманганата калия КМnО4. Обратите внимание на то, что гидроксильные группы в продукте должны располагаться у соседних атомов углерода.
119. *Напишите полные молекулярные уравнения реакций окисления этена водным раствором перманганата калия КМnО4 в нейтральной и кислотной среде (при нагревании). До каких степеней окисления восстанавливается марганец в том и другом случае?
120. 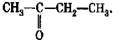 **Деструктивное окисление алкенов перманганатом калия в среде серной кислоты можно использовать для установления положения двойной связи в углеродной цепи. Напишите структурную формулу алкена, если в качестве продуктов данной реакции выделены уксусная кислота СН3—СООН и бутанон-2
**Деструктивное окисление алкенов перманганатом калия в среде серной кислоты можно использовать для установления положения двойной связи в углеродной цепи. Напишите структурную формулу алкена, если в качестве продуктов данной реакции выделены уксусная кислота СН3—СООН и бутанон-2
121. Расскажите об областях применения этиленовых углеводородов.
Date: 2015-07-10; view: 6617; Нарушение авторских прав