
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Устойчивость и коагуляция дисперсных систем
|
|
Под устойчивостью дисперсной системы понимают постоянство во времени ее состояния и основных свойств: дисперсности, равномерного распределения частиц в объеме среды и характера взаимодействия между частицами. Устойчивость дисперсных систем делят на седиментационную (кинетическую), агрегативную и фазовую (конденсационную).
Седиментационная устойчивость характеризует способность дисперсной системы сохранять равномерное распределение частиц в объеме, т.е. противостоять действию силы тяжести и процессам оседания или всплывания частиц.
Агрегативная устойчивость - это способность системы противостоять процессу укрупнения частиц.
По отношению к агрегации дисперсные системы делятся на следующие.
1. Термодинамически устойчивые, или лиофильные, которые самопроизвольно диспергируются и существуют без дополнительной стабилизации (растворы коллоидных ПАВ, растворы полимеров, суспензоиды - глина, мыла, растворы ВМВ и т.п.). При образовании этих систем свободная энергия Гиббса уменьшается: D G <0.
2. Принципиально термодинамически неустойчивые, или лиофобные системы. Их неустойчивость обусловлена избытком поверхностной энергии. Они не могут быть получены самопроизвольным диспергированием (золи, суспензии, эмульсии). На их образование всегда затрачивается энергия: D G >0.
Процесс слипания частиц дисперсной фазы в результате потери агрегативной устойчивости называется коагуляцией.
Под фазовой (конденсационной) устойчивостью понимается структура и прочность агрегатов, образующихся при коагуляции дисперсной системы. Конденсационно неустойчивые системы образуют непрочные агрегаты или рыхлые осадки, в которых частицы теряют свою подвижность, но сами сохраняются длительное время. Этому способствуют прослойки дисперсионной среды между частицами. Агрегаты с такой структурой могут снова распадаться на отдельные частицы, т.е. подвергаться пептизации. Конденсационно устойчивые системы характеризуются образованием агрегатов с прочной структурой. К этому приводит непосредственный фазовый контакт частиц друг с другом, процесс кристаллизации, срастания частиц и т.п.
Объединение частиц может привести к образованию сплошной структурированной системы, обладающей фазовой устойчивостью.
Факторы агрегативной устойчивости дисперсных систем делят на термодинамические и кинетические.
К термодинамическим факторам относятся следующие:
электростатический - способствует созданию электростатичес-ких сил отталкивания вследствие возникновения двойного электрического слоя (ДЭС) на поверхности частиц;
адсорбционно-сольватный - приводит к уменьшению межфазного натяжения, что препятствует сближению частиц;
энтропийный - проявляется в стремлении частиц к равномерному распределению по объему системы.
К кинетическим факторам устойчивости, снижающим скорость агрегации частиц, относятся следующие:
структурно-механический связан с образованием на поверхности частиц защитных пленок, обладающих упругостью и механической прочностью, стойких к разрушению;
гидродинамический - снижает скорость движения частиц вследствие изменения вязкости и плотности дисперсионной среды.
Теория устойчивости гидрофобных коллоидов разработана Деряпшым, Ландау, Фервееми Овербеком (теория ДЛФО). Устойчивость дисперсных систем определяется балансом энергии притяжения и отталкивания частиц. Энергия притяжения обусловлена межмолекулярными силами Ван-дер-Ваальса и изменяется обратно пропорционально квадрату расстояния между частицами. Энергия отталкивания, по теории ДЛФО, определяется только электростатической составляющей расклинивающего давления (давления отталкивания) и убывает с расстоянием по экспоненциальному закону. В зависимости от баланса этих сил в тонкой прослойке жидкости между сближающимися частицами возникает либо положительное расклинивающее давление, препятствующее их соединению, либо отрицательное, приводящее к утончению прослойки и контакту между частицами.
Возникновение расклинивающего давления в тонких жидких слоях обусловлено такими факторами:
1) электростатическим взаимодействием в слое, обусловленное взаимным перекрыванием двойных электрических слоев (ДЭС) – это силы отталкивания с энергией Uотт >0;
2) ван-дер-Ваальсовыми силами притяжения с энергией Uпр <0;
1) адсорбционными силами, возникающими при перекрывании молекулярных адсорбционных слоев, где повышенная концентрация создает осмотический поток в сторону пленки, приводит к росту поверхностной энергии системы и, следовательно, к отталкиванию;
2) структурным, связанным с образованием граничных слоев растворителя с особой структурой. Он характерен для лиофильных систем и соответствует термодинамическим представлениям об адсорбционно-сольватном барьере. Эффект обычно положительны.
Результирующая энергия межчастичного взаимодействия U определяется как сумма двух составляющих:
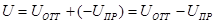
Если | U отт| > | U пр|, то преобладают силы отталкивания, коагуляция не происходит, золь является агрегативно устойчивым. В противоположном случае преобладают силы притяжения между частицами, происходит коагуляция.
Рассмотрим количественную интерпретацию этих сил.
Электростатическое отталкивание между мицеллами возникает при перекрывании диффузных слоёв противоионов. Энергия этого взаимодействия:
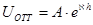 ,
,
где h – расстояние между частицами; 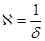 - величина, обратная толщине диффузного слоя δ; A – величина, не зависящая от h и определяемая параметрами ДЭС.
- величина, обратная толщине диффузного слоя δ; A – величина, не зависящая от h и определяемая параметрами ДЭС.
Величины א и A могут быть рассчитаны на основе теории ДЭС.
Расчёты показывают, что энергия отталкивания уменьшается:
· при увеличении зарядов противоионов и их концентрации;
· при уменьшении по абсолютной величине φо и z-потенциала.
Из уравнения следует, что U отт убывает с увеличением расстояния между частицами h по экспоненциальному закону.
Энергия притяжения связана, главным образом, с дисперсионным взаимодействием между молекулами. Она может быть рассчитана по уравнению
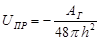 ,
,
где AГ – константа Гамакера.
 Из этого уравнения следует, что энергия притяжения изменяется с увеличением расстояния между частицами h обратно пропорционально квадрату расстояния. Таким образом, притяжение сравнительно медленно уменьшается с увеличением расстояния. Так, при увеличении h в 100 раз энергия притяжения уменьшается в 104 раз. В то же время энергия отталкивания уменьшается в 1043 раз.
Из этого уравнения следует, что энергия притяжения изменяется с увеличением расстояния между частицами h обратно пропорционально квадрату расстояния. Таким образом, притяжение сравнительно медленно уменьшается с увеличением расстояния. Так, при увеличении h в 100 раз энергия притяжения уменьшается в 104 раз. В то же время энергия отталкивания уменьшается в 1043 раз.
Результирующая энергия взаимодействия между частицами, находящимися на расстоянии h, определяется уравнением:
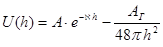
Зависимость суммарной потенциальной энергии межчастичного взаимодействия от расстояния между частицами имеет сложный характер.
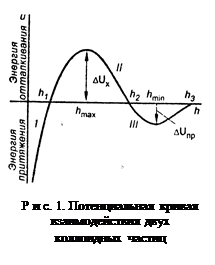
Общий вид этой зависимости U = f(h) представлен на рисунке 1.
На графике есть три участка:
1) 0 < h < h 1. U (h)<0, между частицами преобладают силы притяжения, наблюдается ближний минимум.
U отт → const; U пр → -∞. Происходит коагуляция.
2) h 1 < h < h 2. U (h)>0 – между частицами преобладают силы отталкивания. U отт > | U пр|.
3) h 2 < h < h 3. U (h)<0 – обнаруживается дальний минимум, однако глубина его невелика.
При h = h 1, h 2, h 3 U (h) = 0, т. е. при этих расстояниях между частицами силы притяжения уравновешиваются силами отталкивания.
Таким образом, если частицы сблизятся на расстояние меньше h 1, они неизбежно слипнутся, но для этого должен быть преодолён потенциальный барьер ∆Uк. Это возможно при достаточной кинетической энергии частиц, которая среднестатистически близка к произведению κТ.
Рассмотрим взаимодействие двух частиц. Будем одну частицу считать неподвижной, а вторую – приближающейся к ней с энергией, равной κТ.
Если κТ < ∆U пр, частицы останутся на расстоянии hmin и будут связаны между собой через слой дисперсионной среды, т. е. образуют “пару”, но непосредственно не слипаются и не теряют своей седиментационной устойчивости. В таких случаях говорят, что взаимодействие происходит в дальнем минимуме.
Если ∆ Umin < κТ << ∆ Uк, то частицы при столкновении отлетают друг от друга. Система агрегативно устойчива.
Если κТ < ∆Uк, то происходит медленная коагуляция.
Если κТ > ∆Uк, то происходит быстрая коагуляция.
Так как золь обычно рассматривают при постоянной температуре, кинетическая энергия частиц остаётся постоянной. Следовательно, для коагуляции должен быть уменьшен потенциальный барьер коагуляции ∆Uк.
Обычно для понижения потенциального барьера в систему вводится электролит-коагулянт. Теория ДЛФО даёт возможность вычислить порог быстрой коагуляции СКБ:
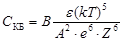 ,
,
где А, В – постоянные величины, которые могут быть рассчитаны;
ε – диэлектрическая проницаемость среды;
Z – заряд иона-коагулянта;
ē – заряд электрона.
Лиофобные дисперсные системы (золи, эмульсии, суспензии) агрегативно неустойчивы, поскольку у них имеется избыток поверхностной энергии. Процесс укрупнения частиц протекает самопроизвольно, так как он ведет к уменьшению удельном поверхности и снижению поверхностной энергии Гиббса.
Увеличение размера частиц может идти как за счет коагуляции, т.е. слипания частиц, так иза счет изотермической перегонки (перенос вещества от мелких частиц к крупным). Коагуляция лиофобных дисперсных систем может происходить под влиянием ряда факторов: механических воздействий, света, изменения температуры, изменения концентрации дисперсной фазы, при добавлении электролитов.
Различают два типа электролитной коагуляции коллоидных систем: нейтрализации иную и концентрационную.
Нейтрализщионная коагуляция наблюдается у золей со слабо заряженными частицами. Ионы добавляемого электролита адсорбируются на заряженной поверхности, снижая поверхностный потенциал частиц. В результате уменьшения заряда электрические силы отталкивания между частицами ослабевают, частицы при сближении слипаются и выпадают в осадок.
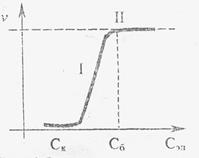 Р и с. 2. Зависимость скорости коа-
гуляции от концентрации электро-лита
Р и с. 2. Зависимость скорости коа-
гуляции от концентрации электро-лита
| Концентрационная коагуляция наблюдается в сильнозаряженных дисперсных системах. Она протее-кает вследствие сжатия диффузной части ДЭС при увеличенииконцентрации ионов электролита в растворе. Частицы могут подойти друг к другу на расстояние, где действуют силы притяжения. Коагуляция наступает при добав-лении определенного количества электролита. |
Наименьшая концентрация электролита С к, при которой начинается медленная коагуляция, называется порогом коагуляции.
При дальнейшем увеличении концентрации электролита выше порога коагуляции скорость коагуляции сначала нарастает (участок I на рисунке 2) - это область медленной коагуляции.
Область, в которой скорость коагуляции перестает зависеть от концентрации электролита, называется областью быстрой коагуляции (участок II на рисунке 2).
При электролитной коагуляции по концентрационному типу порог коагуляции Ск в соответствии с правилом Дерягина - Ландау обратно пропорционален заряду противоионов Z в шестой степени:
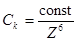 (1)
(1)
Из него следует, что значения порогов коагуляции для одно-, двух-и трехзарядных ионов относятся как
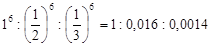 (2)
(2)
Величина, обратная порогу коагуляции, называется коагулирую-щей способностью. Значение коагулирующей способности для одно-, двух- и трехзарядных противоионов относятся между собой как 1:64:729.
Порог коагуляции, кмоль/м3, рассчитывают по формуле
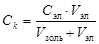 . (3)
. (3)
где С эл - концентрация электролита, кмоль/м3;
V эл, - минимальный объем электролита, вызывающий коагуляцию, м3;
V золь - объем золя, м3.
Date: 2015-07-02; view: 1819; Нарушение авторских прав