
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Аполипротеиды плазмы человека
|
|
| Аполипротеид | Молекулярная масса, Д | Функция | Место синтеза |
| A-I | Связывает липиды, кофактор ЛХАТ*; входит в состав ЛВП (основной белок) | Печень, кишечник | |
| A-II | Входит в состав ЛВП (второй белок), Активирует ЛХАТ (кофактор) | Печень | |
| A-IV | 43000- | Кофактор ЛХАТ | Печень, кишечник |
| B-100 | Транспорт триглицеридов в печени, маркер ЛОНП | Печень | |
| В-48 | Транспорт триглицеридов в кишечнике, маркер хиломикронов | Кишечник | |
| С-I | Активирование ЛХАТ | Печень, Кишечник | |
| С-II | Активирование ЛПЛ (липо- | Печень, | |
| протеиновая липаза) | кишечник | ||
| С-III | Ингибитор ЛПЛ (?), гликопротеин | Печень, кишечник | |
| Д | Транспорт эфиров холестерина | Печень | |
| Е | Распознавание липопротеидов связывание хилокронов в печени | Печень |
Липиды плазмы транспортируются в виде специальных агрегатов – липопротеидов. В таких агрегатах различают сердцевину и оболочку. Сердцевина в свою очередь состоит из триглицеридов, эфиров холестерина В и эфиров жирных кислот, оболочка – из фосфолипидов, свободного холестерина и аполипопротеидов, обеспечивающих распознавание соответствующих рецепторов на поверхности клеток и активацию указанных выше ферментов.
Образование хиломикронов в кишечнике происходит при обязательном участии аполипопротеида В-48 (апо-В-48), который синтезируется в эпителиальных клетках кишечника. В состав хиломикронов, помимо апо-В-48, входит небольшое количество аполипопротеинов группы А. После попадания лимфы в грудной проток хиломикроны взаимодействуют с ЛВП, носителями аполипопротеидов группы С и Е; при участии липопротеидной липазы (ЛПЛ) триглицериды, содержащиеся в хиломикронах, гидролизуются на глицерин и свободные жирные кислоты (СЖК). ЛПЛ присутствуют на эндотелиальных поверхностях клеток мышцы сердца, жировой ткани и мышц скелета. СЖК способны проникать в клетки, где используются как источник энергии или участвуют в процессах липогенеза.
ЛОНП синтезируются в печени. Их сердцевина состоит из триглицеридов и эфиров холестерина. Белки, входящие в состав оболочки, представлены апо-В-100, апо-Е и апо-С. ЛОНП служат источником образования ЛСП и ЛНП.
ЛНП являются переносчиками эфиров холестерина, необходимого для синтеза стероидных гормонов, образования желчных кислот. Этот класс липопротеидов ответствен за транспорт 70% холестерина плазмы. В состав оболочки ЛНП входит апо-В-100, способный распознать соответствующий рецептор к ЛНП, синтез которого контролируется геном, расположенным на 19-й хромосоме. После взаимодействия ЛНП с рецептором образующийся комплекс проникает внутрь клетки, где в области лизосом под влиянием лизосомальных ферментов происходит гидролиз сердцевины и высвобождение свободного холестерина.
ЛВП образуются в печени и содержат фосфолипиды, свободный холестерин, апо-Е, апо-С и небольшое количество апо-А-1. ЛВП связывают свободный холестерин на периферии и транспортируют его к печени. ЛВП содержат ЛХАТ (лецитин/холестерин ацилтрансфераза), которая активирует перенос ацетиловой группы фосфолипидов на свободный холестерин, осуществляя эстерификацию холестерина. Эфиры холестерина депонируются во многих тканях организма (кора надпочечников и др.) и по мере необходимости используются для биосинтеза соответствующих веществ.
Выше указывалось, что в результате обмена углеводов образуются ацетил-КоА, АТФ, NADPH (2), глицерол-3-фосфат, используемые для синтеза жира, и количество липидов, накапливающихся в жировых депо, в большей степени зависит от содержания в пищевом рационе углеводов, а не жиров.
Липогенез – процесс синтеза жирных кислот, интенсивно протекающий в печени и жировой ткани. Следует отметить, что биосинтез липидов осуществляется в основном в цитоплазме клетки и лишь незначительная их часть, как считают некоторые авторы, образуется в митохондриях.
Образовавшийся в митохондриях ацетил-КоА способен проникать через их мембрану в цитоплазму только после взаимодействия с оксалоацетатом и образования цитрата, который достигает цитоплазмы, где вновь превращается в ацетил-КоА и оксалоацетат. Таким образом, оксалоацетат выполняет функцию катализатора, способствуя переносу ацетильной группы из интрамитохондриального пространства в цитозоль, где при участии ацетил-КоА-карбоксилазы происходит карбоксилирование ацетил-КоА с образованием малонил-КоА. Последний, взаимодействуя с комплексом жирные кислоты – белок при участии АТФ и КоА, превращается в комплекс жирнокислотный ацетил-КоА, что является необходимой стадией образования триглицеридов.
Карбоксилирование ацетил-КоА является важным регулятором синтеза жирных кислот и на всех последующих этапах липогенеза участвуют либо малонил-КоА, либо ацетил-КоА. Так под влиянием синтетазы жирных кислот и при использовании одной молекулы ацетил-КоА и 7 молекул малонил-КоА образуется пальмитил-КоА, способный к разнообразным превращениям. При потере одной молекулы СО2 и КоА образуется пальмитиновая кислота, молекула которой содержит 16 атомов углерода. Путем удлинения цепи в митохондриях или в плазматическом ретикулуме до 18 атомов углерода пальмитиновая кислота может быть превращена в стеариновую, а после десатурации она же преобразуется в пальмитоолеиновую и олеиновую кислоты.
При эстерификации жирных кислот с глицерином образуются триглицериды, причем в реакции участвует не свободный глицерин, а его производное – глицерол-3-фосфат, образующийся в печени из глицерина при участии глицеролкиназы. Эстерификация жирных кислот в жировой ткани может происходить лишь при достаточном поступлении дигидроксиацетонфосфата, который образуется в процессе гликолиза и конвертируется в глицерол-3-фосфат при участии глицерофосфатдегидрогеназы.
В печени и жировой ткани инсулин увеличивает синтез жирных кислот и триглицеридов. При эндогенном биосинтезе триглицеридов, кроме глюкозы, могут использоваться соединения, образующиеся из гликогенных аминокислот. Липогенез в печени контролируется тиротропным гормоном и гормонами щитовидной железы. Так, после гипофизэктомии синтез липидов печенью уменьшается и восстанавливается после введения тироксина.
Липолиз – процесс гидролиза липидов с образованием неэстерифицированных жирных кислот и глицерина – катализируется внутриклеточной гормональнозависимой липазой (триацилглицериновая липаза), которая воздействует на триглицериды и стимулируется цАМФ. Липаза лимитирует скорость липолиза, а образование цАМФ под влиянием аденилатциклазы находится в свою очередь под контролем различных гормонов.
Мембрана адипоцитов содержит рецепторы, взаимодействующие с гормонами, обладающими липолитическими свойствами (катехоламины, АКТГ, СТГ), и рецепторы к инсулину. В результате действия липолитических гормонов повышается активность аденилатциклазы, увеличивается образование цАМФ, активизируются ЛПЛ и липолиз жира. Взаимодействие инсулина с соответствующими рецепторами, наоборот, приводит к угнетению аденилатциклазы, снижению концентрации цАМФ и торможению липолиза. Липолиз увеличивается во время голодания, при продолжительной работе, охлаждении, стрессе. Липолитическое действие катехоламинов (адреналина, норадреналина) и глюкагона осуществляется путем активации аденилатциклазы. С физиологической точки зрения, роль норадреналина в процессе липолиза представляется более важной, чем адреналина. Он образуется в адренергических нервных окончаниях в жировой ткани и обеспечивает мобилизацию жирных кислот.
Гормон роста оказывает мощное липолитическое действие, которое отличается от действия катехоламинов. Он вызывает увеличение концентрации свободных жирных кислот в плазме через 2-3 часа. Это действие, отмечающееся при введении даже небольших доз СТГ, по-видимому, связано с торможением процесса реэстерификации свободных жирных кислот. Тем не менее СТГ оказывает определенное модулирующее влияние и на активность аденилатциклазы.
Другие гипофизарные гормоны (АКТГ, ТТГ, меланоцитостимулирующий гормон) также оказывают липолитическое действие, хотя и менее выраженное, чем у СТГ. Большинство авторов считают, что оно осуществляется путем активации аденилатциклазы и повышения скорости образования цАМФ.
Тироидные гормоны и кортикостероиды оказывают пермиссивное (разрешающее) действие на липолиз, поскольку липолитический и калоригенный эффекты катехоламинов не проявляются в отсутствие кортикостероидов и тироидных гормонов. Имеются данные о том, что ТТГ, АКТГ, гормоны щитовидной железы и коры надпочечников индуцируют синтез аденилатциклазы и, следовательно, принимают непосредственное участие в стимуляции липолиза. Кроме того, тироидные гормоны влияют на активность ацил-КоА-синтетазы, локализующейся в митохондриях, и цитоплазматического фермента глицеролфосфатдегидрогеназы. Эти ферменты участвуют в регуляции скорости липолиза и липогенеза.
Как уже отмечалось, инсулин обладает характерным антилиполитическим свойством, и при сахарном диабете вследствие увеличения липолиза повышается концентрация свободных жирных кислот в плазме, снижению которой способствует инсулинотерапия.
Белковый обмен. Белки в организме также являются источником энергии. Они содержатся главным образом в мышцах и их количество составляет в организме здорового человека массой 70 кг около 6000 г, что соответствует 24 000 ккал. Циркуляция их в крови в виде аминокислот незначительна и составляет всего 6 г, или 24 ккал. Белки – необходимый компонент любой ткани организма – поступают в организм с пищей и в желудочно-кишечном тракте после воздействия на них ферментов (пепсина, трипсина) гидролизуются до небольших пептидов и аминокислот, которые затем всасываются в кровь и лимфу. В организме человека для синтеза пуринов, пиримидинов, порфиринов используются только аминокислоты, поэтому все поступающие с пищей белки должны быть диссоциированы в различных ферментативных реакциях до отдельных аминокислот.
Некоторые аминокислоты могут синтезироваться в организме, поэтому называются заменимыми: аланин, аспарагиновая кислота, цистеин, глутаминовая кислота, глицин, пролин, серин, тирозин, аспарагин, глутамин; другие же не могут быть синтезированы и называются незаменимыми: лейцин, изолейцин, валин, лизин, метионин, фенилаланин, триптофан, треонин, гистидин, аргинин (гистидин и аргинин синтезируются в организме взрослого человека).
Синтез белка – сложный процесс, происходящий постоянно. Информация о структуре любого белка данного организма хранится в хромосомах в виде генетического кода. При поступлении сигнала о необходимости синтеза определенного белка с участка ДНК, на котором закодирована структура данного белка, при участии фермента РНК-полимеразы начинает образовываться мРНК. Процесс образования мРНК называется “транскрипция”. Если молекула ДНК относительно стабильна, то период полураспада мРНК составляет 2-80 ч (время, необходимое для синтеза белка).
Образовавшаяся мРНК покидает ядро и направляется к рибосомам, где и осуществляется синтез белка. На рибосомах локализуются рибосомальная РНК (рРНК) и транспортная РНК (тРНК), которые вместе участвуют в процессе считывания информации, заложенной в мРНК, и“сборки” нового белка. Обычно рРНК и метионил-тРНК присоединяются к специальной точке мРНК, и с этого момента начинается их движение вдоль молекулы мРНК, во время которого “считываются” триплетные кодоны и начинается “сборка” полипептидной цепи нового белка.
Аминокислоты могут использоваться рибосомами лишь после их активации соответствующими ферментами, число которых по всей вероятности соответствует количеству аминокислот.
Гормоны влияют на скорость синтеза белка несколькими путями: повышением или снижением активности ферментов, участвующих в процессе “сборки” белковой молекулы, изменением транспорта аминокислот, необходимых для синтеза белка, повышением активности и скорости образования рибосом, осуществляющих синтез белка, повышением скорости начала образования полисом, повышением активности РНК-полимеразы и скорости образования мРНК. Некоторые вещества могут в той или иной степени ингибировать перечисленные процессы. Так, актиномицин, связываясь с ДНК, угнетает синтез мРНК и таким образом препятствует действию гормонов на процессы транскрипции. Пуромицин угнетает синтез белка, влияя на тРНК, и ингибирует гормональную регуляцию процессов трансляции.
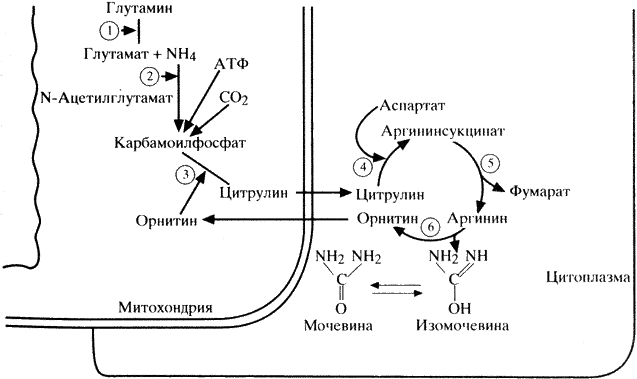
Наряду с процессами синтеза белка в организме постоянно протекают процессы белкового катаболизма, конечным продуктом которого у человека является мочевина. Аммиак, образующийся в большинстве клеток в процессе катаболизма аминокислот, наряду с другими азотсодержащими веществами превращается в печени в мочевину в цикле Кребса-Гензелейта (схема 10). При этом аммиак транспортируется в печень не в свободной форме, а детоксицируется глутаматом с образованием глутамина под влиянием фермента глутаминсинтетазы. В митохондриях печени глутамин при участии глутаминазы вновь диссоциирует на аммиак и глутамат. Последний возвращается в ткани, а аммиак используется для образования карбамоилфосфата с помощью фермента карбамоилфосфатсинтетазы.
Date: 2015-07-01; view: 671; Нарушение авторских прав