
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Законы раздражения. Параметры возбудимости
|
|
Реакция клеток, тканей на раздражитель определяется законами раздражения:
1) Закон “все или ничего”: При допороговых раздражениях клетки ответной реакции не возникает, при пороговой силе раздражителя развивается максимальная ответная реакция, поэтому увеличение силы раздражения выше пороговой не сопровождается её усилением. В соответствии с этим законом реагирует на раздражения одиночное нервное и мышечное волокно, сердечная мышца.
2) Закон силы: Чем больше сила раздражителя, тем сильнее ответная реакция. Однако выраженность ответной реакции растет лишь до определенного максимума. Закону силы подчиняется целостная скелетная, гладкая мышца, так как они состоят из многочисленных мышечных клеток, имеющих различную возбудимость.
3) Закон силы-длительности. Чем сильнее раздражитель, тем меньшее время требуется для возникновения ответной реакции. Зависимость между пороговой силой и необходимой длительностью раздражения отражается кривой силы-длительности. По этой кривой можно определить ряд параметров возбудимости:
а) Порог раздражения – это минимальная сила раздражителя, при которой возникает возбуждение.
б) Реобаза – это минимальная сила раздражителя, вызывающая возбуждение при его действии в течение неограниченно долгого времени. На практике порог и реобаза имеют одинаковый смысл. Чем ниже порог раздражения или меньше реобаза, тем выше возбудимость ткани.
в) Полезное время – это минимальное время действия раздражителя силой в одну реобазу за которое возникает возбуждение.
Противосвертывающая система крови. Первичные и вторичные антикоагулянты, фибринолиз.
1. Первичные антикоагулянты, постоянно содержащиеся в крови. Эти вещества выделяются в кровоток с постоянной скоростью, где они взаимодействуют с активными факторами свертывания, вызывая их нейтрализацию. В силу этого кровь продолжает оставаться в жидком состоянии. К первичным антикоагулянтам относятся антитромбин III, гепарин, протеин С, протеин S, тромбомодулин и др.
2. Вторичные антикоагулянты образуются в процессе гемокоагуляции и фибринолиза и являются результатом дальнейшей ферментативной деградации некоторых коагуляционных факторов; в силу чего они после изначальной активации теряют способность к участию в процессе свертывания крови и приобретают свойства антикоагулянтов. К вторичным антикоагулянтам фибрин, антитромбин IX, антитромбопластины, фибринопептиды.
Регуляция уровня кальция в крови. Роль паратиреотропина, кальцитонина и витамина Д3.
Кальций участвует в физиологических процессах только в ионизированном виде. Этот катион необходим для обеспечения возбудимости нервно- мышечной системы, проницаемости мембран, свертывания крови. Ионизация кальция в крови зависит от рН. При ацидозе содержание ионизированного кальция повышается, а при алкалозе — падает. Алкалоз и снижение уровня кальция ведут к резкому повышению нейромышечной возбудимости и тетании. Влияет на уровень кальция и концентрация белков в плазме крови. Содержание кальция в крови поддерживается в норме в диапазоне 2-4 ммоль/л. Внутриклеточный ионизированный кальций является важнейшим вторичным посредником нервно-гуморальных регуляторных влияний, обеспечивает процессы освобождения медиаторов и секрецию гормонов, энергетику клетки. Основное депо кальция — костная ткань, в которой содержится 90% катиона в связанном виде.
В щитовидной железе образуется тирокальцитонин, снижающий содержание кальция в крови. Под влиянием тирокальцитонина угнетается функция остеокластов, разрушающих костную ткань, и активируется функция остеобластов, способствующих образованию костной ткани и поглощению ионов Са2+ из крови. Тирокальцитонин – гормон, сберегающий кальций в организме.
Если кальция поступает мало или он теряется слишком активно, может развиться его недостаточность. Это обычно проявляется нарушением строения скелета, сосудов, кровоточивостью и многими другими симптомами. Нарушения в скелете именуются терминами остеопения и остеомаляция. Остеопенией называют снижение показателей костной массы, а остеомаляцией – остеопенические состояния, связанные с нарушением минерализации костей. У старших детей и взрослых может развиться остеопороз – системное заболевание скелета, которое характеризуется уменьшением массы кости и микроскопической его структуры, специфической перестройкой костей, которая приводит к хрупкости и повышенной ломкости костей, а значит высок риск переломов.
Детей раннего возраста дефицит кальция приводит к отставаниям в росте и веса, развитию рахита в первые полгода жизни, нарушает строение костей. Кроме того, тормозится психическое развитие малыша и созревание функций внутренних органов. Врачами указывается и связь недостатка кальция и фосфора в развитии кариеса, нарушениями осанки, деформациями грудной клетки и ног – Х или О-образные ноги и нарушением тонуса мышц.
Многие заболевания внутренних органов приводят к нарушению обмена кальция – это заболевания щитовидной железы, сахарный диабет, патологии почек, нарушения работы кишечника и пищеварительных желез – печени и поджелудочной железы.
В кишечнике повышение реабсорбции кальция происходит благодаря стимулирующему действию паратгормона на синтез кальцитриола – активного метаболита витамина D3. Витамин D3 образуется в неактивном состоянии в коже под воздействием ультрафиолетового излучения. Под влиянием паратгормона происходит его активация в печени и почках. Кальцитриол повышает образование кальцийсвязывающего белка в стенке кишечника, что способствует обратному всасыванию кальция. Влияя на обмен кальция, паратгормон одновременно воздействует и на обмен фосфора в организме: он угнетает обратное всасывание фосфатов и усиливает их выведение с мочой (фосфатурия).
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 7
Состав и свойства желудочного сока, роль ферментов, соляной кислоты и слизи. Нервная и гуморальная регуляция сокоотделения.
У взрослого человека в течение суток образуется и выделяется около 2-2,5 л желудочного сока. Желудочный сок имеет кислую реакцию (рН 1,5- 1,8). В его состав входят вода – 99% и сухой остаток – 1%. Сухой остаток представлен органическими и неорганическими веществами. Главный неорганический компонент желудочного сока – соляная кислота, которая находится в свободном и связанном с протеинами состоянии.
Соляная кислота выполняет ряд функций: 1) способствует денатурации и набуханию белков в желудке, что облегчает их последующее расщепление пепсинами;
2) активирует пепсиногены и превращает их в пепсины;
3) создает кислую среду, необходимую для действия ферментов желудочного сока;
4) обеспечивает антибактериальное действие желудочного сока;
5) способствует нормальной эвакуации пищи из желудка: открытию пилорического сфинктера со стороны желудка и закрытию со стороны 12-перстной кишки;
6)возбуждает панкреатическую секрецию. Кроме того, в желудочном соке содержатся следующие неорганические вещества: хлориды, бикарбонаты, сульфаты, фосфаты, натрий, калий, кальций, магний и др. В состав органических веществ входят протеолитические ферменты, главную роль среди которых играют пепсины. Пепсины выделяются в неактивной форме в виде пепсиногенов. Под влиянием соляной кислоты они активируются. Оптимум протеазной активности находится при рН 1,5-2,0. Они расщепляют белки до альбумоз и пептонов. Гастриксин гидролизует белки при рН 3,2-3,5. Реннин (химозин) вызывает створаживание молока в присутствии ионов кальция, так как переводит растворимый белок казеиноген в нерастворимую форму – казеин. В желудочном соке имеются также и непротеолитические ферменты. Желудочная липаза мало активна и расщепляет только эмульгированные жиры. В желудке продолжается гидролиз углеводов под влиянием ферментов слюны. Это становится возможным потому, что пищевой комок, попавший в желудок, пропитывается кислым желудочным соком постепенно, И в это время во внутренних слоях пищевого комка в щелочной среде продолжается действие ферментов слюны. В состав органических веществ входит лизоцим, обеспечивающий бактерицидные свойства желудочного сока. Желудочная слизь, содержащая муцин, защищает слизистую оболочку желудка от механических и химических раздражении и от самопереваривания. В желудке вырабатывается гастромукопротеид, или внутренний фактор Касла. Только при наличии внутреннего фактора возможно образование комплекса с витамином В12, участвующего в эритропоэзе. В желудочном соке содержатся также аминокислоты, мочевина, мочевая кислота
Проводящая система сердца. Градиент автоматии, ионный механизм потенциала действия клеток синоатриального узла.
проводящая система сердц:
1. синоатриальный узел (Кейса-Флека). Он расположен в устье полых вен, т.е. в венозных синусах;
2. межузловые и межпредсердные проводящие пути Бахмана, Венкенбаха и Торелла. Проходят по миокарду предсердий и межпредсердной перегородке;
3. атриовентрикулярный узел (Ашоффа-Тавара). Находится в нижней части межпредсердной перегородки под эндокардом правого предсердия;
4. атриовентрикулярный пучок или пучок Гиса. Идет от атриовентрикулярного узла по верхней части межжелудочковой перегородки. Затем делится на две ножки – правую и левую. Они образуют ветви в миокарде желудочков;
5. волокна Пуркине. Это концевые разветвления ветвей ножек пучка Гиса. Образуют контакты с клетками сократительного миокарда желудочков.
Синоатриальный узел образован преимущественно Р-клеткми. Остальные отделы проводящей системы – переходными кардиомиоцитами. Однако небольшое количество клеток-пейсмекеров имеется и в них, а также сократительном миокарде предсердий и желудочков. Сократительные кардиомиоциты соединены с волокнами Пуркинье, а также между собой нексусами, т.е. межклеточными контактами с низким электрическим сопротивлением. Благодаря этому и примерно одинаковой возбудимости кардиомиоцитов, миокард является функциональным синцитием, т.е. сердечная мышца реагирует на раздражение как единое целое. Для нормальной работы кардиоцитов очень важно сохранение постоянства концентраций ионов во внутри- и внеклеточной жидкости, т.к. сердце очень чутко реагирует на изменения электролитного баланса крови и тканевой жидкости в самом миокарде.Значительный избыток ионов калия во внеклеточной жидкости приводит к падению возбудимости, проводимости, угнетению активности синоатриального узла, развитию синусовой брадикардии, а затем к полному прекращению электрической и сократительной активности миокарда, к остановке сердца в диастоле. В естественных условиях значительное повышение концентрации ионов калия в плазме крови практически невозможно, однако оно может наблюдаться, например, при передозировке вводимых внутривенно препаратов калия. В кардиохирургии гиперкалиевые растворы (так называемые кардиоплегические) используются специально для временной остановки сердца.Гипокалиемия приводит к синусовой тахикардии и другим нарушениям сердечного ритма, вплоть до фибрилляции желудочков. Увеличение внеклеточной концентрации ионов кальция влияет, прежде всего, на сократительную функцию рабочих кардиоцитов. Увеличение входа кальция в цитоплазму вызывает усиление сократимости миокарда. Подобные эффекты вызывают адреналин и норадреналин, под влиянием которых открываются дополнительные кальциевые каналы и увеличивается кальциевый ток в клетку. В клетках синоатриального узла ускоряется деполяризация и возрастает частота возбуждения.Удаление кальция из внеклеточной среды приводит к снижению его внутриклеточной концентрации, к ослаблению сократительной активности.
Роль рецепторов слизистой оболочки полости рта и пародонта в регуляции акта жевания.
жевательный аппарат, который включает в себя зубные ряды, жевательные мышцы, височно-нижнечелюстной сустав
Пищу принимают в виде кусков, смесей различного состава и консистенции или жидкостей. В зависимости от этого она или сразу проглатывается, или подвергается механической и химической обработке в полости рта.
Процесс механической обработки пищи зубами посредством движения нижней челюсти относительно верхней называется жеванием. Жевательные движения осуществляются сокращениями жевательных и мимических мышц, мышц языка.
При жевании резцы могут развивать давление на пищу 11—25 кГс/см, коренные зубы — 29—90 кГс/см. Акт жевания осуществляется рефлекторно, имеет цепной характер, автоматизированные и волевые компоненты.
В ротовой полости пища в процессе жевания измельчается, смачивается слюной, перемешивается с ней, растворяется (без чего невозможна оценка вкусовых качеств пищи и ее гидролиз). В результате формируется относительно гомогенный ослизненный пищевой комок для глотания.
Регуляция жевания осуществляется рефлекторно. Возбуждение от рецепторов слизистой оболочки рта (механо-, хемо- и терморецепторов) передается по афферентным волокнам II, III ветви тройничного, языкоглоточного, верхнего гортанного нерва и барабанной струны в центр жевания, который находится в продолговатом мозге. Возбуждение от центра к жевательным мышцам передается по эфферентным волокнам тройничного, лицевого и подъязычного нервов. Возбуждение от чувствительных ядер ствола мозга по афферентному пути через специфические ядра таламуса переключается на корковый отдел вкусовой сенсорной системы, где осуществляется анализ и синтез информации, поступающей от рецепторов слизистой оболочки ротовой полости. На уровне коры больших полушарий происходит переключение сенсорных импульсов на эфферентные нейроны, которые по нисходящим путям посылают регулирующие влияния к центру жевания продолговатого мозга.
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 8
Условия возникновения артериального давления в сосудистой системе. Причины непрерывности тока крови по сосудам. Изменение сопротивления и давления по ходу сосудистого русла (начертить графики).
По функциональному значению в сосудистой системе можно выделить следующие отделы:
1.Компрессионный отдел – аорта и крупные артерии, сосуды эластического типа с упруго-растяжимыми стенками. Указанные сосуды растягиваются поступающей из сердца кровью во время систолы, а во время диастолы спадаются, тем самым поддерживая давление крови и подталкивая её в артериолы и капилляры.
2.Резистивный отдел – артериолы, сосуды с хорошо выраженной мышечной стенкой. Артериолы ввиду малого их диаметра создают основное сопротивление току крови и не дают ей быстро оттекать в дистальные отделы. Это позволяет поддержать артериальное давление на достаточном уровне даже во время диастолы.
3.Обменный отдел – капилляры, где происходит обмен газами, жидкостью и другими веществами между кровью и тканями.
4.Шунтирующие сосуды – артерио-венозные анастомозы, при необходимости обеспечивающие сброс крови из артериальной системы в венозную, минуя капилляры.
5.Ёмкостные сосуды – вены, обладающие большой растяжимостью и содержащие до 80% крови. Обеспечивают венозный возврат крови к сердцу.
Условия создания давления в сосудистой системе.
Рассмотрев функциональное значение различных отделов сосудистого русла, можно сделать вывод об условиях, необходимых для создания и поддержания давления крови и непрерывного кровотока в сосудистой системе. Несмотря на то, что кровь из сердца поступает только во время систолы, давление в системе сохраняется также во время диастолы, и кровь не прерывает своего движения. Этому служит: 1. нагнетательная работа сердца; 2. эластические свойства крупных сосудов – аорты и артерий, и 3. наличие периферического сопротивления.
Н.р-75./35 1г-90/40 3г-95/60 5л-100/65 10л 105/70 15л-115/75
Условия образования отрицательного давления в плевральной полости, изменение его величины во время вдоха и выдоха (модель Дондерса).
Несмотря на то, что легкие не сращены с грудной стенкой, они повторяют ее движения. Это объясняется тем, что между ними имеется замкнутая плевральная щель. Изнутри стенка грудной полости покрыта париетальным листком плевры, а легкие ее висцеральным листком. В межплевральной щели находится небольшое количество серозной жидкости. При вдохе объем грудной полости возрастает, а так как плевральная полость изолирована от атмосферы, то давление в ней понижается. Легкие расширяются, давление в альвеолах становится ниже атмосферного и воздух через трахею и бронхи поступает в альвеолы. Во время выдоха объем грудной клетки уменьшается, давление в плевральной щели возрастает, легкие сжимаются и воздух выходит из альвеол.
Механизмы изменения объема легких при дыхании можно продемонстрировать с помощью модели Дондерса на которой с помощью двух манометров можно проследить за изменением давления и в легких, и в плевральной полости.
Если отсосать воздух из колокола, то легкие расправятся, т.к. в плевральной полости давление станет ниже внутрилегочного, появится разница давлений между внутрилегочным пространством и плевральной полостью – транспульмональное давление.
Теперь можно попробовать снизить давление в легких, оттягивая эластическую мембрану вниз и имитируя сокращение диафрагмы и увеличение объема грудной клетки. При этом уменьшится и внутриплевральное давление, что будет видно по изменению уровня жидкости в манометре. Такие изменения внутрилегочного и плеврального давлений характерны для фазы вдоха.
Методы исследования функции слюнных желез у человека (сиалометрия, рентгенконтрастная и радиоизотопная сиалография, ультразвуковая эхолокация, термовизиография, томография).
Сиалометрия применяется для оценки функциональной способности больших или малых слюнных желез.
Существуют различные методики раздельного получения слюны из протоков околоушных и поднижнечелюстных слюнных желез. Для сбора слюны применяют капсулы Лешли – Ющенко – Красногорского, специальные металлические канюли, ватные шарики. Можно также пользоваться полиэтиленовыми катетерами, которые позволяют осуществить полную обтурацию протока и в силу своей гибкости исключают его перфорацию. Полиэтиленовый катетер удерживается в протоке на протяжении всего исследования и не требует дополнительной фиксации
Сиалосонография(ультразвуковое исследование слюнных желез)
Сиалосонография является методом изучения структурных изменений больших слюнных желез. Основными достоинствами метода являются высокая информативность, неинвазивность и биологическая безвредность. Сиалосонография является одним из самых чувствительных методов диагностики опухолей слюнных желез независимо от их размера и локализации.
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 9
Возбуждение. Потенциал действия, его фазы, ионный механизм возникновения. График ПД.
Потенциал действия (ПД) – быстрое изменение мембранного потенциала в ответ на действия раздражителя пороговой силы. ПД имеет стандартные амплитуду и временные параметры, не зависящие от силы стимула – правило “ВСЕ ИЛИ НИЧЕГО”.
Начальная деполяризация мембраны под действием раздражителя:

Если сила раздражителя достаточна, чтобы деполяризовать мембрану до КУД, открываются быстрые потенциал-зависимые натриевые каналы. Клетка возбуждена – возник нервный импульс.
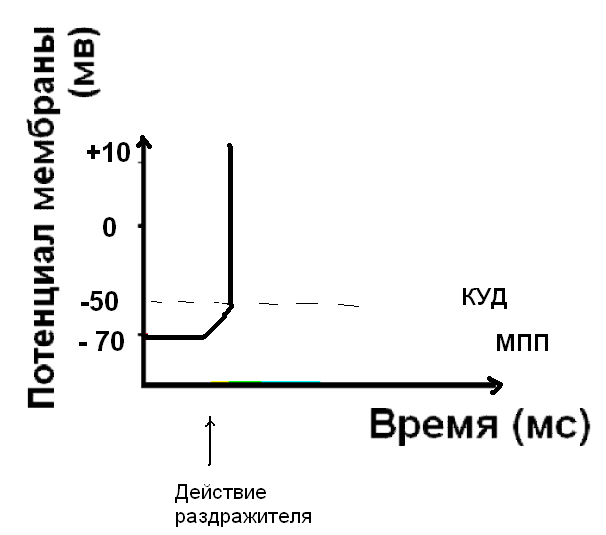
Восстановление мембранного потенциала покоя – реполяризация мембраны.
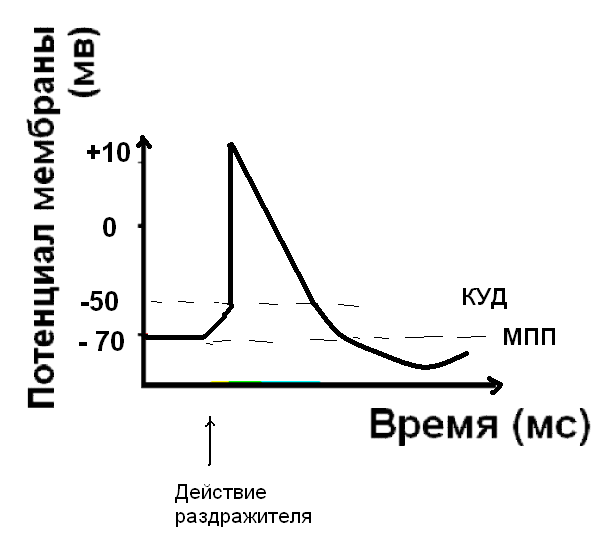
Следующий этап – восстановление мембранного потенциала покоя – реполяризация, обусловлена активным ионным транспортом. Наиболее важен процесс активного транспорта – это работа Na/K – насоса, который выкачивает ионы натрия из клетки, одновременно закачивая ионы калия внутрь клетки. Восстановление мембранного потенциала происходит благодаря току ионов калия из клетки – калиевые каналы активируются и пропускают ионы калия до достижения равновесного калиевого потенциала. Это процесс важен потому, что до тех пор, пока не восстановлен МПП, клетка не способна воспринимать новый импульс возбуждения.
ГИПЕРПОЛЯРИЗАЦИЯ – кратковременное увеличение МП после его восстановления, которое обусловлено повышением проницаемости мембраны для ионов калия и хлора. Гиперполяризация бывает только после ПД.
Деполяризация мембраны до КУД – могут открыться любые натриевые каналы, иногда кальциевые, и быстрые, и медленные, и потенциал-зависимые, и рецептор-управляемые. Это зависит от вида раздражителя и типа клеток
Быстрое поступление натрия в клетку – открываются быстрые, потенциал-зависимые натриевые каналы, и деполяризация достигает точки реверса потенциала – происходит перезарядка мембраны, знак заряда меняется на положительный.
Восстановление градиента концентрации по калию – работа насоса. Калиевые каналы активированы, калий переходит из клетки во внеклеточную среду – реполяризация, начинается восстановление МПП
Следовая деполяризация, или отрицательный следовой потенциал – мембрана еще деполяризована относительно МПП.
Следовая гиперполяризация. Калиевые каналы остаются открытыми и дополнительный ток калия гиперполяризует мембрану. После этого клетка возвращается к исходному уровню МПП. Длительность ПД составляет для разных клеток от 1 до 3-4 мс.

Обратите внимание на три величины потенциала, важные и постоянные для каждой клетки ее электрические характеристики.
МПП – электроотрицательность мембраны клетки в покое, обеспечивающая способность к возбуждению – возбудимость.
КУД – критический уровень, величина мембранного потенциала, при достижении которой открываются быстрые, потенциал зависимые натриевые каналы и происходит перезарядка мембраны за счет поступления в клетку положительных ионов натрия. Чем выше электроотрицательность мембраны, тем труднее деполяризовать ее до КУД, тем менее возбудима такая клетка.
Точка реверса потенциала (овершут) – такая величина положительного мембранного потенциала, при которой положительно заряженные ионы уже не проникают в клетку – кратковременный равновесный натриевый потенциал.
При действии раздражителя подпороговой силы возникает неполная деполяризация – ЛОКАЛЬНЫЙ ОТВЕТ (ЛО). Неполная, или частичная деполяризация – это такое изменение заряда мембраны, которое не достигает критического уровня деполяризации (КУД).
Аденогипофиз, его структурные и функциональные связи с гипоталамусом. Физиологическая роль гормонов. Гипо- и гиперфункция аденогипофиза.
Передняя и средняя доли гипофиза объединяются под названием аденогипофиза или адреногипофиза.
В передней доле гипофиза вырабатывается ряд тропных гормонов (гормонов, оказывающих стимулирующее влияние):
- соматотропный гормон, регулирующий процессы роста и развития молодого организма;
- тиреотропный гормон, активирующий работу щитовидной железы (продуцирование тиреоидных гормонов);
- адренокортикотропный гормон, стимулирующий секрецию стероидных гормонов надпочечниками;
- гонадотропные гормоны (фолликулостимулирующий гормон, лютеинизирующий гормон и пролактин), влияющие на половое созревание и стимулирующие развитие фолликулов в яичнике и овуляцию у женщин, а также сперматогенез у мужчин.
Поскольку передняя доля гипофиза вырабатывает гормоны, стимулирующие развитие и функцию других желез внутренней секреции, гипофиз считают центром эндокринного аппарата.
В промежуточной части передней доли образуется меланоцитстимулирующий гормон, контролирующий образование пигментов -меланинов.
Связь гипоталамуса с аденогипофизом осуществляется гуморальным путем через портальную систему.
Отделение гипофиза от гипоталамуса и пересадка его в участки тела, отдаленные от гипоталамуса, вызывает прекращение продукции фолликулостимулирующего и, возможно, лютеинизирующего гормонов, существенное уменьшение выработки адренокортикотропного и тиреотропного гормонов. Выработка пролактина при нарушении сосудистой связи гипофиза с гипоталамусом повышается. Это говорит в пользу представления, что гипоталамус оказывает тормозящее влияние на выработку пролактина. Подсадка гипофизэктомированным животным гипофиза в область основания мозга приводит после регенерации портальной системы к восстановлению гормональной функции гипофиза.
Гиперфункция
болезнь Иценко—Кушинга — результат усиленного синтеза АКТГ, вследствие чего развивается гиперфункция пучковой зоны коры надпочечников.(иммунодефицит,Вторичный сахарный диабет, снижение минерализации костной ткани, Ожирение — отложение жира на лице и туловище, конечности при этом остаются худыми). Юношеский базофилизм — гиперпродукция АКТГ, СТГ и гонадотропных гормонов, у подростков в период полового созревания и проявляется ожирением, а также ускорением физического и полового развития.
Гипофункция
Гипофизарная кахексия - проявляющейся снижением образования практически всех гормонов, что приводит к нарушению всех видов обмена веществ и прогрессирующему истощению.
Гипофизарная карликовость – недостаточность соматотропина. Отставание в росте и массе тела, недоразвитием половых желез и вторичных половых признаков в сочетании с первичным бесплодием.
Функциональная связь процессов дыхания, жевания и глотания.
Включением ротового дыхания (продувание воздуха над пищей) во время жевания в основном добиваются охлаждения горячей пищи в полости рта.
В момент глотания пища продвигается в пространстве между языком и мягким небом до соприкосновения его с дужками. На этом заканчивается произвольная часть глотания и наступает вторая, рефлекторная и непроизвольная его часть. Для этой фазы характерным является приподнимание мягкого неба, языка, глотки, подъязычной кости и гортани.Мягкое небо поднимается за счет сокращения m. levator veli palatini, в напряженном и растянутом за счет m. tensor veli palatini состоянии, и примыкает к валику Пассавана, который образуется за счет сокращения верхнего глоточного констриктора (сжимателя). Таким образом предотвращается попадание пищи в носовую полость.Задняя часть языка, который в этот момент бывает укорочен своими продольными мышцами, поднимается тоже кверху в результате сокращения mm. palatoglossi и styloglossi. В результате, хотя носовая часть глотки будет мягким небом целиком отделена от остальных частей, зев тоже будет закрыт после прохождения пищевого комка в глотку. Шило-язычные мышцы оттягивают язык не только вверх, но и назад, надвигая его на надгортанник, который и закрывает вход в гортань.Первым открывается вход в пищевод, куда и проталкивается пищевой комок последовательным сокращением сжимателей глотки: вначале верхнего, потом среднего и, наконец, нижнего
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 10
Рефлекторная регуляция тонуса сосудов. Афферентные нервы (И.Ф.Цион, Э.Геринг), сосудодвигательный центр, сосудодвигательные нервы (К. Бернар).
Нейрогенный компонент сосудистого тонуса определяется исключительно тонической активностью симпатических адренергических вазоконстрикторных нервных волокон (симпатические и парасимпатические холинергические вазодилататорные волокна тонической активностью не обладают). Базальный тонус неодинаков в сосудах разных органов и имеет разное функциональное значение. Он высок в артериолах и значительно ниже в венозных сосудах.
Гуморальная регуляция осуществляется физиологически активными веществами, находящимися в крови или тканевой жидкости. Их можно разделить на следующие группы:
1. Метаболические факторы. Они включают несколько групп веществ.
а) неорганические ионы. Ионы калия вызывают расширение сосудов, ионы кальция суживают их;
б) неспецифические продукты метаболизма. Молочная кислота и другие кислоты цикла Кребса расширяют сосуды. Таким же образом действует повышение содержания СO2 и протонов, т.е. сдвиг реакции среды в кислую сторону;
в) осмотическое давление тканевой жидкости. При его повышении происходит расширение сосудов.
2. Гормоны. По механизму действия на сосуды делятся на 2 группы:
а) Гормоны, непосредственно действующие на сосуды.
Адреналин и норадреналин суживают большинство сосудов, взаимодействуя с альфа-адренорецепторами гладких мышц. В то же время, адреналин вызвает расширение сосудов мозга, почек, скелетных мышц, воздействуя на бета-адренорецепторы. Вазопрессин преимущественно суживает вены, а ангиотензин II – артерии и артериолы. Ангиотензин II образуется из белка плазмы ангиотензиногена в результате действия фермента ренина. Ренин начинает синтезироваться в юкстагломерулярном аппарате почек при снижении почечного кровотока. Поэтому при некоторых заболеваниях почек развивается почечная гипертензия. Брадикинин, гистамин, простагландины Е расширяют сосуды, а серотонин суживает их.
б) Гормоны опосредованного действия.
АКТГ и кортикостероиды надпочечников постепенно увеличивают тонус сосудов и повышают кровяное давление. Таким же образом действует тироксин.
Особенности действия норадреналина и адреналина на сосуды различных органов.
Регуляция сосудов – это регуляция сосудистого тонуса, который определяет величину их просвета. Просвет сосудов определяется функциональным состоянием их гладкой мускулатуры, а просвет капилляров зависит от состояния клеток эндотелия и гладкой мускулатуры прекапиллярного сфинктера.
Гуморальная регуляция сосудистого тонуса. Эта регуляция осуществляется за счет тех химических веществ, которые циркулируют в кровеносном русле и изменяют ширину просвета сосудов. Все гуморальные факторы, которые оказывают влияние на тонус сосудов, делят на сосудосуживающе (вазоконстрикторы) и сосудорасширяющие (вазодилятаторы).
К сосудосуживающим веществам относятся:
• адреналин – гормон мозгового вещества надпочечников, суживает артериолы кожи, органов пищеварения и легких, в низких концентрациях расширяет сосуды мозга, сердца и скелетных мышц, обеспечивая тем самым адекватное перераспределение крови, необходимое для подготовки организма к реагированию в трудной ситуации;
• норадреналин – гормон мозгового вещества надпочечников по своему действию близок к адреналину, но его действие более выражено и более продолжительно;
• вазопрессин – гормон, образующийся в нейронах супраоптического ядра гипоталамуса, форму в клетках задней доли гипофиза, действует в основном на артериолы;
• серотонин – вырабатывается клетками стенки кишки, в некоторых участках головного мозга, а также выделяется при распаде кровяных пластинок;.
К сосудорасширяющим веществам относятся:
• гистамин – образуется в стенке желудка, кишечника, других органах, расширяет артериолы;
• ацетилхолин – медиатор парасимпатических нервов и симпатических холинергических вазодилятаторов, расширяет артерии и вены;
• брадикинин – выделен из экстрактов органов (поджелудочной железы, подчелюстной слюнной железы, легких), образуется при расщеплении одного из глобулинов плазмы крови, расширяет сосуды скелетных мышц, сердца, спинного и головного мозга, слюнных и потовых желез;
• простагландины – образуются во многих органах и тканях, оказывают местное сосудорасширяющее действие;
Нервная регуляция сосудистого тонуса. Нервная регуляция сосудистого тонуса осуществляется вегетативной нервной системой. Сосудосуживающий эффект преимущественно оказывают волокна симпатического отдела вегетативной (автономной) нервной системы, а сосудорасширяющее – парасимпатические и, частично, симпатические нервы. Сосудосуживающее действие симпатических нервов не распространяется на сосуды головного мозга, сердца, легких и работающих мышц. Сосуды этих органов при возбуждении симпатической нервной системы расширяются. Следует также отметить, что не все парасимпатические нервы являются вазодилятаторами, например, волокна парасимпатического блуждающего нерва суживают сосуды сердца.
Сосудосуживающие и сосудорасширяющие нервы находятся под влиянием сосудодвигательного центра. Вазомоторный или сосудодвигательный центр – это совокупность структур, расположенных на различных уровнях ЦНС и обеспечивающих регуляцию кровообращения. Структуры, входящие в состав сосудодвигательного центра, расположены, в основном, в спинном и продолговатом мозге, гипоталамусе, коре больших полушарий. Сосудодвигательный центр состоит из прессорного и депрессорного отделов.
Депрессорный отдел снижает активность симпатических сосудосуживающих влияний и, тем самым, вызывает расширение сосудов, падение периферического сопротивления и снижение артериального давления.
Прессорный отдел вызывает сужение сосудов, повышение периферического сопротивления и давления крови.
Информацию о величине артериального давления нейронам центра блуждающего нерва несут афферентные (чувствительные) ветви блуждающего нерва — депрессорный нерв и два синокаротидных нерва
Рецепторы, расположенные в дуге аорты, являются окончаниями чувствительного нерва, открытого русским физиологом И. Ф. Ционом и названного депрессорным нервом. Раздражение окончаний этого нерва ведет к падению артериального давления, так как афферентные влияния, идущие по этому нерву, поступают к нейронам центра блуждающего нерва, а оттуда идут к сосудам и сердцу.
Антигены системы резус. Методы определения резус-принадлежности. Механизмы резус-иммунизации.
В 1940 году К.Ландштейнер и И.Винер обнаружили в эритроцитах еще один агглютиноген. Впервые он был найден в крови макак-резусов. Поэтому был назван ими резус-фактором. В отличие от антигенной системы АВ0, где к агглютиногенам А и В имеются соответствующие агглютинины, агглютиниов к резус-антигену в крови нет. Они вырабатываются в том случае, если резус-положительную кровь (содержащую резус-фактор) перелить реципиенту с резус-отрицательной кровью. При первом переливании резус-несовместимой крови никакой трансфузионной реакции не будет. Однако в результате сенсибилизации организма реципиента, через 3-4 недели в его крови появятся резус-агглютинины. Они очень длительное время сохраняются. Поэтому при повторном переливании резус-положительной крови этому реципиенту произойдет агглютинация и гемолиз эритроцитов донорской крови.
Резус-фактор крови имеет большое значение в акушерской практике, т.к. эритроциты плода могут попадать в кровяное русло матери. Если плод имеет резус-положительную кровь, а мать резус-отрицательную, то попавшие в ее организм с эритроцитами плода резус-антигены, вызовут образование резус-агглютининов. Титр резус-агглютининов нарастает медленно, поэтому при первой беременности особых осложнений не возникает. Если при повторной беременности плод опять наследует резус-положительную кровь, то поступающие через плаценту резус-агглютинины матери вызовут агглютинацию и гемолиз эритроцитов плода. В легких случаях возникает анемия, гемолитическая желтуха новорожденных. В тяжелых – эритробластоз плода и мертворожденность. Это явление называется резус-конфликтом. С целью его профилактики сразу после первых подобных родов вводят антирезус-глобулин. Он разрушает резус-положительные эритроциты, попавшие в кровь матери.
Существует 6 разновидностей резус-агглютиногенов: С, D, Е, с, d, e. Наиболее выраженные антигенные свойства у резус-агглютиногена D. Именно им определяется резус-принадлежность крови. Другие антигены этой системы практического значения не имеют.В настоящее время известно около 400 антигенных систем крови. Кроме систем АВ0 и Rh, известны систем MNSs, P, Келла, Кидда и другие. Учитывая все антигены, число их комбинаций составляет около 300 млн. Но так как их антигенные свойства выражены слабо, для переливания крови их роль чаще всего незначительна.
Переливание несовместимой крови вызывает тяжелейшее осложнение – гемотрансфузионный шок. Он возникает вследствие того, что склеившиеся эритроциты закупоривают мелкие сосуды. Кровоток нарушается. Затем происходит их гемолиз, и из эритроцитов донора в кровь поступают чужеродные белки. В результате резко падает кровяное давление, угнетается дыхание, сердечная деятельность, нарушается работа почек, центральной нервной системы. Переливание даже небольших количеств такой крови может закончиться смертью реципиента.
В настоящее время допускается переливание только одногрупповой крови по системе АВ0. Обязательно учитывается и ее резус-принадлежность.
Состав и свойства слюны. Регуляция слюнообразования. Роль симпатических и парасимпатических нервов. Дуга слюноотделительного рефлекса.
Свойства слюны. Смешанная слюна (полученная сплевыванием слюна называется ротовой жидкостью) представляет собой вязкую, слегка опалесцирующую мутноватую жидкость. рН смешанной слюны 5,8— 7,4; рН слюны околоушных желез ниже (5,81), чем подчелюстных (6,39). С увеличением скорости секреции рН слюны повышается до 7,8.
Вязкость слюны, обусловленная муцином, важна для склеивания пищевых частиц в пищевой комок, который будучи ослизненным легче проглатывается. Этому способствует также пенообразование. На употребляемые пищевые вещества выделяется много муцина, на отвергаемые — мало. Слизь слюны выполняет и защитную функцию, обвалакивая нежную слизистую оболочку рта и пищевода.
Состав слюны. Секрет слюнных желез содержит около 99% воды и 1 % сухого остатка, в который входят анионы хлоридов, фосфатов, сульфатов, бикарбонатов, иодитов, бромидов, фторидов. В слюне содержатся катионы натрия, калия, кальция, магния, а также микроэлементы (железо, медь, никель и др.). Органические вещества представлены в основном белками. В слюне имеются самые различные по происхождению белки в том числе и белковое слизистое вещество муцин. В слюне содержатся азотсодержащие компоненты: мочевина, аммиак, креатинин и др.
Функции слюны.
1. Пищеварительная функция
2. Защитная функция слюны выражается в следующем:
3. Трофическая функция
4. Выделительная функция
Date: 2016-07-25; view: 727; Нарушение авторских прав