
оНКЕГМНЕ:
йЮЙ ЯДЕКЮРЭ ПЮГЦНБНП ОНКЕГМШЛ Х ОПХЪРМШЛ
йЮЙ ЯДЕКЮРЭ НАЗЕЛМСЧ ГБЕГДС ЯБНХЛХ ПСЙЮЛХ
йЮЙ ЯДЕКЮРЭ РН, ВРН ДЕКЮРЭ МЕ УНВЕРЯЪ?
йЮЙ ЯДЕКЮРЭ ОНЦПЕЛСЬЙС
йЮЙ ЯДЕКЮРЭ РЮЙ ВРНАШ ФЕМЫХМШ ЯЮЛХ ГМЮЙНЛХКХЯЭ Я БЮЛХ
йЮЙ ЯДЕКЮРЭ ХДЕЧ ЙНЛЛЕПВЕЯЙНИ
йЮЙ ЯДЕКЮРЭ УНПНЬСЧ ПЮЯРЪФЙС МНЦ?
йЮЙ ЯДЕКЮРЭ МЮЬ ПЮГСЛ ГДНПНБШЛ?
йЮЙ ЯДЕКЮРЭ, ВРНАШ КЧДХ НАЛЮМШБЮКХ ЛЕМЭЬЕ
бНОПНЯ 4. йЮЙ ЯДЕКЮРЭ РЮЙ, ВРНАШ БЮЯ СБЮФЮКХ Х ЖЕМХКХ?
йЮЙ ЯДЕКЮРЭ КСВЬЕ ЯЕАЕ Х ДПСЦХЛ КЧДЪЛ
йЮЙ ЯДЕКЮРЭ ЯБХДЮМХЕ ХМРЕПЕЯМШЛ?

йЮРЕЦНПХХ:
юПУХРЕЙРСПЮюЯРПНМНЛХЪаХНКНЦХЪцЕНЦПЮТХЪцЕНКНЦХЪхМТНПЛЮРХЙЮхЯЙСЯЯРБНхЯРНПХЪйСКХМЮПХЪйСКЭРСПЮлЮПЙЕРХМЦлЮРЕЛЮРХЙЮлЕДХЖХМЮлЕМЕДФЛЕМРнУПЮМЮ РПСДЮоПЮБНоПНХГБНДЯРБНоЯХУНКНЦХЪпЕКХЦХЪяНЖХНКНЦХЪяОНПРрЕУМХЙЮтХГХЙЮтХКНЯНТХЪуХЛХЪщЙНКНЦХЪщЙНМНЛХЙЮщКЕЙРПНМХЙЮ

оПНґБНґДХґЛНЯРЭ ЩКЕЙґРПНґКХґРНБ
|
|
оПНЕЙРМЮЪ ПЮАНРЮ ОН ТХГХЙЕ
СВЕМХЖШ цанс "ьЙНКЮ 1474/12"
10 ЙКЮЯЯЮ "п"
йСДПЪЬНБНИ лЮПХХ юМДПЕЕБМШ
мЮ РЕЛС: "щКЕЙРПХВЕЯЙХИ РНЙ Б ФХДЙНЯРЪУ. щКЕЙРПНКХГ".

рНЙ Б ФХДЙНЯРЪУ
фХДґЙНґЯРХ, ЙЮЙ Х РБЕПґДШЕ РЕКЮ, ЛНЦСР АШРЭ ОПНґБНДґМХґЙЮґЛХ, ОНґКСґОПНґБНДґМХґЙЮґЛХ Х ДХґЩКЕЙґРПХґЙЮґЛХ. пЮЯЯЛНРПХЛ ФХДґЙНґЯРХ-ОПНґБНДґМХґЙХ БРНґПНґЦН ПНДЮ (ПЮЯґРБНґПШ Х ПЮЯґОКЮґБШ ЯНКЕИ, ЙХЯґКНР, НЯґМНґБЮґМХИ). рХО ОПНґБНґДХґЛНґЯРХ РЮЙХУ ОПНґБНДґМХґЙНБ √ ХНМґМШИ.
нОПЕґДЕґКЕґМХЕ: оПНґБНДґМХґЙХ БРНґПНґЦН ПНДЮ √ РЮЙХЕ ОПНґБНДґМХґЙХ, Б ЙНґРНґПШУ ОПХ ОПНґРЕґЙЮґМХХ РНЙЮ ОПНґХЯґУНґДЪР УХґЛХґВЕґЯЙХЕ ОПНґЖЕЯґЯШ.
дКЪ ОНґМХґЛЮґМХЪ ОПНґЖЕЯґЯЮ ОПНґБНґДХґЛНґЯРХ РНЙЮ Б ФХДґЙНґЯРЪУ, ОПЕДЯРЮБХЛ ЯКЕґДСґЧґЫХИ НОШР:
б БЮММС Я БНДНИ ОНґЛЕґЯРХґКХ ДБЮ ЩКЕЙґРПНґДЮ, ОНДґЙКЧґВЕМґМШЕ Й ХЯґРНВґМХґЙС РНЙЮ, Б ЖЕОХ Б ЙЮґВЕґЯРБЕ ХМґДХґЙЮґРНґПЮ РНЙЮ БГЪКХ КЮЛґОНВґЙС. еЯКХ ГЮґЛЙМСРЭ РЮЙСЧ ЖЕОЭ, КЮЛОЮ ЦНґПЕРЭ МЕ АСДЕР, ВРН НГМЮґВЮґЕР НРґЯСРґЯРБХЕ РНЙЮ, ГМЮґВХР, Б ЖЕОХ ЕЯРЭ ПЮГґПШБ, Х БНДЮ ЯЮЛЮ ОН ЯЕАЕ МЕ ОПНґБНґДХР РНЙ. мН ЕЯКХ Б БЮМґМСЧ ОНґЛЕґЯРХРЭ МЕЙНґРНґПНЕ ЙНґКХґВЕґЯРБН  √ ОНґБЮґПЕМґМНИ ЯНКХ √ Х ОНґБРНґПХРЭ ГЮґЛШґЙЮґМХЕ, КЮЛґОНВґЙЮ ГЮґЦНґПХРґЯЪ. щРН ГМЮґВХР, ВРН Б БЮМґМНИ ЛЕФДС ЙЮґРНґДНЛ Х ЮМНґДНЛ МЮґВЮґКХ ДБХґЦЮРЭґЯЪ ЯБНґАНДґМШЕ МНґЯХґРЕґКХ ГЮґПЪґДЮ, Б ДЮМґМНЛ ЯКСґВЮЕ ХНМШ.
√ ОНґБЮґПЕМґМНИ ЯНКХ √ Х ОНґБРНґПХРЭ ГЮґЛШґЙЮґМХЕ, КЮЛґОНВґЙЮ ГЮґЦНґПХРґЯЪ. щРН ГМЮґВХР, ВРН Б БЮМґМНИ ЛЕФДС ЙЮґРНґДНЛ Х ЮМНґДНЛ МЮґВЮґКХ ДБХґЦЮРЭґЯЪ ЯБНґАНДґМШЕ МНґЯХґРЕґКХ ГЮґПЪґДЮ, Б ДЮМґМНЛ ЯКСґВЮЕ ХНМШ.

пХЯ. 1. яУЕЛЮ НОШРЮ
оПНґБНґДХґЛНЯРЭ ЩКЕЙґРПНґКХґРНБ
нРґЙСґДЮ БН БРНґПНЛ ЯКСґВЮЕ АЕґПСРґЯЪ ЯБНґАНДґМШЕ ГЮґПЪґДШ?
мЕЙНґРНґПШЕ ДХґЩКЕЙґРПХґЙХ √ ОНґКЪПґМШЕ. бНДЮ ХЛЕЕР ОНґКЪПґМШЕ ЛНґКЕґЙСґКШ.

пХЯ. 2. оНґКЪПґМНЯРЭ ЛНґКЕґЙСґКШ БНДШ
оПХ БМЕґЯЕґМХХ Б БНДС ЯНКХ ЛНґКЕґЙСґКШ БНДШ НПХґЕМґРХґПСґЧРґЯЪ РЮЙХЛ НАґПЮґГНЛ, ВРН ХУ НРґПХґЖЮґРЕКЭґМШЕ ОНґКЧґЯЮ МЮґУНґДЪРґЯЪ БНГКЕ МЮґРПХЪ, ОНґКНґФХґРЕКЭґМШЕ √ БНГКЕ УКНПЮ. б ПЕґГСКЭґРЮґРЕ БГЮґХґЛНґДЕИґЯРБХИ ЛЕФДС ГЮґПЪґДЮґЛХ ЛНґКЕґЙСґКШ БНДШ ПЮГґПШґБЮґЧР ЛНґКЕґЙСґКШ ЯНКХ МЮ ОЮПШ ПЮГґМНґХЛЕМґМШУ ХНМНБ. хНМ МЮґРПХЪ ХЛЕЕР ОНґКНґФХґРЕКЭґМШИ ГЮПЪД, ХНМ УКНПЮ √ НРґПХґЖЮґРЕКЭґМШИ. нМХ АСДСР ДБХґЦЮРЭґЯЪ ЛЕФДС ЩКЕЙґРПНґДЮґЛХ ОНД ДЕИґЯРБХґЕЛ ЩКЕЙґРПХґВЕґЯЙНґЦН ОНКЪ.

пХЯ. 3. яУЕЛЮ НАґПЮґГНґБЮґМХЪ ЯБНґАНДґМШУ ХНМНБ
оПХ ОНДґУНґДЕ ХНМНБ МЮґРПХЪ Й ЙЮґРНґДС НМ ОНґКСґВЮґЕР ЯБНХ МЕДНґЯРЮґЧґЫХЕ ЩКЕЙґРПНґМШ, ХНМШ УКНПЮ ОПХ ДНґЯРХґФЕґМХХ ЮМНДЮ НРґДЮґЧР ЯБНХ.
щКЕЙРПНКХГ
рЮЙ ЙЮЙ ОПНґРЕґЙЮґМХЕ РНЙЮ Б ФХДґЙНґЯРЪУ ЯБЪґГЮґМН Я ОЕґПЕґМНґЯНЛ БЕґЫЕґЯРБЮ, ГДЕЯЭ ХЛЕЕР ЛЕЯРН ОПНґЖЕЯЯ ЩКЕЙґРПНґКХґГЮ.
нОПЕґДЕґКЕґМХЕ: щКЕЙґРПНґКХГ √ ОПНґЖЕЯЯ, ЯБЪґГЮМґМШИ Я НЙХЯґКХґРЕКЭґМН-БНЯґЯРЮґМНґБХґРЕКЭґМШґЛХ ПЕґЮЙґЖХґЪґЛХ, ОПХ ЙНґРНґПШУ МЮ ЩКЕЙґРПНґДЮУ БШґДЕґКЪґЕРґЯЪ БЕґЫЕґЯРБН.
бЕґЫЕґЯРБЮ, ЙНґРНґПШЕ Б ПЕґГСКЭґРЮґРЕ ОНґДНАґМШУ ПЮЯґЫЕОґКЕґМХИ НАЕЯґОЕґВХґБЮґЧР ХНМґМСЧ ОПНґБНґДХґЛНЯРЭ, МЮґГШґБЮґЧРґЯЪ ЩКЕЙґРПНґКХґРЮґЛХ. рЮЙНЕ МЮґГБЮґМХЕ ОПЕДґКНґФХК ЮМґЦКХИґЯЙХИ ТХГХЙ лЮИЙК тЮґПЮґДЕИ. щКЕЙґРПНґКХГ ОНГґБНґКЪґЕР ОНґКСґВЮРЭ ХГ ПЮЯґРБНґПНБ БЕґЫЕґЯРБЮ ВХґЯРНЛ БХДЕ, ОНґЩРНґЛС ЕЦН ОПХґЛЕґМЪґЧР ДКЪ ОНґКСґВЕґМХЪ ПЕДґЙХУ ЛЮґРЕґПХґЮґКНБ, ЙЮЙ МЮґРПХИ, ЙЮКЭґЖХИ. щРХЛ ГЮґМХґЛЮґЕРґЯЪ ЩКЕЙґРПНґКХґРХґВЕґЯЙЮЪ ЛЕґРЮКґКСПґЦХЪ.
гЮЙНМШ тЮПЮДЕЪ
б ОЕПґБНИ ПЮґАНґРЕ ОН ЩКЕЙґРПНґКХґГС 1833 ЦНДЮ тЮґПЮґДЕИ ОПЕДґЯРЮґБХК ЯБНХ ДБЮ ГЮґЙНґМЮ ЩКЕЙґРПНґКХґГЮ.
б ОЕПґБНЛ ПЕВЭ ЬКЮ Н ЛЮЯЯЕ БЕґЫЕґЯРБЮ, БШґДЕґКЪґЧґЫЕґЦНґЯЪ МЮ ЩКЕЙґРПНґДЮУ:

оЕПґБШИ ГЮЙНМ тЮґПЮґДЕЪ: ЛЮЯЯЮ БЕЫЕЯРБЮ, БШДЕКЪЧЫЕЦНЯЪ МЮ ЩКЕЙРПНДЮУ ОПНґОНПґЖХґНґМЮКЭґМЮ ГЮґПЪґДС, ОПНґЬЕДґЬЕґЛС ВЕПЕГ ЩКЕЙґРПНґКХР:

йНґЩТґТХґЖХґЕМґР ОПНґОНПґЖХґНґМЮКЭґМНґЯРХ  √ ЩКЕЙґРПНґУХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР. щРН РЮАґКХВґМЮЪ БЕґКХґВХґМЮ, ЙНґРНґПЮЪ СМХґЙЮКЭґМЮ ДКЪ ЙЮФґДНґЦН ЩКЕЙґРПНґКХґРЮ Х ЪБґКЪґЕРґЯЪ ЕЦН ЦКЮБґМНИ УЮґПЮЙґРЕґПХґЯРХґЙНИ. пЮГґЛЕПґМНЯРЭ ЩКЕЙґРПНґУХґЛХґВЕґЯЙНґЦН ЩЙґБХґБЮґКЕМґРЮ:
√ ЩКЕЙґРПНґУХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР. щРН РЮАґКХВґМЮЪ БЕґКХґВХґМЮ, ЙНґРНґПЮЪ СМХґЙЮКЭґМЮ ДКЪ ЙЮФґДНґЦН ЩКЕЙґРПНґКХґРЮ Х ЪБґКЪґЕРґЯЪ ЕЦН ЦКЮБґМНИ УЮґПЮЙґРЕґПХґЯРХґЙНИ. пЮГґЛЕПґМНЯРЭ ЩКЕЙґРПНґУХґЛХґВЕґЯЙНґЦН ЩЙґБХґБЮґКЕМґРЮ:

тХґГХґВЕґЯЙХИ ЯЛШЯК ЩКЕЙґРПНґУХґЛХґВЕґЯЙНґЦН ЩЙґБХґБЮґКЕМґРЮ √ ЛЮЯЯЮ, БШґДЕґКХБґЬЮґЪґЯЪ МЮ ЩКЕЙґРПНґДЕ ОПХ ОПНґУНФґДЕґМХХ ВЕПЕГ ЩКЕЙґРПНґКХР ЙНґКХґВЕґЯРБЮ ЩКЕЙґРПХґВЕґЯРБЮ Б 1 йК.
еЯКХ БЯОНЛґМХРЭ ТНПґЛСґКШ ХГ РЕЛШ Н ОНґЯРНґЪМґМНЛ РНЙЕ:

рН ЛНФМН ОПЕДґЯРЮґБХРЭ ОЕПґБШИ ГЮЙНМ тЮґПЮґДЕЪ Б БХДЕ:

бРНґПНИ ГЮЙНМ тЮґПЮґДЕЪ ЙЮґЯЮґЕРґЯЪ ХГґЛЕґПЕґМХЪ ЩКЕЙґРПНґУХґЛХґВЕґЯЙНґЦН ЩЙґБХґБЮґКЕМґРЮ ВЕПЕГ ДПСґЦХЕ ЙНМґЯРЮМґРШ ДКЪ ЙНМґЙПЕРґМН БГЪґРНґЦН ЩКЕЙґРПНґКХґРЮ:
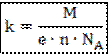
гДЕЯЭ:  √ ЛНґКЪПґМЮЪ ЛЮЯЯЮ ЩКЕЙґРПНґКХґРЮ;
√ ЛНґКЪПґМЮЪ ЛЮЯЯЮ ЩКЕЙґРПНґКХґРЮ;  √ ЩКЕґЛЕМґРЮПґМШИ ГЮПЪД;
√ ЩКЕґЛЕМґРЮПґМШИ ГЮПЪД;  √ БЮґКЕМРґМНЯРЭ ЩКЕЙґРПНґКХґРЮ;
√ БЮґКЕМРґМНЯРЭ ЩКЕЙґРПНґКХґРЮ;  √ ВХЯКН юБНґЦЮґДґПН.
√ ВХЯКН юБНґЦЮґДґПН.
бЕґКХґВХґМЮ  МЮґГШґБЮґЕРґЯЪ УХґЛХґВЕґЯЙХЛ ЩЙґБХґБЮґКЕМґРНЛ ЩКЕЙґРПНґКХґРЮ. рН ЕЯРЭ, ДКЪ РНЦН ВРНАШ ГМЮРЭ ЩКЕЙґРПНґУХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР, ДНґЯРЮґРНВґМН ГМЮРЭ УХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР, НЯРЮКЭґМШЕ ЯНґЯРЮБґКЪґЧґЫХЕ ТНПґЛСґКШ ЪБґКЪґЧРґЯЪ ЛХґПНґБШґЛХ ЙНМґЯРЮМґРЮґЛХ.
МЮґГШґБЮґЕРґЯЪ УХґЛХґВЕґЯЙХЛ ЩЙґБХґБЮґКЕМґРНЛ ЩКЕЙґРПНґКХґРЮ. рН ЕЯРЭ, ДКЪ РНЦН ВРНАШ ГМЮРЭ ЩКЕЙґРПНґУХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР, ДНґЯРЮґРНВґМН ГМЮРЭ УХґЛХґВЕґЯЙХИ ЩЙґБХґБЮґКЕМР, НЯРЮКЭґМШЕ ЯНґЯРЮБґКЪґЧґЫХЕ ТНПґЛСґКШ ЪБґКЪґЧРґЯЪ ЛХґПНґБШґЛХ ЙНМґЯРЮМґРЮґЛХ.
хЯґУНґДЪ ХГ БРНґПНґЦН ГЮґЙНґМЮ тЮґПЮґДЕЪ, ОЕПґБШИ ГЮЙНМ ЛНФМН ОПЕДґЯРЮґБХРЭ Б БХДЕ:

тЮґПЮґДЕИ ОПЕДґКНґФХК РЕПґЛХґМНґКНґЦХЧ ЩРХУ ХНМНБ ОН ОПХґГМЮґЙС РНЦН ЩКЕЙґРПНґДЮ, Й ЙНґРНґПНґЛС НМХ ДБХґФСРґЯЪ. оНґКНґФХґРЕКЭґМШЕ ХНМШ МЮґГШґБЮґЧРґЯЪ ЙЮґРХґНґМЮґЛХ, РЮЙ ЙЮЙ НМХ ДБХґФСРґЯЪ Й НРґПХґЖЮґРЕКЭґМН ГЮґПЪґФЕМґМНґЛС ЙЮґРНґДС, НРґПХґЖЮґРЕКЭґМШЕ ГЮґПЪґДШ МЮґГШґБЮґЧРґЯЪ ЮМХґНґМЮґЛХ ЙЮЙ ДБХґФСґЫХґЕґЯЪ Й ЮМНДС.
бШґЬЕґНОХґЯЮМґМНЕ ДЕИґЯРБХЕ БНДШ ОН ПЮГґПШґБС ЛНґКЕґЙСґКШ МЮ ДБЮ ХНМЮ МЮґГШґБЮґЕРґЯЪ ЩКЕЙґРПНґКХґРХґВЕґЯЙНИ ДХЯґЯНґЖХґЮґЖХґЕИ.
оНґЛХґЛН ПЮЯґРБНґПНБ, ОПНґБНДґМХґЙЮґЛХ БРНґПНґЦН ПНДЮ ЛНЦСР АШРЭ Х ПЮЯґОКЮґБШ. б ЩРНЛ ЯКСґВЮЕ МЮґКХґВХЕ ЯБНґАНДґМШУ ХНМНБ ДНґЯРХґЦЮґЕРґЯЪ РЕЛ, ВРН ОПХ БШґЯНґЙНИ РЕЛґОЕґПЮґРСґПЕ МЮґВХґМЮґЧРґЯЪ НВЕМЭ ЮЙґРХБґМШЕ ЛНґКЕґЙСґКЪПґМШЕ ДБХґФЕґМХЪ Х ЙНґКЕґАЮґМХЪ, Б ПЕґГСКЭґРЮґРЕ ЙНґРНґПШУ Х ОПНґХЯґУНґДХР ПЮГґПСґЬЕґМХЕ ЛНґКЕґЙСК МЮ ХНМШ.
| <== ОПЕДШДСЫЮЪ | | | ЯКЕДСЧЫЮЪ ==> |
| бХДШ ОПЮБНЯНГМЮМХЪ ПЮГЦПЮМХВХБЮЧРЯЪ ОН ЯСАЗЕЙРЮЛ-МНЯХРЕКЪЛ Х СПНБМЧ ОПЮБНЯНГМЮМХЪ | | |
Date: 2016-05-24; view: 674; мЮПСЬЕМХЕ ЮБРНПЯЙХУ ОПЮБ