
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Рассчитываем порядок связи. Смотрим, чем больше ne, тем прочнее молекула
|
|
Расставляем электроны согласно Принципам минимальной энергии, Паули, Гунда, Клечковского.
Записываем полную электронную формулу.
Смотрим, есть или нет неспаренные электроны. Определяем магнитные свойства вещества.
Рассчитываем порядок связи. Смотрим, чем больше ne, тем прочнее молекула.
N= 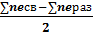
12. Выполняем задание:
|
N=∑e=∑p=17(Электронов)
∑n=Ar-N=35-17=18
 
|  
|  
| 
| ||||||
 
|  
|  
|  
| ||||||
 
|
Cl0: 1S22S22P63S23P53d0
Cl-: ∑e=17+1=18;
 | |||
 | |||
 
|  
|  
| 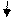 
| ||||||
 
|  
|  
|  
| ||||||
 
|
Cl-: 1S22S22P63S23P63d0
Cl+: ∑e=17-1=16
 
|  
| 
| 
| ||||||
 
|  
|  
|  
| ||||||
 
|
Cl+: 1S22S22P63S23P43d0
 Рисуем энергетическую диаграмму:
Рисуем энергетическую диаграмму:
3P
3S σ*3Sраз 3S
разрыхляющие
Расщепление на 4 уровня энергии
σ2px Cвязывающие
2s σ2S связ 2s
σ1S*раз
σ1S связ
Происходит расщепление энергетических уровней, так как одни уровни по энергии – ниже, а другие выше.Расставляем электроны согласно принципам минимальной энергии, Паули, Гунда, Клечковского, с двух сторон.
Всего расставляем 35 электронов: 17+18;
Сумма связующих электронов: 18;
Сумма разрыхляющих электронов – 17.
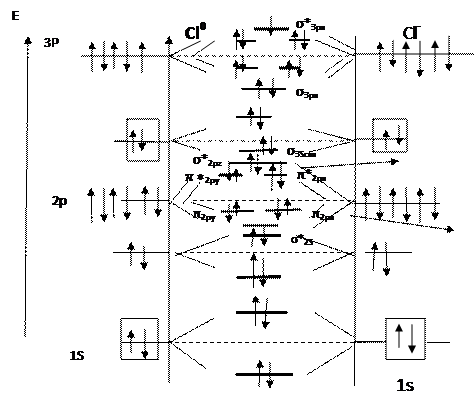
N= 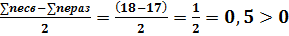 ;
;
Аналогично, строим для Cl2+
Cl+: 1S22S22P63S23P43d0
Всего расставляем 33 электрона: 17+16;





















 3P 3P
3P 3P
N= 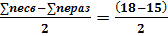 =3/2=1,5 (1,5:0,5 =3)
=3/2=1,5 (1,5:0,5 =3)
В молекулярном ионе Сl2+имеется избыток трех связывающих электронов, что соответствует полуторной связи или порядку связи, равному 1,5.
Увеличение количества связывающих электронов приводит к упрочнению связи и уменьшению межъядерного расстояния (длины связи). В молекулярном ионе Сl2+ имеется один неспаренный электрон, частица обладает магнитными свойствами (парамагнитна).
Порядок связи n определяется разностью количества электронов на СМО и РМО и показывает прочность молекулы. С увеличением порядка связи прочность связи (энергия связи) возрастает: 392 кДж/моль > 124 кДж/моль
| <== предыдущая | | | следующая ==> |
| | | Понятие «активные методы обучения» |
Date: 2015-05-22; view: 736; Нарушение авторских прав