
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Применение теории Бора к атому водорода
|
|
Для объяснения спектра атомарного водорода Н.Бор, основываясь на своих постулатах, сделал предположение, что в атоме водорода стационарными, разрешенными, устойчивыми орбитами являются только те орбиты, для которых момент импульса электрона равен целому кратному постоянной Планка, деленной на 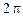 , т.е.
, т.е.
 , (19)
, (19)
где 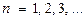 – главное квантовое число;
– главное квантовое число; 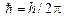 ;
; 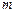 – масса электрона;
– масса электрона; 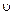 – скорость электрона;
– скорость электрона; 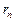 – радиус орбиты электрона.
– радиус орбиты электрона.
Исходя из этих представлений, вычислим радиусы стационарных орбит. Рассмотрим электрон, движущийся в поле атомного ядра с зарядом 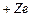 . При
. При 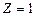 такая система соответствует атому водорода, при иных
такая система соответствует атому водорода, при иных 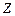 – водородоподобному иону, т.е. атому с порядковым номером
– водородоподобному иону, т.е. атому с порядковым номером 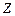 , из которого удалены все электроны, кроме одного.
, из которого удалены все электроны, кроме одного.
На электрон действует кулоновская сила притяжения к ядру, которая является центростремительной. Согласно второму закону Ньютона
 . (20)
. (20)
Из (19) получаем: 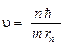 . Подставляем в (20):
. Подставляем в (20):
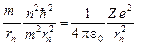 .
.
Получаем радиус 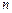 -й орбиты электрона:
-й орбиты электрона:
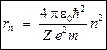 . (21)
. (21)
Для первой орбиты атома водорода (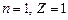 ) получим:
) получим:
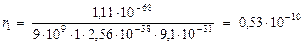 (м),
(м),
т.е. порядка газокинетических размеров атома.
Энергия электрона в атоме слагается из его потенциальной энергии в электрическом поле ядра:
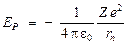
и кинетической энергии его движения по орбите со скоростью 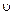 :
:
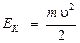 .
.
Таким образом, полная энергия электрона 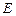 равна:
равна:
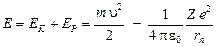 . (22)
. (22)
Из формулы (20) получаем:
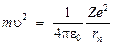 . (23)
. (23)
Подставляя (23) в (22), получаем выражение для полной энергии:
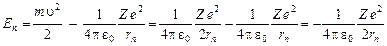 .
.
 Подставляя в это выражение значение радиуса из (21), получаем:
Подставляя в это выражение значение радиуса из (21), получаем:
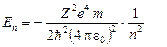 .
.
Таким образом, схема энергетических уровней атома водорода будет иметь вид, изображенный на рис. 14.
Согласно формуле (18) при переходе электрона из одного энергического состояния в другое испускается квант электромагнитной волны с энергией:
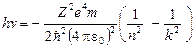 .
.
Следовательно, частота излучаемого света будет равна:
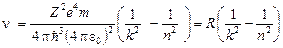 . (24)
. (24)
Сравнивая (24) и (16), получаем, что постоянная Ридберга должна определяться выражением:
 .
.
Таким образом, получено теоретическое выражение для постоянной Ридберга. Подставляя значения универсальных констант, получаем:
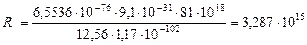 с-1.
с-1.
Полученное значение очень хорошо согласуется с экспериментальным, найденным из спектроскопических данных.
Подставляя в формулу (15) 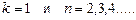 , получаем группу линий, образующих серию Лаймана (24) и соответствующих переходам электронов с возбуждённых уровней (
, получаем группу линий, образующих серию Лаймана (24) и соответствующих переходам электронов с возбуждённых уровней (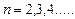 ) на основной (
) на основной (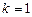 ). Аналогично при подстановке
). Аналогично при подстановке 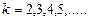 и соответствующих им значений
и соответствующих им значений 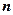 получим серии Бальмера, Пашена, Пфунда и т.д.
получим серии Бальмера, Пашена, Пфунда и т.д.
Следовательно, по теории Бора спектральные серии соответствуют излучению, возникающему в результате перехода атомов в данное состояние из возбуждённых состояний, расположенных выше данного.
Итак, теория атома Бора в применении к атому водорода дала поразительно точные результаты.
Теория Бора показала, что к внутриатомным процессам нельзя применять понятия классической физики.
Date: 2015-05-19; view: 741; Нарушение авторских прав