
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретические сведения. Цель работы: ознакомление с устройством, работой и градуировкой призменного спектроскопа; изучение спектра водорода и определение постоянной Ридберга
|
|
Лабораторная работа № 3.2
ИЗУЧЕНИЕ СПЕКТРА ВОДСРОДА И ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ РИДБЕРГА
Цель работы: ознакомление с устройством, работой и градуировкой призменного спектроскопа; изучение спектра водорода и определение постоянной Ридберга.
Оборудование: спектроскоп, неоновая и водородная лампы.
Теоретические сведения
Линейчатые спектры, присущие атомам разреженных газов в простейшем случае (для атоме водорода и водородоподобных систем) хорошо объясняются полуклассической теорией Бора, основанной на трех постулатах.
1й- постулат -: существуют стационарные состояния атомов, находясь в которых атом не излучает энергии. Стационарным состояниям соответствует движение электрона по определенным стационарным орбитам. Находясь на ней, электрон, несмотря на наличие ускорения, не излучает энергии.
2й- постулат -: при переходе атома из, одного стационарного состояния в другое атом излучает (или поглощает) квант энергии. Величина кванта энергии равна разности энергий, соответствующих тем стационарным состояниям, между которыми совершается переход:
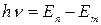 (1)
(1)
где n - частота излучения, h - постоянная Планка, En и Em - энергия атома в стационарных состояниях, между которыми совершается переход;. Если En>Em - атом излучает квант энергии; если En<Em - атом поглощает квант энергии.
3й – постулат –: электрон в атоме движется по таким (стационарным) круговым орбитам, для которых момент импульса электрона 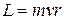 кратен величине
кратен величине 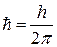
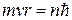 (2)
(2)
где m - масса электрона, v - его скорость, r - радиус круговой стационарной орбиты, n = 1, 2, 3. целое число.
Стационарное состояние, таким образом, характеризуется дискретными (квантованными) значениями энергии Еn и момента импульса Ln. Согласно теории Бора для атома водорода:
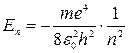 (3)
(3)
где e - заряд электроне.
Тогда частоты спектральных линии атома водорода при переходе с орбиты с энергией Еn2 на орбиту с энергией: En1 будут следующие:
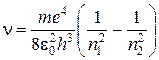 (4)
(4)
Величина 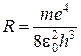 называется постоянной Ридберга для атома водорода. Тогда:
называется постоянной Ридберга для атома водорода. Тогда:
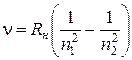 (5)
(5)
|где n1. - номер, стационарного состояния (т.е. энергетического уровня), на который совершается переход, n2, - с которого совершается переход.
При переходе электронов в атоме водорода на орбиту с наименьшей энергией (n 1 = 1) излучается серия линий, лежащих в ультрафиолетовой части спектра (серия Ланмана). При -переходе на орбиту с n1 = 2 излучаются линии серии Бальмера, четыре линяй которой лежат в видимой части спектра.
На рис. 1 числа у коротких стрелок указывают наибольшую длину волны в Å данной серия. По оси указаны значения энергии в электронвольтах.
Следует заметить, что по современным представлениям нельзя говорить об орбитах как о траекториях истинного движения электронов. Движение; электрона описывается с учетом его волновых свойств уравнением Шредингера.
Однако представление о стационарных уровнях энергии атома остается в силе на основе более точной квантовой теории.
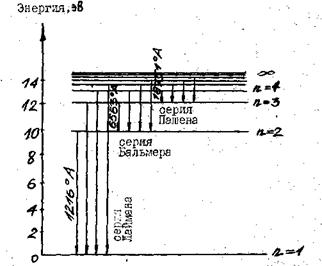
Рис. 1. Схема энергетических, уровней и излучательных переходов для атома водорода
| <== предыдущая | | | следующая ==> |
| | |
Date: 2015-05-18; view: 424; Нарушение авторских прав