
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

I-е начало термодинамики
|
|
Термодинамика базируется на первом и втором началах (законах).
Первое начало термодинамики представляет собой одну из форм записи закона сохранения энергии. Оно было сформулировано независимо друг от друга Ю.Р. Майером (1842г.), Д.П. Джоулем (1843г.) и Г.Л. Гельмгольцем (1847г.). Двое из них (Майер и Гельмгольц) были врачами и закладывали основы термодинамики, рассматривая преобразования энергии как в живой, так и в неживой природе.
Смысл первого начала термодинамики сводится к тому, что изменение внутренней энергии системы может произойти только при обмене энергией с окружающей средой.
Энергетический обмен между системой и средой осуществляется двумя способами – посредством передачи тепла и путём совершения работы.
 ;
; 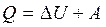
Этот вид формул и выражает I начало термодинамики.
Q – количество теплоты, переданное системе;
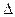 U – изменение внутренней энергии системы;
U – изменение внутренней энергии системы;
А – работа, совершаемая системой.
В живых организмах формы совершения работы очень разнообразны (Аi).
Остановимся на способах совершения работы:
- механическая работа dA(l) =Fdl, где F – сила, l – перемещение;
- работа расширения газа dA(V) =pdV, где p – давление, V – изменение объёма.
- работа переноса заряда, при разности потенциалов 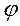 , dA(A) =
, dA(A) = 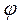 dq, где
dq, где
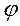 - потенциал, q – электрический заряд;
- потенциал, q – электрический заряд;
- работа переноса работа переноса вещества за счёт осмотического давления
dA(C) = pосмdc, где pосм -осмотическое давление, с – концентрация вещества;
- работа, совершаемая при химической реакции dA( 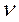 )=
)= 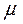 xd
xd 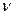 ,
,
где 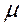 x –химический потенциал,
x –химический потенциал, 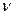 - число молей вещества, вступающих в реакцию;
- число молей вещества, вступающих в реакцию;
Все эти формулы имеют сходную структуру dA(x)=Xdx A= 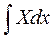 ,
,
где х – величина, характеризующая перенос (V, q, c, 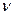 ), а Х – сила, характеризующая причину переноса (F, p,
), а Х – сила, характеризующая причину переноса (F, p,  , pосм,
, pосм, 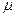 x).
x).
Используя принятые обозначения, основной закон термодинамики можно записать в виде


То есть количество тепла (Q), полученное системой, определяется изменениями внутренней энергии (DU), а также суммой всех видов работы (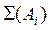 ), совершаемой системой.
), совершаемой системой.
Эту формулу можно считать наиболее общим выражением первого начала термодинамики.
ПРИМЕНЕНИЕ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ
К ЖИВЫМ СИСТЕМАМ (ОРГАНИЗМАМ)
(Различие термодинамических процессов в живой и неживой системах)
Классическая форма первого начала термодинамики отображает запросы теплотехники, интенсивно развивающиеся в эпоху открытия этого основного закона. Поэтому эта форма не вполне удобна для биологии, т.к. не отображает сути термодинамических процессов, происходящих в живых системах. В отличие от тепловых машин, живые организмы производят работу не за счёт тепловой энергии, а посредством использования химической энергии пищевых продуктов, усвоенных ими (Wпищи).
Поэтому для живой системы 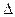 U = Wпища – Q – A (перед Q стоит знак «–», т.к. биологическая система отдаёт тепло окружающей среде).
U = Wпища – Q – A (перед Q стоит знак «–», т.к. биологическая система отдаёт тепло окружающей среде).
Организм гомойотермных животных имеет постоянную температуру, химический состав его в среднем не изменяется, поэтому U=const и DU=0. Учитывая это, предыдущую формулу можно записать так: 0 = Wпищи – Q – A
или Wпищи = Q + A, если при этом помнить, что совершаемая работа (АС) и теплообмен (Q) могут иметь разнообразные формы, то получаем, что
Wпищи = 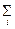 Q +
Q + 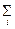 A
A
Эта форма наиболее точно отображает первое начало термодинамики для биологических систем.
Итак, термодинамические процессы в тепловой машине можно представить схемой (источник энергии на Земле – Солнце)
(неживая система) Wc 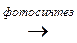 Wтоплива
Wтоплива  Q ® DU+A,
Q ® DU+A,
где в биологической системе
(живая система) Wc  Wпищи
Wпищи 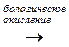 DU+A+Q
DU+A+Q
Wc – энергия солнца Wt – энергия топлива Wn– энергия пищи.
В живой системе между Wc и последним значением A отсутствует промежуточное звено в форме тепловой энергии, следовательно, КПД живой системы выше, чем у неживой и достигает значения 20-60 %.
Таким образом, обмен веществ в организме сопровождается процессами превращения энергии. Обмен энергии и вещества представляет собой единый процесс, лежащий в основе жизнедеятельности. Живой организм расходует химическую энергию всех рабочих процессов, выполняемых в организме, и выделяет избыточное количество тепла (тепловой эффект).
Date: 2015-05-09; view: 1527; Нарушение авторских прав