
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Энтальпийный и энтропийный факторы процесса. Энергия Гиббса
|
|
Направление протекания процесса определяется двумя противоположными тенденциями:
1) стремлением системы перейти в состояние с наименьшей энергией;
2) стремлением системы перейти в состояние с наибольшей энтропией.
В реальных химических процессах происходит одновременное изменение и энтальпии, и энтропии системы. Для учета обоих этих факторов вводится новая функция состояния системы:
G = H – TS
G – энергия Гиббса; свободная энергия; изобарно-изотермический потенциал.
Для процессов, протекающих при T=const и p=const:
DG = DH - TDS
Изменение энергии Гиббса равно по абсолютной величине максимальной полезной работе, которую может совершить система:
DG = - Amax
Таким образом общий энергетический эффект процесса DН можно представить как сумму двух составляющих:
DH = DG + TDS,
где DG – это та часть энергии, которую можно превратить в работу (“свободная” энергия); TDS – “связанная” энергия, которая ни при каких условиях не может быть превращена в работу и неизбежно рассеивается в виде теплоты.
Знак величины DG однозначно определяет направление самопроизвольного протекания процесса в изобарно-изотермических условиях. Согласно второму закону термодинамики:
При p=const и T=const самопроизвольно могут протекать процессы в направлении уменьшения энергии Гиббса (DG<0).
Термодинамические процессы могут быть обратимыми и необратимыми. Обратимые процессы заканчиваются установлением равновесия. Равновесие – это такое состояние системы, при котором все ее параметры остаются постоянными как угодно долго при отсутствии внешних воздействий. Равновесие – это динамическое состояние. Оно означает не отсутствие процессов в системе, а равенство скоростей прямого и обратного процессов.
Процесс будет протекать самопроизвольно только в направлении, приближающем систему к состоянию равновесия. В состоянии равновесия энергия Гиббса принимает минимальное значение и не изменяется:
DG<0 – процесс протекает самопроизвольно в прямом направлении;
DG=0 – состояние равновесия
DG>0 – самопроизвольное протекание прямого процесса невозможно (самопроизвольно протекает обратная реакция, для которой DG<0).
Соотношение энтальпийного (DН) и энтропийного (TDS) факторов процесса:
1) если DН<0 и DS>0, то DG<0 всегда, т.е. процесс протекает самопроизвольно при любых Т;
2) если DН>0 и DS<0, то DG>0 всегда, т.е. процесс невозможен ни при каких Т;
3) если DH<0 и DS<0, то DG<0) при условии ÷DHô>ôTDS÷, т.е. процесс протекает самопроизвольно при низких температурах;
4) если DH>0 и DS>0, то DG<0) при условии ÷DHô<ôTDS÷, т.е. процесс протекает самопроизвольно при высоких температурах.
Энергия Гиббса – это функция состояния системы. Ее изменение DG в процессе может быть рассчитано на основании закона Гесса и его следствий. Стандартные энергии Гиббса образования веществ D 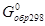 [кДж/моль] приводятся в справочных таблицах. Стандартные энергии Гиббса образования простых веществ принимаются равными нулю.
[кДж/моль] приводятся в справочных таблицах. Стандартные энергии Гиббса образования простых веществ принимаются равными нулю.
Для того чтобы определить, будет ли процесс протекать самопроизвольно при стандартном состоянии и данной температуре, необходимо рассчитать D 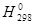 и D
и D 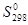 процесса, а затем определить знак D
процесса, а затем определить знак D 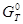 при данной температуре.
при данной температуре.
Date: 2015-05-09; view: 1776; Нарушение авторских прав