
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Водородный электрод
Водородный электрод (рис. 7) представляет собой покрытую платиновой чернью платиновую пластинку, насыщенную газообразным водородом, которая опущена в водный раствор кислоты.
Водород, растворенный в платине, частично диссоциирует на протоны и электроны: Н2↔2Н+ + 2ē
В результате такая платиновая пластинка приобретает способность обмениваться с раствором ионами водорода:
Н+(Рt) + Н2О↔Н3О+(Рt)
Возникающий при этом потенциал зависит от активности ионов водорода в растворе и ионов водорода в платине
Н3О+(р) +2ē↔ Н2(Рt) +2Н2О
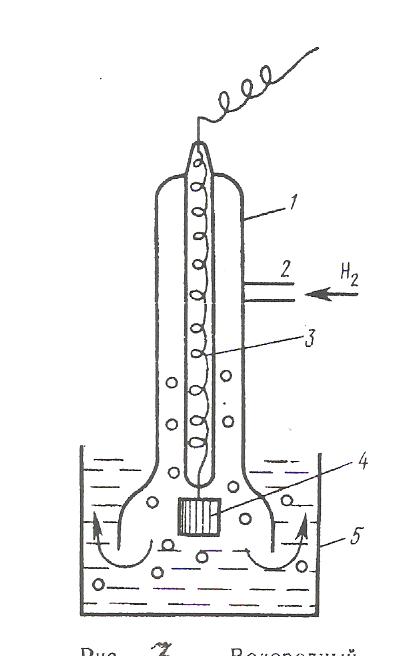 Рис. 7. Водородный электрод: 1,3 – стеклянные трубки;2 – патрубок для ввода водорода; 4- платинированные платиновый электрод; 5 – сосуд с исследуемым раствором
Рис. 7. Водородный электрод: 1,3 – стеклянные трубки;2 – патрубок для ввода водорода; 4- платинированные платиновый электрод; 5 – сосуд с исследуемым раствором
|
Активность ионов водорода в платине пропорциональна давлению газообразного водорода. Количественно эта зависимость выражается уравнением Нернста:
RT a²(н+)
φн2 = φ° н2 + ln
F р(н2)
где р(н2) – давление газообразного водорода, Па.
Стандартным водородным электродом (φ°н2) называют электрод, в котором давление газообразного водорода поддерживается равным 101 кПа, а активность ионов водорода в растворе равна 1.
Потенциал стандартного водородного электрода условно принят за нуль: φ°н2 = 0
При всех других активностях ионов водорода при условии, что р(н2)=101 кПа уравнение Нернста для водородного электрода принимает вид
RT
φ°н2= ln a (н+),
F
или с учетом, что – lg а (н+) =рН
RT
φ°н2 = - 2,3 · рН
F
Стандартный водородный электрод используется как электрод, относительно которого измерены потенциалы всех остальных стандартных электродов.
Стандартный электродный потенциал численно равен электродвижущей силе со знаком «+» или «–» гальванического элемента, составленного из стандартного водородного и стандартного данного электродов.
Например, цепь с цинковым электродом
Zn|ZnSO4||H2SO4|H2, Pt
ЭДС водородно-цинковой цепи будет равна
Е °= φ°н2 - φ°Zn;
φ°Zn = - Е°
в случае медно – водородной гальванической цепи ЭДС равна
Pt, H2 | H2SO4 | CuSO4 | Cu
Е°= φ°Cu - φ°н2
φ°Cu = Е°
Date: 2015-09-17; view: 594; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |