
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Средства, влияющие на лейкопоэз
Средства, стимулирующие лейкопоэз
Натрия нуклеинат
Пентоксил
Молграмостим
Филграстим
Средства, угнетающие лейкопоэз
Новэмбихин
Миелосан
Меркаптопурин
Допан
Тиофосфамид и др. (см. главу 32)
18.1. СРЕДСТВА, ВЛИЯЮЩИЕ НА ЭРИТРОПОЭЗ
Из стимуляторов эритропоэза, применяемых при гипохромной анемии, основную роль играют препараты железа.
Основой развития гипохромной анемии является недостаточная продукция гемоглобина эритробластами костного мозга в связи с дефицитом железа или с нарушением его метаболизма.
Железо содержится в организме в количестве 2-5 г. Основная его часть (2/3) входит в состав гемоглобина. Остальная часть находится в тканевых депо (в костном мозге, печени, селезенке). Железо входит также в состав миоглобина и ряда ферментов.
Из желудочно-кишечного тракта всасывается только ионизированное железо, причем лучше всего в виде двухвалентного иона (схема 18.1). В связи с этим наличие хлористоводородной кислоты (переводит молекулярное железо в ионизированную форму) и аскорбиновой кислоты (восстанавливает трехвалентное железо в двухвалентное) способствует всасыванию железа из пищеварительного тракта. Всасывание происходит главным образом в тонкой кишке (особенно в двенадцатиперстной кишке) за счет активного транспорта и, возможно, путем диффузии. Содержащийся в слизистой оболочке кишечника белок апоферритин связывает часть всасывающегося железа, образуя с ним комплекс — ферритин. После прохождения кишечного барьера железо в сыворотке крови вступает в связь с β1-глобулином — трансферрином. В виде комплекса с трансферрином железо поступает к различным тканям, где вновь высвобождается. В костном мозге оно включается в построение гемоглобина. Что касается тканевых депо, то в них железо находится в связанном состоянии (в виде ферритина или гемосидерина).
Интенсивность всасывания железа в значительной степени зависит от степени насыщения им белков, участвующих в его транспорте и депонировании (апоферритина слизистой оболочки кишечника, трансферрина плазмы крови, апоферритина тканевых депо).
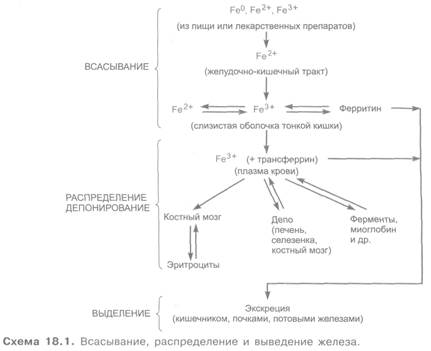
Выводится железо пищеварительным трактом (невсосавшаяся часть; с эпителием слизистой оболочки, который подвергается десквамации; с желчью), почками и потовыми железами.
Применяют препараты железа при железодефицитной гипохромной анемии (например, при хронических кровотечениях, нарушениях всасывания железа, при беременности). Внутрь назначают железа закисного сульфат (FeSO4∙7H2O), железа закисного лактат [(CH3CHOHCOO)2Fe∙ЗН2О].
Принимают эти препараты в таком виде, чтобы избежать контакта железа с полостью рта (например, в капсулах, драже с соответствующим покрытием). Такая необходимость обусловлена тем, что при взаимодействии железа с сероводородом (образуется при кариесе зубов и других заболеваниях полости рта) выделяется сульфид железа, который окрашивает зубы в черный цвет.
Применяют также комбинированные препараты железа, например драже «Ферроплекс» (содержит железа закисного сульфат и кислоту аскорбиновую), ферамид (комплексное соединение железа с никотинамидом). Создан также препарат пролонгированного действия ферро-градумет (таблетки, покрытые оболочкой и содержащие железа закисного сульфат в полимерной губкообразной массе — градумете; последняя обеспечивает постепенное всасывание железа).
Препараты железа могут приводить к развитию запора. Объясняется это связыванием сероводорода кишечника, который является физиологическим стимулятором его моторики.
Если всасывание железа из пищеварительного тракта нарушено, используют препараты для парентерального введения, например ферковен (содержит железа сахарат, кобальта глюконат и раствор углеводов), феррум Лек (комплекс железа с мальтозой для внутримышечного введения и железа сахарат для внутривенного введения) и др. При передозировке ферковена появляются гиперемия кожи лица, шеи, боли в пояснице, ощущение сдавления в области груди. Введение анальгетиков и атропина сульфата устраняет эти явления.
При гипохромной анемии применяют также некоторые препараты кобальта. Одним из них является коамид. По химической структуре представляет собой комплексное соединение кобальта с амидом никотиновой кислоты. Кобальт стимулирует эритропоэз и способствует усвоению железа для образования гемоглобина. Вводят коамид подкожно.
За последние годы арсенал противоанемических средств пополнился человеческим рекомбинантным эритропоэтином, являющимся фактором роста, регулирующим эритропоэз (табл. 18.1). По химической структуре это гликопротеин. В организме эритропоэтин в основном образуется в перитубулярных интерстициальных клетках почек (90%) и в печени (10%). Стимулирует пролиферацию и дифференцировку красных кровяных клеток. Соответствующие препараты выпускаются под названием эпоэтин альфа (эпоген, эпрекс) и эпоэтин бета (рекормон).
Применяют их при анемии, связанной с хронической недостаточностью почек, с ревматоидным артритом, злокачественными опухолями, СПИДом при анемии у недоношенных детей.
Эффект развивается через 1-2 нед, нормализация кроветворения наступает через 8-12 нед. Если имеется дефицит железа, эпоэтин следует применять с препаратами железа. Вводят препарат внутривенно и подкожно (в пищеварительном тракте он разрушается), t1/2 ~ 9,3 ч. Переносится хорошо. Из побочных эффектов возможны головная боль, артралгия, гиперкалиемия.
При гиперхромной анемии применяют цианокобаламин и кислоту фолиевую (см. главу 21), участвующие в синтезе нуклеиновых кислот.
Цианокобаламин (витамин В12) назначают при злокачественной (пернициозной) анемии.
При дефиците цианокобаламина эритропоэз протекает по мегалобластическому типу: эритробласт → гиперхромный мегалобласт → мегалоцит.
Возникновение пернициозной анемии связано с нарушением всасывания цианокобаламина, поскольку у таких больных отсутствует внутренний фактор Касла (по химической структуре — гликопротеин). В обычных условиях он вырабатывается слизистой оболочкой желудка и обеспечивает всасывание цианокобаламина в тонкой кишке.
| Таблица 18.1Сравнительная характеристика колониестимулирующих факторов (факторов роста, регулирующих гемопоэз) | |||
| Препарат | Стимуляция созревания, дифференцировки и пролиферации клеток-прекурзоров | Побочные эффекты | Объекты для получения препаратов методом рекомбинантной ДНК-технологии |
| Эритропоэтин | Эритроцитов | Головная боль, артралгия, гиперкалиемия, кожная сыпь | Escherichia соli |
| Филграстим (G-CSF) | Нейтрофилов | «Костные» боли, кожная сыпь | Клетки дрожжевого гриба |
| Молграмостим (GM-CSF) | Нейтрофилов, эозинофилов, базофилов, эритроцитов, макрофагов | Пирогенная реакция, «костные» боли, диспепсия, гипотензия, кожная сыпь | Escherichia coli |
| Сарграмостим (GM-CSF) | То же | То же | Клетки яичника китайского хомяка |
Цианокобаламин при злокачественной анемии нормализует картину крови, а также устраняет или ослабляет неврологические нарушения и поражения слизистой оболочки языка. Ахлоргидрия желудочного сока сохраняется.
Кислоту фолиевую (витамин Вс) назначают при макроцитарной анемии.
При дефиците кислоты фолиевой образуются макроциты: эритробласт → гиперхромный макронормобласт → макроцит.
В организме кислота фолиевая превращается в фолиниевую, которая и обладает физиологической активностью.
Кислоту фолиевую используют при алиментарной и медикаментозной макроцитарной анемии, спру, анемии беременных. Для лечения злокачественной анемии кислоту фолиевую отдельно не назначают, так как она не только не устраняет патологические изменения со стороны нервной системы, но даже усиливает их. Нормализуется лишь картина крови. В связи с этим при злокачественной анемии кислота фолиевая комбинируется с цианокобаламином.
Средства, угнетающие эритропоэз, используют при полицитемии (эритремии). Одним из таких средств является раствор натрия фосфата, меченного фосфором-32 (Na2H32PO4). Применение его приводит к снижению числа эритроцитов, тромбоцитов. Вводят препарат внутрь или внутривенно. Дозируют в милликюри (мКи).
18.2. СРЕДСТВА, ВЛИЯЮЩИЕ НА ЛЕЙКОПОЭЗ
При лейкопении и агранулоцитозе (при агранулоцитарной ангине, алиментарно-токсической алейкии, при отравлении рядом химических веществ, при лучевой болезни) используют средства, стимулирующие лейкопоэз. С этой целью применяют натрия нуклеинат, пентоксил. Однако они эффективны только при легких формах лейкопений.
Натрия нуклеинат — это натриевая соль нуклеиновой кислоты, получаемой из дрожжей. Применяют для стимуляции образования костным мозгом лейкоцитов. Вводят внутрь и внутримышечно.
Пентоксил относится к синтетическим препаратам. По химическому строению он является производным пиримидина. Стимулирует лейкопоэз, ускоряет заживление ран, обладает противовоспалительным эффектом. Принимают его внутрь. Может вызывать диспепсические нарушения. Аналогичными свойствами обладает метилурацил, но в отличие от пентоксила раздражающего действия у него нет.
Иногда используют лейкоген, батилол, этаден и др.
При лейкопениях применяют также факторы роста, регулирующие лейкопоэз. Путем генной инженерии в последнее время удалось создать соответствующие лекарственные препараты (см. табл. 18.1). Одним из них является рекомбинантный человеческий гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF). Препарат получил название молграмостим (лейкомакс). Он является гликопротеином. Образуется в Т-лимфоцитах, эндотелиальных клетках, фибробластах, макрофагах. Стимулирует пролиферацию, дифференцировку и функцию гранулоцитов и моноцитов/макрофагов. Гранулоциты и моноциты/макрофаги образуют одну из важных систем защиты организма. Они осуществляют фагоцитоз, секретируют биологически активные соединения, стимулируют иммунные процессы, регулируют продукцию цитокинов. Наличие отмеченных механизмов позволяет расценивать ее как систему защиты организма от бактерий, грибов, паразитов, опухолевых поражений.
Молграмостим в небольшой степени стимулирует пролиферацию эозинофилов и является кофактором эритропоэтина в регуляции эритропоэза.
Применяют его при угнетении лейкопоэза, связанном с химиотерапией опухолей, при миелодиспластическом синдроме, апластической анемии, лейкопении, вызванной различными инфекциями, при пересадке костного мозга, в комплексной терапии СПИДа. Вводят внутривенно.
Возможные побочные эффекты: тошнота, рвота, анорексия, диарея, гипертермия, кожные высыпания и другие аллергические реакции, мышечно-скелетные боли и пр.
Создан и рекомбинантный человеческий гранулоцитарный колониестимулирующий фактор (G-CSF). Препарат известен под названием филграстим (нейпоген). Он является гликопротеином. Продуцируется моноцитами, фибробластами и клетками эндотелия. Стимулирует пролиферацию и дифференцировку предшественников гранулоцитов и активность (хемотаксическую и фагоцитарную) зрелых гранулоцитов (нейтрофилов).
Показания к применению филграстима те же, что и для молграмостима. Вводят препарат внутривенно и подкожно.
Побочные эффекты наблюдаются редко. Возможны «костные» боли, иногда аллергические реакции, нарушения функции печени, дизурия.
Средства, угнетающие лейкопоэз, применяют при лейкозах и лимфогранулематозе (см. главу 32).
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Средства, стимулирующие эритропоэз | ||
| Железа закисного лактат — Ferri lactas | Внутрь 1 г | Порошок |
| Ферковен — Fercovenum | Внутримышечно 2-5 мл | Ампулы по 5 мл |
| Коамид — Coamidum | Внутрь 0,1 г; под кожу 0,01 г | Порошок; ампулы по 1 мл 1% раствора |
| Эпоэтин альфа — Epoetin alfa | Внутривенно и подкожно по 30-100 ЕД на 1 кг массы тела 3 раза в неделю | Раствор для инъекций в шприцах по 1000; 2000; 3000; 4000 и 10 000 ЕД; раствор для инъекций во флаконах по 1 мл (2000; 4000 и 10 000 ЕД) |
| Цианокобаламин — Cyanocobalaminum | Подкожно, внутримышечно и внутривенно 0,0001-0,0005 г | Ампулы по 1 мл 0,003%, 0,01%, 0,02% и 0,05% раствора |
| Средства, стимулирующие лейкопоэз | ||
| Натрия нуклеинах — Natrii nucleinas | Внутрь 0,25-1 г; внутримышечно 0,1-0,5 г (в виде 2% и 5% раствора) | Порошок |
| Пентоксил — Pentoxylum | Внутрь 0,2-0,3 г | Порошок; таблетки, покрытые оболочкой, по 0,2 г |
| Филграстим — Filgrastim | Внутривенно и подкожно 5 мкг на 1 кг массы тела | Флаконы по 0,3 и 0,48 мг |
| Молграмостим —Molgramostim | Подкожно и внутривенно (капельно) 1 0 мкг/кг | Лиофилизированный порошок во флаконах по 50; 150; 300; 400; 500 и 700 мкг |
Гл а в а 19
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ВЛИЯЮЩИЕ НА АГРЕГАЦИЮ ТРОМБОЦИТОВ, СВЕРТЫВАНИЕ КРОВИ И ФИБРИНОЛИЗ
Процесс гемостаза обеспечивает тромбообразующая система (агрегация тромбоцитов, свертывание крови), которая функционально взаимосвязана с тромболитической (фибринолитической) системой. В организме эти две системы находятся в динамическом равновесии и в зависимости от конкретных условий преобладает одна или другая. Так, если повреждается сосуд и возникает кровотечение, сосуд спазмируется, активируются агрегация тромбоцитов и свертывание крови, образуется тромб и кровотечение останавливается. Вместе с тем в норме чрезмерного тромбообразования не происходит, так как оно лимитируется процессом фибринолиза. В последующем фибринолитическая система обеспечивает постепенное растворение тромба и восстанавливает проходимость сосуда. При нарушенном равновесии между свертывающей и противосвертывающей системами может возникать либо повышенная кровоточивость, либо распространенный тромбоз. Оба состояния требуют коррекции путем назначения лекарственных препаратов.
Средства, влияющие на тромбообразование, могут быть систематизированы следующим образом.
I. Средства, применяемые для профилактики и лечения тромбоза
1. Средства, уменьшающие агрегацию тромбоцитов (антиагреганты)
2. Средства, понижающие свертывание крови (антикоагулянты)
3. Фибринолитические средства (тромболитические средства)
II. Средства, способствующие остановке кровотечений (гемостатики)
1. Средства, повышающие свертывание крови
а) для местного применения
б) системного действия
2. Антифибринолитические средства
19.1. СРЕДСТВА, ПРИМЕНЯЕМЫЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТРОМБОЗА
Данная группа препаратов имеет широкое применение в медицинской практике. Она используется при лечении тромбофлебитов, в комплексной терапии инфаркта миокарда, для профилактики тромбоэмболии, при нарушениях микроциркуляции и т.д. Средства, препятствующие тромбообразованию, могут действовать на различных этапах этого процесса. Так, они могут влиять на агрегацию тромбоцитов и эритроцитов, на образование нитей фибрина, на процесс фибринолиза. Кроме того, действие их может быть направлено на гемодинамику, морфофункциональное состояние сосудистой стенки, химический состав плазмы крови.
19.1.1. СРЕДСТВА, УМЕНЬШАЮЩИЕ АГРЕГАЦИЮ ТРОМБОЦИТОВ (АНТИАГРЕГАНТЫ)
Агрегация тромбоцитов в значительной степени регулируется системой тромбоксан—простациклин. Оба соединения образуются из циклических эндопероксидов, являющихся продуктами превращения в организме арахидоновой кислоты (см. схему 24.1), и действуют соответственно на тромбоксановые и простациклиновые рецепторы.
Тромбоксан А2 (ТХА2) повышает агрегацию тромбоцитов и вызывает выраженную вазоконстрикцию (рис. 19.1). Синтезируется он в тромбоцитах. Механизм стимулирующего действия тромбоксана на агрегацию тромбоцитов, очевидно, связан со стимуляцией фосфолипазы С вследствие влияния на тромбоксановые рецепторы, что увеличивает образование инозитол 1,4,5-трифосфата и диацилглицерола и таким путем повышает содержание в тромбоцитах Са2+. Тромбоксан — соединение очень нестойкое (t1/2 = 30 с при 37 °С).
Наряду с тромбоксаном к числу стимуляторов агрегации тромбоцитов относятся также коллаген сосудистой стенки, тромбин, АДФ, серотонин, простагландин Е2, катехоламины.
Прямо противоположную роль играет простациклин (простагландин I2). Он препятствует агрегации тромбоцитов и вызывает вазодилатацию. Это наиболее активный эндогенный ингибитор агрегации тромбоцитов. В больших концентрациях он угнетает адгезию (прилипание) тромбоцитов к субэндотелиальному слою стенки сосудов (препятствует их взаимодействию с коллагеном).
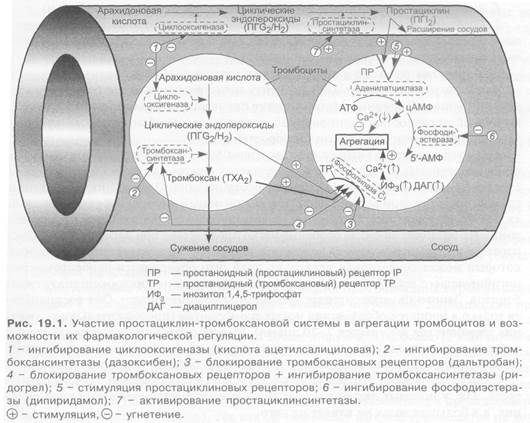
Синтезируется простациклин в основном эндотелием сосудов; наибольшее его количество содержится в интиме сосудов. Простациклин циркулирует также в крови. Основное его действие заключается в том, что он стимулирует простациклиновые рецепторы и связанную с ними аденилатциклазу и повышает содержание цАМФ в тромбоцитах и стенке сосудов (содержание внутриклеточного Са2+ снижается).
Помимо простациклина, агрегацию понижают простагландины E1 и D, окись азота (NO), гепарин, АМФ, аденозин, антагонисты серотонина и др.
Для практических целей основное значение имеют средства, препятствующие агрегации тромбоцитов. Действуют они в следующих направлениях:
I. Угнетение активности тромбоксановой системы
1. Снижение синтеза тромбоксана
а. Ингибиторы циклооксигеназы (кислота ацетилсалициловая)
б. Ингибиторы тромбоксансинтетазы (дазоксибен)
2. Блок тромбоксановых рецепторов
3. Вещества смешанного действия (1б + 2; ридогрел)
II. Повышение активности простациклиновой системы
1. Средства, стимулирующие простациклиновые рецепторы (эпопростенол)
III. Средства, угнетающие связывание фибриногена с тромбоцитарными гликопротеиновыми рецепторами (GP IIb/IIIa)
1. Антагонисты гликопротеиновых рецепторов (абциксимаб, тирофибан)
2. Средства, блокирующие пуриновые рецепторы тромбоцитов и препятствующие стимулирующему действию на них АДФ (гликопротеиновыерецепторы при этом не активируются) (тиклопидин, клопидогрел)
IV. Средства разного типа действия (дипиридамол, антуран).
Наиболее распространенным в практике антиагрегантом является кислота ацетилсалициловая (аспирин). Многие другие препараты либо обладают относительно низкой активностью (дипиридамол, антуран, дазоксибен), либо малоудобны для введения обычными путями (эпопростенол).
Кислота ацетилсалициловая (см. главы 8; 8.2 и 24) является ингибитором циклооксигеназы, вследствие чего нарушается синтез циклических эндопероксидов и их метаболитов тромбоксана и простациклина. Однако циклооксигеназа тромбоцитов более чувствительна, чем аналогичный фермент сосудистой стенки. Поэтому синтез тромбоксана подавляется в большей степени, чем простациклина. Это различие эффекта особенно четко проявляется при использовании препарата в небольших дозах. В результате преобладает антиагрегантный эффект, который может сохраняться несколько дней, что объясняется необратимостью ингибирующего действия кислоты ацетилсалициловой на циклооксигеназу тромбоцитов. Заново циклооксигеназу тромбоциты не синтезируют. Она восполняется только в процессе образования новых тромбоцитов (продолжительность «жизни» тромбоцитов измеряется 7-10 днями). Вместе с тем циклооксигеназа стенки сосудов восстанавливает свою активность в течение нескольких часов. Поэтому длительность снижения содержания тромбоксана больше, чем простациклина.
Следует учитывать, что действие кислоты ацетилсалициловой зависит от возраста. Так, у молодых людей в малых дозах препарат удлиняет время кровотечения, а в больших дозах не влияет на него.
Синтезирован новый препарат нитроаспирин, отщепляющий в организме окись азота. Как известно, последняя является одним из эндогенных антиагрегантных соединений. Таким образом, угнетение агрегации тромбоцитов нитроаспирином обусловлено двумя механизмами действия — ингибированием циклооксигеназы (что приводит к снижению биосинтеза тромбоксана) и продукцией NO. Отрицательное влияние на слизистую оболочку пищеварительного тракта у нитроаспирина выражено в меньшей степени, чем у кислоты ацетилсалициловой (аспирина). Кроме того, благодаря высвобождению NO препарат оказывает антигипертензивное действие. Нитроаспирин проходит клинические испытания.
Значительный интерес привлекли исследования, направленные на создание веществ, ингибирующих тромбоксансинтетазу, т.е. веществ, избирательно снижающих синтез тромбоксана (см. рис. 19.1). Такие средства теоретически должны более направленно и эффективно подавлять агрегацию тромбоцитов. Принципиально эта задача была решена: синтезировали производное имидазола, названное дазоксибеном, которое избирательно блокирует тромбоксансинтетазу. Однако ожидания не оправдались, так как монотерапия дазоксибеном оказалась малоэффективной. Связано это, очевидно, с накоплением на фоне его действия проагрегирующих веществ (циклические эндопероксиды), образующихся в циклооксигеназном пути превращения арахидоновой кислоты, которые стимулируют тромбоксановые рецепторы. В практической медицине дазоксибен применяют в сочетании с кислотой ацетилсалициловой. Более перспективны блокаторы тромбоксановых рецепторов тромбоцитов и особенно препараты, сочетающие такое действие с ингибированием тромбоксансинтетазы (ридогрел), однако необходимо более тщательное их изучение.
Приведенные выше препараты снижают агрегацию тромбоцитов за счет угнетения тромбоксановой системы. Вторая возможность заключается в активировании простациклиновой системы. Это можно осуществить путем влияния на соответствующие рецепторы либо за счет повышения активности простациклинсинтетазы.
Принцип антиагрегантного действия простациклина рассмотрен выше. Кроме того, препарат вызывает вазодилатацию и снижает артериальное давление. С учетом малой устойчивости (t1/2 = 3 мин при 37 °С) его пробовали вводить больным в виде длительной (многочасовой) внутриартериальной инфузии при сосудистых заболеваниях нижних конечностей. Простациклин вызывал стойкое (в течение 3 дней) улучшение кровообращения мышц и других тканей, устранял ишемические боли и способствовал заживлению трофических язв. Этот эффект связан с локальным угнетением агрегации тромбоцитов и расширением сосудов. Препарат простациклина получил название эпопростенол.
Синтезирован химически более стойкий аналог простациклина карбациклин. Однако в биологической среде он также оказался нестойким. Карбациклин при внутривенной инфузии снижает агрегацию тромбоцитов. В эксперименте было показано, что эффект сохраняется на время инфузии и не более 10 мин после ее прекращения. Оба вещества в связи с кратковременностью действия малоудобны для практического применения. Желательно создание длительно действующих препаратов, эффективных при разных путях введения. Однако эпопростенол нашел свою область применения: его рекомендуют использовать при проведении гемодиализа (вместо гепарина), так как он уменьшает адгезию тромбоцитов на диализной мембране и не вызывает кровотечений. Препарат применяют также при гемосорбции и экстракорпоральном кровообращении. Кроме того, его используют при легочной гипертензии (сосудорасширяющее + антиагрегантное действие).
Идея создания антиагрегантов, избирательно активирующих синтез эндогенного простациклина, представляет несомненный интерес. Простациклинсинтетаза, обеспечивающая этот процесс, содержится в эндотелиальных клетках и отсутствует в тромбоцитах и может быть «мишенью» для действия фармакологических веществ. Однако препараты такого рода пока не получены.
В последние годы большое внимание привлекли вещества, действующие на гликопротеиновые рецепторы (GP IIb/IIIa) тромбоцитов (рис. 19.2). Эти рецепторы играют важнейшую роль в агрегации тромбоцитов. Препараты, которые влияют на их активность, подразделяются на 2 группы. Первая — это конкурентные или неконкурентные блокаторы гликопротеиновых рецепторов (абциксимаб, тирофибан и др.). Вторая группа представлена препаратами, которые препятствуют активирующему действию АДФ на тромбоциты и экспрессии их гликопротеиновых рецепторов (тиклопидин, клопидогрел). В обоих случаях не происходит или уменьшается связывание с гликопротеиновыми рецепторами фибриногена и ряда других факторов, что и лежит в основе антиагрегантного действия указанных веществ.
Блокаторы гликопротеиновых рецепторов по химической структуре относятся к следующим группам:
1. Моноклоналъные антитела — абциксимаб.
2. Синтетические пептиды — эптифибатид.
3. Синтетические непептидные соединения — тирофибан
1.. 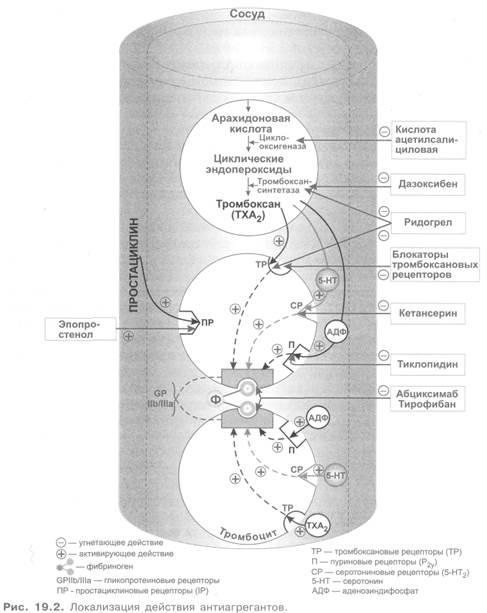
Первым препаратом этой группы, внедренным в медицинскую практику, был абциксимаб (реопро) — неконкурентный блокатор гликопротеиновых рецепторов (IIb/IIIa) тромбоцитов: он препятствует связыванию с ними фибриногена и ряда других соединений. Благодаря этому препарат уменьшает агрегацию тромбоцитов и последующее образование тромбов. Максимальный антиагрегантный эффект наблюдается при связывании не менее 80% гликопротеиновых рецепторов. Препарат обладает также антикоагулянтной активностью.
Абциксимаб является фрагментом специальных моноклональных антител.
Вводят его внутривенно одномоментно или путем инфузии. Связывание с рецепторами происходит быстро (через 5-30 мин). Максимальный эффект развивается примерно через 2 ч. После прекращения введения препарата выраженный эффект продолжается до 1 сут, а остаточные явления блокады гликопротеиновых рецепторов могут сохраняться более 10 дней.
Используют при хирургических вмешательствах на коронарных сосудах при стенокардии, инфаркте миокарда. Нередко комбинируют с гепаринами, а также с фибринолитиками.
Из побочных эффектов наиболее часто отмечается повышенная кровоточивость разной локализации. Возможны аллергические реакции, тромбоцитопения, гипотензия, брадикардия, диспепсия и др.
Дальнейшие поиски антагонистов гликопротеиновых рецепторов были направлены на создание препаратов, получаемых путем химического синтеза. Сейчас известен ряд таких антиагрегантов для внутривенного и энтерального введения. Одним из них является циклический пептид эптифибатид (интегрилин). Он специфично связывается с гликопротеиновыми рецепторами IIb/IIa, препятствуя взаимодействию с ними фибриногена. Вводится внутривенно. Действует быстрее и менее длительно, чем абциксимаб. После прекращения инфузии эффект проходит через 2-8 ч; t1/2 ~ 1,5-2,5 ч. Около 25% вещества связывается с белками плазмы крови. Частично метаболизируется в печени. 40-50% выделяется почками, в основном в неизмененном виде.
К группе конкурентных блокаторов гликопротеиновых рецепторов относится также непептидное соединение тирофибан (аграстат). Механизм снижения агрегации тромбоцитов и показания к применению аналогичны таковым для абциксимаба.
Препарат вводят внутривенно. Действует он менее продолжительно, чем абциксимаб. После прекращения инфузии агрегация тромбоцитов восстанавливается через 4-8 ч. Метаболизируется в небольшой степени, t1/2 = примерно 2 ч. Выделяется преимущественно в неизмененном виде почками (65%) и кишечником (25%).
Синтетические вещества также могут вызывать кровоточивость, тромбоцитопению, аллергические реакции.
Вторая группа веществ (тиклопидин, клопидогрел) действует по иному принципу. Непосредственно на гликопротеиновые рецепторы они не влияют. Механизм их антиагрегантного эффекта заключается в том, что они препятствуют стимулирующему действию АДФ на пуриновые рецепторы (P2Y) тромбоцитов. При этом тромбоциты и гликопротеиновые рецепторы не активируются, что препятствует взаимодействию последних с фибриногеном.
Тиклопидин (тиклид) обладает выраженной антиагрегантной активностью. Эффективен при энтеральном введении. Действие развивается постепенно и достигает максимума через 3-5 дней. Применяют при нестабильной стенокардии для профилактики инфаркта миокарда, уменьшения частоты тромботических осложнений после операций на сердце и сосудах и др. Побочные эффекты наблюдаются довольно часто. К ним относятся диспепсические явления, кожная сыпь, повышение в крови уровня атерогенных липопротеинов. Иногда возникают лейкопения, агранулоцитоз и панцитопения, поэтому необходим систематический контроль крови. При первых признаках нарушения лейкопоэза препарат следует отменить. Тиклопидин обычно назначают при непереносимости кислоты ацетилсалициловой.
К препаратам группы тиклопидина относится также клопидогрел (плавике). Является пролекарством. В печени из него образуется активный метаболит, который и обеспечивает антиагрегантный эффект. Он избирательно и необратимо блокирует рецепторы, с которыми взаимодействует АДФ, и аналогично тиклопидину устраняет активацию гликопротеиновых рецепторов GP IIb/IIIa. В результате нарушается агрегация тромбоцитов.
Препарат вводят внутрь один раз в сутки. Всасывается быстро, но не полностью (около 50%). Максимальная концентрация в крови накапливается примерно через 1 ч. Большая часть вещества и метаболитов связывается с белками плазмы крови. Выделяются они почками и кишечником. t1/2 метаболита ~ 8 ч. При ежедневном введении препарата максимальный антиагрегантный эффект (угнетение на 40-60%) развивается через 3-7 дней.
Переносится препарат относительно хорошо. По сравнению с тиклопидином реже возникают побочные эффекты со стороны кожных покровов (различные сыпи), желудочно-кишечного тракта (кровотечения), состава периферической крови (нейтропения). Реже, чем кислота ацетилсалициловая, вызывает желудочно-кишечные кровотечения и изъязвление слизистой оболочки, однако чаще отмечаются диарея и кожные высыпания.
Группа препаратов разного типа действия включает дипиридамол и антуран.
Дипиридамол (курантил) известен в качестве коронарорасширяющего средства (см. главу 14.3). Вместе с тем он обладает некоторой антиагрегантной активностью. Механизм его действия недостаточно изучен. Известно, что он угнетает фосфодиэстеразу и значительно повышает содержание в тромбоцитах цАМФ. Кроме того, он потенцирует действие аденозина, который тормозит агрегацию тромбоцитов и обладает сосудорасширяющим эффектом. Последнее связано с тем, что дипиридамол угнетает захват и метаболизм аденозина эритроцитами и эндотелиальными клетками. Кроме того, он потенцирует действие простациклина. Из побочных эффектов чаще всего возникают головная боль, диспепсические нарушения, кожная сыпь. Обычно дипиридамол применяют в сочетании с антикоагулянтами непрямого действия или с кислотой ацетилсалициловой.
Препарат антуран (сульфинпиразон) является противоподагрическим средством (см. главу 25). Наряду с этим он подавляет адгезию тромбоцитов и обладает антиагрегантной активностью. Возможно, последнее связано с угнетением циклооксигеназы и(или) действием на мембрану тромбоцитов, а также снижением высвобождения АДФ и серотонина, способствующих агрегации тромбоцитов. Эффективность препарата небольшая.
19.1.2. СРЕДСТВА, ПОНИЖАЮЩИЕ СВЕРТЫВАНИЕ КРОВИ (АНТИКОАГУЛЯНТЫ)
Антикоагулянты могут влиять на разные этапы свертывания крови. По направленности действия они относятся к 2 основным группам.
1. Антикоагулянты прямого действия (вещества, влияющие на факторы свертывания непосредственно в крови)
Гепарин
Фраксипарин
Эноксапарин
Лепирудин
2. Антикоагулянты непрямого действия (вещества, угнетающие синтез факторов свертывания крови — протромбина и др. — в печени)
Неодикумарин
Синкумар
Варфарин
Фенилин
Направленность их действия отражена на схеме 19.1.
К антикоагулянтам прямого действия относится гепарин — естественное противосвертывающее вещество, образующееся в организме тучными клетками. Особенно большие количества гепарина содержатся в печени и легких. По химическому строению является мукополисахаридом. Его молекулярная масса равна 15 000-20 000.
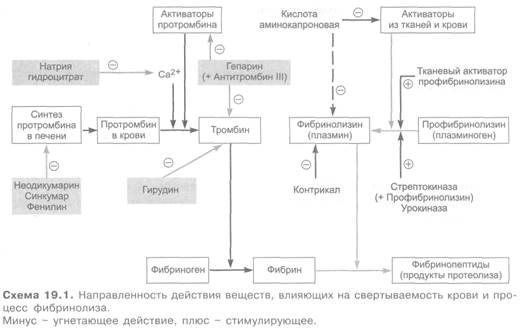
Содержит в своей молекуле остатки серной кислоты, в связи с чем обладает выраженной кислотностью. В растворе несет на себе сильный отрицательный заряд, который способствует взаимодействию гепарина с белками, участвующими в свертывании крови.
Гепарин расценивается как кофактор антитромбина III. В плазме крови он активирует последний (и, очевидно, антитромбин II), ускоряя его противосвертывающее действие. При этом нейтрализуется ряд факторов, активирующих свертывание крови (ХIIа, калликреин, ХIа, Ха, ХIIIа). Нарушается переход протромбина в тромбин. Кроме того, ингибируется тромбин (IIа).
Поскольку гепарин относится к антикоагулянтам прямого действия, он активен не только в условиях целостного организма, но и in vitro. В больших дозах гепарин тормозит агрегацию тромбоцитов.
Гепарин эффективен только при парентеральном введении. Наиболее часто его применяют внутривенно. Действие наступает быстро (при внутривенном введении сразу же после инъекции) и в зависимости от дозы продолжается от 2 до 6 ч. Гепарин инактивируется в печени ферментом гепариназой.
Гепарин выпускают также для наружного применения при флебитах, тромбофлебитах, варикозных язвах конечностей, подкожных гематомах. Один из таких препаратов называется лиотон 1000 (гепарин натрий в виде геля).
Помимо основного противосвертывающего действия, у гепарина отмечена способность понижать содержание в крови липидов. Считается, что это происходит за счет высвобождения из тканей липопротеинлипазы. Последняя гидролизует сорбированные на эндотелии триглицериды липопротеинов с высвобождением свободных жирных кислот, которые поступают в ткани.
Дозируют гепарин в единицах действия — ЕД (1 мг = 130 ЕД). Об эффективности препарата судят по свертываемости крови.
В последние годы создана новая группа антикоагулянтов — низкомолекулярные гепарины — фраксипарин (нандропарин кальций) и др. Они обладают выраженной антиагрегантной и антикоагулянтной активностью. Снижение свертываемости крови под влиянием низкомолекулярных гепаринов связано с тем, что они усиливают угнетающее действие антитромбина III на фактор Xа. Последний необходим для перехода протромбина в тромбин. В отличие от гепарина его низкомолекулярные аналоги не оказывают ингибирующего влияния на тромбин. В связи с тем что эти препараты мало связываются с белками плазмы, их биодоступность выше, чем у гепарина. Выводятся они из организма медленно. Действуют более продолжительно, чем гепарин. Вводят их подкожно 1-2 раза в сутки.
К этой группе препаратов относится также эноксапарин.
Антагонистом гепарина является протамина сульфат (выделен из спермы рыб). Он имеет свойства основания и несет на себе положительный заряд. Взаимодействуя с гепарином, инактивирует его, приводя к образованию нерастворимого комплекса. Вводят протамина сульфат внутривенно; 1 мг его нейтрализует 100 ЕД гепарина. Протамина сульфат является антагонистом и низкомолекулярных гепаринов.
Представляет интерес гирудин, продуцируемый медицинскими пиявками. Он состоит из 65 аминокислот. Создан рекомбинантный вариант, применяемый в качестве активного антикоагулянта прямого действия, — лепирудин (рефлудан). Гирудин инактивирует тромбин; эффект его не зависит от антитромбина III. Вводят препарат внутривенно.
К антикоагулянтам прямого действия может быть отнесен и натрия гидроцитрат. Механизм его противосвертывающего действия заключается в связывании ионов кальция (образуется кальция цитрат), необходимых для превращения протромбина в тромбин. Используется натрия гидроцитрат (4-5%) для стабилизации крови при консервации.
Антикоагулянты непрямого действия включают 2 химические группы веществ:
а) производные 4-оксикумарина — неодикумарин, синкумар, варфарин;
б) производное индандиона — фенилин.
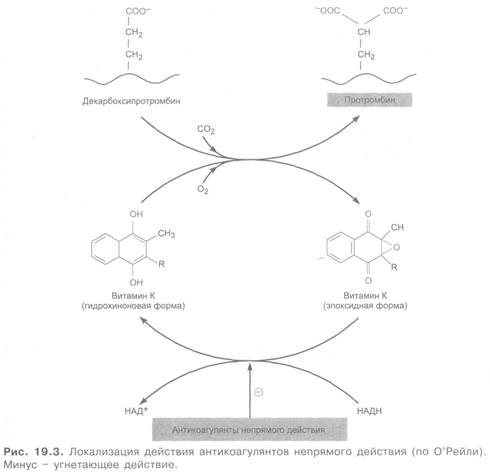
Производные 4-оксикумарина и индандиона условно обозначают антагонистами витамина К1 Принцип их действия заключается в том, что они ингибируют редуктазу эпоксида витамина К и препятствуют восстановлению К1-эпоксида в активную форму витамина К, что блокирует синтез факторов II, VII, IX, X (см. рис. 19.3). Таким образом, они угнетают в печени зависимый от витамина К синтез протромбина, а также проконвертина и ряда других факторов (содержание этих факторов в крови понижается). В отличие от гепарина антикоагулянты непрямого действия эффективны только в условиях целостного организма; in vitro они не влияют на свертываемость крови. Большим преимуществом данной группы антикоагулянтов является их активность при энтеральном применении (табл. 19.1). Все препараты характеризуются значительным латентным периодом и постепенным нарастанием эффекта. Так, максимальное снижение свертываемости крови при их назначении развивается через 1-2 дня и позже, общая продолжительность действия до 2-4 дней. Все эти вещества кумулируют.
Эффективность непрямых антикоагулянтов контролируется по протромбиновому индексу (не должен быть меньше 40-50%). Кроме того, проводятся анализы мочи; появление гематурии является одним из признаков передозировки препаратов.
Побочные эффекты 4-оксикумаринов и производных индандиона сходны. Чаще это кровотечения, кровоизлияния, диспепсические расстройства, угнетение функции печени, аллергические реакции. Антагонистом антикоагулянтов непрямого действия является витамин К1.
| Таблица 19.1Сравнительная характеристика антикоагулянтов прямого и непрямого действия | |||||||
| Препараты | Локализация действия | Механизм действия | Путь введения | Скорость развития эффекта | Продолжительность действия | Длительность применения | Антагонисты |
| Антикоагулянты прямого действия (гепарины) | Кровь | Нарушение превращения протромбина в тромбин в крови 1 | Парентеральный | Быстрая (секунды2, минуты) | Часы | Часы, дни | Протамина сульфат |
| Антикоагулянты непрямого действия (неодикумарин, фенилин, варфарин и др.) | Печень | Нарушение биосинтеза факторов свертывания (в частности, протромбина) в печени | Энтеральный | Медленная (часы) | Дни | Недели | Фитоменадион (витамин K1) |
| 1 Естественный гепарин приводит также к инактивации тромбина. 2 При внутривенном введении. |
Один из наиболее широко применяемых антикоагулянтов непрямого действия — варфарин. Вводится в основном внутрь, хотя имеются препараты и для внутривенного введения.
Хорошо всасывается из пищеварительного тракта. Биодоступность около 100%. Для достижения максимального эффекта требуется около 4 сут. До 97% препарата связывается с белками плазмы крови. Большая часть метаболизируется в печени. Антикоагулянтной активностью метаболиты практически не обладают.
Выводятся варфарин и метаболиты преимущественно почками (~ 92%). Восстановление свертываемости крови после прекращения введения препарата происходит примерно через 4 дня.
Серьезный побочный эффект — кровотечения, возникающие на фоне имеющейся патологии либо при передозировке препарата. Локализация кровотечений весьма разнообразна (желудочно-кишечный тракт, мочеполовая система, ЦНС и др.). Возможны нарушения функции печени, диспепсические расстройства, лейкопения, аллергические реакции, редко некроз кожи и др. Следует также иметь в виду, что варфарин проходит через плаценту и обладает тератогенностью.
Применяют антикоагулянты для профилактики и лечения тромбозов и эмболии (при тромбофлебите, тромбоэмболии, инфаркте миокарда, стенокардии, ревматических пороках сердца). Если нужно быстро понизить свертываемость крови, вводят гепарин. Для более длительного лечения целесообразно назначать антикоагулянты непрямого действия. Нередко сначала вводят гепарин и одновременно дают антикоагулянты непрямого действия. Учитывая, что у последних значительный латентный период, первые 2-4 дня продолжают вводить гепарин, затем его инъекции прекращают и дальнейшее лечение проводят только с помощью антикоагулянтов непрямого действия.
Противосвертывающие вещества противопоказаны при гематурии, язвенной болезни желудка и двенадцатиперстной кишки, язвенном колите, мочекаменной болезни с тенденцией к гематурии, при беременности. Антикоагулянты непрямого действия следует назначать с осторожностью при патологии печени.
19.1.3. ФИБРИНОЛИТИЧЕСКИЕ СРЕДСТВА (ТРОМБОЛИТИЧЕСКИЕ СРЕДСТВА)
Большой практический интерес представляют фибринолитические средства, способные растворять уже образовавшиеся тромбы. Принцип их действия заключается в том, что они активируют физиологическую систему фибринолиза. Применяются обычно для растворения тромбов в коронарных сосудах при инфаркте миокарда, эмболии легочной артерии, тромбозе глубоких вен, остро возникающих тромбах в артериях разной локализации.
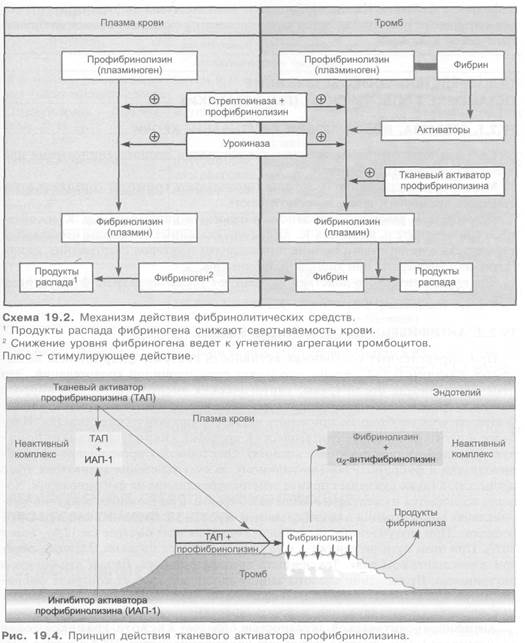
Одним из наиболее широко применяемых фибринолитических средств является соединение белковой структуры стрептокиназа (стрептаза, стрептолиаза). Ее продуцируют β-гемолитические стрептококки группы С. Сама стрептокиназа протеолитической активностью не обладает. Она взаимодействует с профибринолизином; образующийся комплекс приобретает протеолитическую активность и стимулирует переход профибринолизина (плазминогена) в фибринолизин (плазмин) как в тромбе, так и в плазме крови (см. схему 19.1). Фибринолизин, будучи протеолитическим ферментом, растворяет фибрин. Следовательно, стрептокиназа является фибринолитиком непрямого действия, t1/2 = 80 мин, однако эффект сохраняется несколько часов.
Стрептокиназа эффективна при свежих тромбах (примерно до 3 сут). Чем раньше начинать лечение, тем благоприятнее результат. Так, при остром инфаркте миокарда, вызванном тромбозом коронарных артерий, лучший результат дает применение препарата в первые 1-3 ч. Венозные тромбы лизируются лучше, чем артериальные. Особенно хорошо рассасываются тромбы, содержащие большие количества профибринолизина.
Дозируют стрептокиназу в единицах действия (ЕД), вводят обычно внутривенно (капельно). Побочные эффекты: кровотечения, гипотензия, пирогенная и аллергические реакции.
С учетом принципа действия стрептокиназы был создан препарат анистреплаза (эминаза) — нековалентный комплекс стрептокиназы с модифицированным профибринолизином (лизин-профибринолизином). Является пролекарством; в организме происходит его деацетилирование, что сопровождается активацией содержащегося в препарате профибринолизина. При этом стимулируется переход профибринолизина в фибринолизин. t1/2 по фибринолитической активности равно 70-120 мин. Вводят препарат внутривенно; дозируется в ЕД. Может вызывать кровотечения, аллергические реакции и преходящую гипотензию.
Эффективным фибринолитиком прямого действия является урокиназа — фермент, образующийся в почках. По направленности действия аналогична стрептокиназе, но редко вызывает аллергические реакции. Лихорадка возникает у 2-3% больных. t1/2 = 15-20 мин. Раньше урокиназу выделяли из мочи. В настоящее время препарат производят методом генной инженерии или получают из культуры эмбриональных клеток почек человека.
В результате превращения циркулирующего в крови профибринолизина в фибринолизин урокиназа, как и стрептокиназа, может вызвать системный фибринолиз. Последний обусловлен тем, что фибринолизин является неизбирательно действующей протеазой, способной метаболизировать многие белковые соединения, находящиеся в плазме крови. Это приводит к снижению в плазме уровня фибриногена, α2-антиплазмина, ряда факторов свертывания крови (V, VIII). Естественно, что при этом содержание в крови продуктов распада фибрина и фибриногена нарастает.
Системный фибринолиз является причиной кровотечений при применении фибринолитиков.
Назначение фибринолитических средств требует систематического контроля фибринолитической активности крови, а также содержания в ней фибриногена и профибринолизина.
Принципиально новым типом фибринолитиков является тканевый активатор профибринолизина. Соответствующий препарат под названием алтеплаза (актилизе) получают методом генной инженерии. Его действие направлено преимущественно на профибринолизин, связанный с фибрином тромба, и поэтому образование фибринолизина и его действие в основном ограничиваются тромбом (схема 19.2, рис. 19.4). При этом системную активацию профибринолизина препарат вызывает в значительно меньшей степени, чем стрептокиназа и урокиназа. Тканевый активатор профибринолизина обладает высокой терапевтической эффективностью и при своевременном применении способствует реканализации
тромбированных сосудов, t1/2 ~ 5 мин. Вводят препарат внутривенно, дозируют в ЕД. Антигенностью не обладает.
Поиски новых фибринолитических средств продолжаются. Так, получены стафилокиназа (из Staphylococcus aureus) и ее рекомбинантные варианты, обладающие высокой специфичностью к фибрину. Создано рекомбинантное производное естественного тканевого активатора профибринолизина тенектеплаза — более стойкое соединение (t1/2 циркуляции в крови ~ 20 мин), а также более специфичное к фибрину. Из яда особого вида змеи выделена алфимепраза, которая в отличие от всех приведенных выше препаратов оказывает прямое фибринолитическое действие.
19.2. СРЕДСТВА, СПОСОБСТВУЮЩИЕ ОСТАНОВКЕ КРОВОТЕЧЕНИЙ (ГЕМОСТАТИКИ)
19.2.1. СРЕДСТВА, ПОВЫШАЮЩИЕ СВЕРТЫВАНИЕ КРОВИ
Средства этой группы применяют для остановки кровотечений местно или путем резорбтивного действия.
Местно для остановки кровотечений используют тромбин (препарат естественного тромбина), губки гемостатические.
К препаратам резорбтивного действия относятся витамины К1, К3 и синтетический заменитель витамина К3 викасол. Указанные витамины необходимы для синтеза в печени протромбина и ряда других факторов свертывания крови. Назначают препараты при гипопротромбинемии.
Для гемостатического действия используют также желатин, фибриноген и др.
19.2.2. АНТИФИБРИНОЛИТИЧЕСКИЕ СРЕДСТВА
При определенных состояниях активность системы фибринолиза повышается в значительной степени, что может стать причиной кровотечений. Это отмечается иногда после травм, хирургических вмешательств, при циррозе печени, передозировке фибринолитических веществ, маточных кровотечениях. В этих случаях необходимо применять антифибринолитические средства. Наиболее широко используют синтетический препарат кислоту аминокапроновую (эпсилон-аминокапроновая кислота). Она тормозит превращение профибринолизина в фибринолизин (по-видимому, за счет угнетения активатора этого процесса), а также оказывает прямое угнетающее влияние на фибринолизин. Хорошо всасывается из желудочно-кишечного тракта. При этом пути введения максимальная концентрация в крови создается через 2-3 ч. За сутки выделяется 60% вещества. При внутривенном введении элиминация идет быстрее (за 12 ч — более 80%). При этом пути введения t1/2 ~ 77 мин. Выводится почками, главным образом в неизмененном виде. Токсичность препарата низкая. Вводят его внутрь и внутривенно. Применение кислоты аминокапроновой требует контроля фибринолитической активности крови и содержания фибриногена. Возможны и побочные эффекты (головокружение, тошнота, диарея).
Антифибринолитической активностью обладает кислота транексамовая (циклокапрон). Она угнетает активацию профибринолизина. Эффективнее кислоты аминокапроновой и действует более продолжительно. Вводят энтерально и внутривенно. При введении внутрь биодоступность соответствует 30-50%. Незначительно связывается с белками плазмы (около 3%). При внутривенном введении t1/2 ~ 2 ч. Выводится почками.
Аналогичными с кислотой аминокапроновой механизмом действия и свойствами обладает препарат амбен (памба).
К средствам, угнетающим фибринолиз, относится также контрикал (см. главу 15; 15.7). Он ингибирует непосредственно фибринолизин, как и ряд других протеолитических ферментов (трипсин, химотрипсин, калликреин).
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Антиагрегантные средства | ||
| Кислота ацетилсалициловая — Acidum acetylsalicylicum | Внутрь 0,25 г | Таблетки по 0,75; 0,1; 0,25; 0,325 и 0,5 г |
| Дипиридамол — Dipyridamole | Внутрь 0,025-0,05 г | Таблетки (драже) по 0,025 и 0,075 г |
| Антикоагулянты | ||
| Гепарин — Heparinum | Внутривенно, внутримышечно и подкожно 5000-20 000 ЕД | Флаконы по 5 мл (1 мл — 5000; 10 000 и 20 000 ЕД) |
| Неодикумарин — Neodicumarinum | Внутрь 0,05-0,1 г | Таблетки по 0,05 и 0,1 г |
| Синкумар — Syncumar | Внутрь 0,001-0,006 г | Таблетки по 0,002 и 0,004 г |
| Варфарин — Warfarin | Внутрь 0,001-0,01 г | Таблетки по 0,001 и 0,01 г |
| Фенилин — Phenylinum | Внутрь 0,03 г | Порошок; таблетки по 0,03 г |
| Фибринолитические средства | ||
| Стрептокиназа — Streptokinase | Внутривенно (капельно) 250 000-500 000 ЕД | Ампулы по 250 000 и 500 000 ЕД (растворяют перед употреблением) |
| Средства, способствующие свертыванию крови | ||
| Тромбин — Thrombinum | Растворы используют местно | Ампулы и флаконы, содержащие не менее 125 ЕД препарата (растворяют перед употреблением) |
| Антифибринолитические средства | ||
| Кислота аминокапроновая — Acidum aminocapronicum | Внутрь 2-3 г; внутривенно 100 мл 5% раствора (капельно) | Порошок; флаконы по 100 мл 5% раствора |
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, РЕГУЛИРУЮЩИЕ ПРОЦЕССЫ ОБМЕНА ВЕЩЕСТВ (главы 20-25)
Глава 20 ГОРМОНАЛЬНЫЕ ПРЕПАРАТЫ
Гормоны — это биологически активные вещества, вырабатываемые эндокринными железами и специальными группами клеток в различных тканях. Они играют важнейшую роль в гуморальной регуляции разнообразных функций организма. Кроме того, отдельные гормоны являются нейромодуляторами.
Значение гормонов особенно наглядно проявляется при гипофункции той или иной эндокринной железы. Например, при недостаточности островкового аппарата поджелудочной железы развивается сахарный диабет, при недостаточности паращитовидных желез — гипокальциемия, сопровождающаяся судорогами, при недостаточности антидиуретического гормона задней доли гипофиза — несахарный диабет. Вместе с тем известны заболевания, связанные с повышенной продукцией гормонов. Так, при гиперфункции щитовидной железы развивается гипертиреоз (базедова болезнь), при образовании избыточных количеств соматотропного гормона передней доли гипофиза — гигантизм, акромегалия.
При недостаточности желез внутренней секреции обычно назначают гормональные препараты. В данном случае требуется так называемая заместительная терапия, при которой длительность применения этих препаратов определяется продолжительностью гипофункции соответствующей железы. Кроме того, используют средства, стимулирующие выработку гормонов.
Получают гормональные препараты синтетическим путем, а также из органов и мочи животных (в последнем случае активность ряда препаратов определяется путем биологической Стандартизации и выражается в единицах действия — ЕД). В настоящее время синтезировано значительное число аналогов и производных естественных гормонов и их синтетических заменителей, отличающихся по строению от естественных гормонов.
Получены и антагонисты ряда гормонов, блокирующие действие последних на уровне соответствующих рецепторов (например, антагонисты половых гормонов).
По химическому строению гормональные препараты относятся к следующим группам:
1) вещества белкового и пептидного строения — препараты гормонов гипоталамуса, гипофиза, паращитовидной и поджелудочной желез, кальцитонин;
2) производные аминокислот — препараты гормонов щитовидной железы, препараты гормонов эпифиза;
3) стероидные соединения — препараты гормонов коры надпочечников и половых желез.
При гиперфункции эндокринных желез используют антагонисты гормонов, блокирующие соответствующие рецепторы или ингибирующие синтез гормонов.
Первичное действие гормонов локализуется на уровне цитоплазматических мембран или внутриклеточно. Одни гормоны (из группы белков и пептидов) взаимодействуют со специфическими рецепторами, расположенными на наружной поверхности клеточных мембран. Многие из этих рецепторов связаны с аденилатциклазой, изменение активности которой в значительной степени определяет содержание внутри клетки цАМФ. Чаще всего гормоны стимулируют аденилатциклазу и повышают содержание цАМФ. Содержание цАМФ можно повысить также за счет угнетения фосфодиэстеразы. Однако из гормонов так действует лишь трийодтиронин, да и то в очень высоких концентрациях. В свою очередь цАМФ активирует протеинкиназы, что влияет на течение различных интрацеллюлярных процессов (рис. 20.1). Таким путем действуют кортикотропин, тиротропин, гонадотропные гормоны гипофиза, меланоцитстимулирующие гормоны, паратгормон, кальцитонин, глюкагон.
Гормоны могут влиять на захват, высвобождение и внутриклеточное распределение ионов кальция, который также может выступать в качестве «посредника»
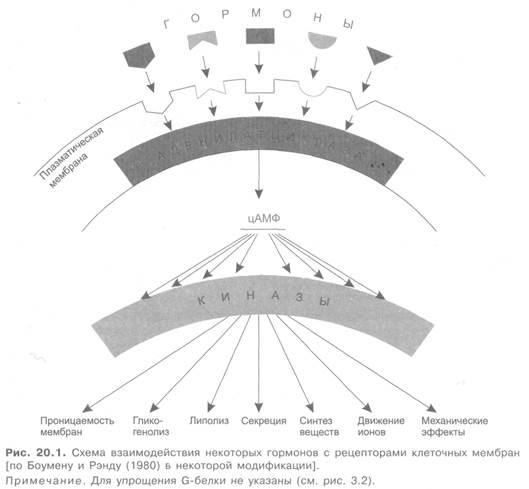
между рецепторами мембран и внутриклеточными процессами. Кроме того, установлены определенные взаимоотношения между цАМФ и кинетикой ионов кальция.
Некоторые гормоны (белки и пептиды) действуют на мембранные рецепторы, не связанные с аденилатциклазой (гормон роста, лактотропный гормон). Вопрос о «посреднике» в данном случае остается открытым. Отдельные гормоны могут влиять на фосфатидилинозитольный цикл, повышая продукцию инозитолтрифосфата и диацилглицерола (например, гормон гипоталамуса, стимулирующий высвобождение гонадотропных гормонов; вазопрессин).
Влияние гормонов на мембраны клеток может также проявляться в том, что они изменяют их проницаемость для других эндогенных веществ (например, инсулин способствует вхождению глюкозы внутрь клетки).
Ряд гормонов, проникающих через мембрану клеток, действуют внутриклеточно (например, стероиды, гормоны щитовидной железы). Стероиды образуют комплекс с цитоплазматическими рецепторами и затем транспортируются в ядро клетки, где и проявляется их основной эффект (рис. 20.2). В ядре клетки они активируют ДНК, а также иРНК, что приводит к индукции синтеза белка.
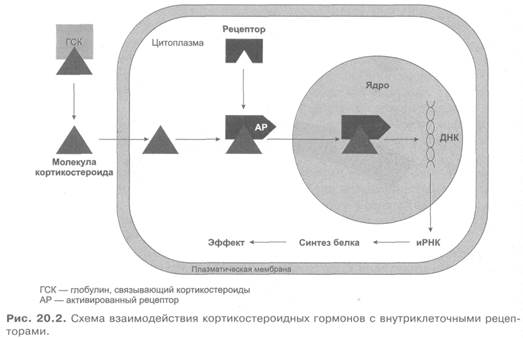
Однако это только возможные принципы действия гормонов, многие стороны этого действия нуждаются в дальнейшем уточнении.
20.1. ПРЕПАРАТЫ ГОРМОНОВ ГИПОТАЛАМУСА И ГИПОФИЗА
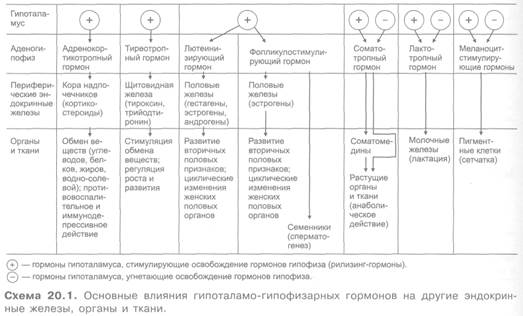
Гипофиз состоит из 3 долей: передней, задней и маловыраженной средней. Передняя и средняя доли содержат железистые клетки и объединяются под названием «аденогипофиз». Передняя доля продуцирует адренокортикотропный, соматотропный, тиреотропный, фолликулостимулирующий, лютеинизирующий и лактотропный гормоны (табл. 20.1). Их образование и освобождение регулируются специальными стимулирующими рилизинг-гормонами и угнетающими гормонами (факторами) гипоталамуса (табл. 20.2). Средняя доля у некоторых млекопитающих секретирует меланоцитстимулирующие гормоны (α, β, γ) и также находится под контролем гипоталамуса.
| Таблица 20.1Гормоны передней и задней долей гипофиза, их препараты и заменители. | ||
| Доля гипофиза | Гормон | Препараты гормонов гипофиза и их заменители |
| Передняя | Адренокортикотропный гормон (АКТГ; кортикотропин) | Кортикотропин Козинтропин |
| Соматотропный гормон (гормон роста; соматотропин) | Гормон роста (соматотропин) Соматрем | |
| Тиреотропный гормон (тиротропин) | Тиротропин | |
| Лактотропный гормон (пролактин, лактотропин, маммотропин) | Лактин | |
| Гонадотропные гормоны | ||
| Фолликулостимулирующий гормон (фоллитропин) | Гонадотропин менопаузный (менотропины) | |
| Лютеинизирующий гормон (лютропин) | Гонадотропин хорионический (пролан) | |
| Задняя | Окситоцин | Окситоцин |
| Вазопрессин (антидиуретический гормон) | Вазопрессин Десмопрессин Липрессин Фелипрессин | |
| Питуитрин Адиурекрин | } | содержат оба гормона |
| Таблица 20.2Гормоны гипоталамуса, регулирующие высвобождение гормонов гипофиза, и их препараты | ||
| Стимулирующие высвобождение гормонов гипофиза (рилизинг-гормоны)1 | Угнетающие высвобождение гормонов гипофиза (ингибирующие гормоны) | Препараты гормонов и их синтетических аналогов |
| Гормон, стимулирующий высвобождение кортикотропина (кортиколиберин) | ||
| Гормон, стимулирующий высвобождение тиротропина (тиролиберин) | Рифатироин (+) | |
| Гормон, стимулирующий высвобождение гонадотропных гормонов — фолликулостимулирующего и лютеинизирующего (гонадорелин) | Гонадорелин (+/–)2 Леупролид (+/–)2 Нафарелин (+/–)2 | |
| Гормон, стимулирующий высвобождение соматотропина (соматолиберин) | Гормон, угнетающий высвобождение соматотропина (соматостатин) | Соматостатин (–) Октреотид (–) |
| Гормон, стимулирующий высвобождение пролактина (пролактолиберин) | Гормон, угнетающий высвобождение пролактина (пролактостатин) | |
| Гормон, стимулирующий высвобождение меланоцитстимулирующих гормонов (меланолиберин) | Гормон, угнетающий высвобождение меланоцитстимулирующих гормонов (меланостатин) | |
| 1 Очевидно, изменяется и биосинтез гормонов. 2 В зависимости от динамики концентраций в плазме крови может оказывать стимулирующее или угнетающее действие. Примечание. Плюс — стимулирующее действие, минус — угнетающее. |
Основные влияния гипоталамо-гипофизарных гормонов на другие эндокринные железы, органы и ткани представлены на схеме 20.1.
Синтез и выделение гормонов гипоталамуса и аденогипофиза регулируются по принципу обратной связи. Проявляется это в том, что активность центров гипоталамуса и гипофиза зависит от концентрации циркулирующих в крови гормонов. Снижение содержания гормонов в крови стимулирует гипоталамо-гипофизарную систему, а повышение сопровождается угнетающим эффектом.
Задняя доля, называемая нейрогипофизом, состоит из нервных окончаний и клеток, напоминающих глию (питуициты). В ней содержатся два гормона: окситоцин и вазопрессин (антидиуретический гормон). Эти гормоны образуются в нейросекреторных клетках, берущих начало в супраоптическом и паравентрикулярном ядрах гипоталамуса. Их аксоны приходят по ножке гипофиза к его задней доле. Окончания этих аксонов вступают в тесный контакт с капиллярами нейрогипофиза, куда и высвобождаются окситоцин и вазопрессин (в нейронах оба гормона находятся в виде неактивного комплекса с белками — нейрофизином I и II). Высвобождение обоих гормонов происходит под влиянием нервных импульсов.
Гормоны гипофиза нашли применение в разных областях медицинской практики. В качестве лекарственных средств начинают использовать и некоторые гормоны гипоталамуса, регулирующие секрецию гормонов передней доли гипофиза.
Образующийся в базофильных клетках передней доли гипофиза АКТГ является полипептидом (состоит из 39 аминокислот). Осуществлен его синтез. N-концевая часть АКТГ 1-20 полностью сохраняет свойства целой молекулы гормона. АКТГ взаимодействует в коре надпочечников со специфическими рецепторами на внешней поверхности клеточной мембраны, стимулирует связанную с ними аденилатциклазу и повышает содержание в клетках цАМФ. В итоге это способствует превращению холестерина в кортикостероиды. АКТГ стимулирует продукцию главным образом глюкокортикоидов. В связи с этим физиологическое действие последних и АКТГ аналогично (о глюкокортикоидах см. ниже). Существенным отличием АКТГ является отсутствие при непродолжительном его применении угнетения функции коры надпочечников, что обычно происходит при использовании кортикостероидов. Однако при длительном введении АКТГ возможно «истощение» надпочечников. Препарат АКТГ кортикотропин получают из гипофизов убойного скота. Дозируют в единицах действия (ЕД). В желудочно-кишечном тракте он разрушается. В связи с этим вводят кортикотропин внутримышечно и внутривенно. Продолжительность действия около 6 ч.
Препараты АКТГ назначают редко — с диагностической целью или после длительного применения глюкокортикоидов. Смысл последнего назначения АКТГ заключается в стимуляции клеток коры надпочечников и восстановлении продукции эндогенных кортикостероидов, которая угнетается глюкокортикоидами. Однако следует учитывать, что длительное введение АКТГ в виде препарата кортикотропина подавляет высвобождение гипоталамического гормона, стимулирующего в естественных условиях биосинтез и выделение АКТГ.
Возможны побочные эффекты: отеки, повышение артериального давления, катаболическое действие (преобладает распад белка), бессонница, задержка процессов регенерации и др.
Следует также иметь в виду, что кортикотропин вызывает образование антител. Поэтому в настоящее время предпочитают пользоваться его синтетическим аналогом тетракозактрином (тетракозактид, синактен-депо, козинтропин; содержит 24 аминокислоты), у которого иммуногенность выражена в небольшой степени.
Date: 2015-07-01; view: 3564; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |