
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Камни мочеиспускательного канала и полости крайней плоти 7 page

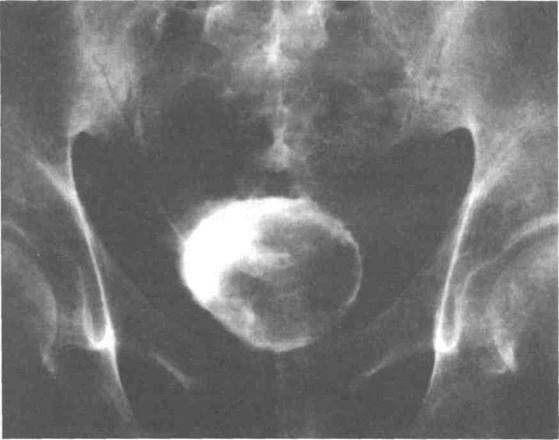
Рисунок21.3. Нисходящая цистограмма при раке мочевого пузыря. Виден дефект наполнения, обусловленный опухолью.
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника
|
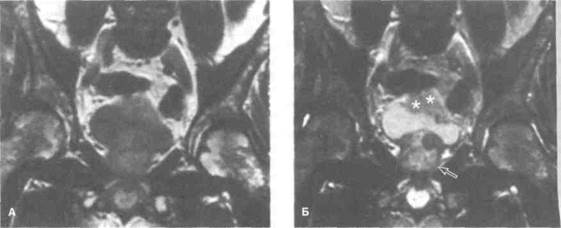
Рисунок 21.4. МРТ при раке мочевого пузыря. А. Т1 -взвешенное изображение. Б. Т2-взвешенное изображение. По сравнениюс Т1 -взвешенным изображением четче видна инвазия, так как лучше различаются опухоль (отмечена звездочками) и стенка мочевого пузыря. Стенка мочевого пузыря выглядит как тонкая полоса с высокой интенсивностью сигнала. При инвазии она прерывается. Неоднородность структуры предстательной железы (показана стрелкой) обусловлена аденомой.
ния у больных с клаустрофобией, имплантированными электрокардиостимуляторами, гемостатическими клипсами в полости черепа и другими металлическими им-плантатами. Следует помнить, что ни КТ, ни МРТ не позволяет отличить опухоли Та и Tl, T2b и ТЗа. Главное достоинство обоих методов — возможность точно установить, выходит ли опухоль за пределы мочевого пузыря или ограничивается его стенкой. При выявлении метастазов в лимфоузлы и при КТ, и при МРТ ориентируются на размеры последних. Подозрительными на наличие метастазов считаются лимфоузлы диаметром более 1 см. Метастазы меньшего размера при КТ и МРТ, как правило, не визуализируются. При инвазивных опухолях обязательно выполняют рентгенографию грудной клетки и сцинтиграфию костей, так как возможны метастазы в легкие и кости.
Цистоскопия и ТУР опухоли
Цистоскопия и ТУР опухоли требуются для подтверждения диагноза и определения стадии рака мочевого пузыря. Используют как жесткие, так и гибкие цистоскопы. При применении последних процедура менее болезненна. В мочеиспускательный канал вводят местный анестетик. Поверхностные высокодифференци-рованные опухоли выглядят, как правило, как одиночные или множественные папиллярные образования диаметром менее 3 см. Умеренно- и низкодифферен-цированные опухоли обычно крупнее и имеют широкое основание. При раке in situ слизистая может быть гиперемированной, с бархатистой поверхностью. После выявления опухоли или подозрительных участков проводят ректальное или обычное бимануальное исследование под общей анестезией и ТУР или биопсию. Такая тактика позволяет не только поставить диагноз и
определить глубину инвазии, но и излечить больных раком мочевого пузыря ранних стадий.
Больного укладывают в положение лежа на спине, ноги фиксируют в ногодержателях. Сначала берут смыв для цитологического исследования. Затем проводят бимануальное исследование. При этом подтверждают наличие объемного образования, уточняют его локализацию и размеры, а также смещаемость стенки мочевого пузыря, Повторяют цистоскопию, при этом тщательно осматривают всю стенку мочевого пузыря. После этого резекто-скопом удаляют все видимые опухоли. С помощью био-псийных щипцов выполняют биопсию подозрительны) участков. Кровотечение останавливают электрокоагуляцией. Некоторые авторы рекомендуют выполнять множественные биопсии неизмененной слизистой. Друга возражают против этой тактики. По их мнению, повреж дение слизистой способствует имплантации опухолевн клеток, попадающих в полость мочевого пузыря во врем ТУР. Хотя, по данным отдельных авторов, частота дис плазии или рака in situ у больных раком мочевого пузыр достигает 65%, эти изменения вряд ли встречаются чащ чем в 15% случаев. Однако именно у этих больных осе бенно высок риск прогрессирования опухоли.
Прогноз и тактика лечения
Традиционные прогностические факторы
Течение рака мочевого пузыря определяется рецидив: рованием и переходом поверхностных опухолей в инв зивные. Второе особенно опасно, поскольку повыша риск метастазов. Даже поверхностные опухоли мочев го пузыря сопряжены с высоким риском осложнени поскольку требуют регулярного проведения цистоск
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника
 пии, периодических ТУР и нередко внутрипузырной терапии. Последняя не всегда хорошо переносится, имеет специфические осложнения и может быть достаточно дорогой. Тактику лечения определяют после уточнения стадии, степени дифференцировки, размера и числа опухолей, а также риска прогрессирования (табл. 21.2).
пии, периодических ТУР и нередко внутрипузырной терапии. Последняя не всегда хорошо переносится, имеет специфические осложнения и может быть достаточно дорогой. Тактику лечения определяют после уточнения стадии, степени дифференцировки, размера и числа опухолей, а также риска прогрессирования (табл. 21.2).
На момент постановки диагноза примерно 50—70% злокачественных опухолей мочевого пузыря соответствуют индексам Tis—Та. Инвазия собственной пластинки слизистой и мышечной оболочки встречается реже — у 28 и 24% больных соответственно, регионарные или отдаленные метастазы — примерно у 15% больных. Примерно 80% больных с инвазивными и диссеминирован-ными опухолями раньше не лечились по поводу рака мочевого пузыря. На момент выявления примерно у 43% больных опухоли высокодифференцированные, у 25% — умереннодифференцированные и у 32% — низкодиф-ференцированные. Риск прогрессирования и выживаемость зависят от степени дифференцировки и стадии. Если при поверхностных опухолях (pTis—рТ1) 5-летняя выживаемость составляет 81%, то при опухолях рТ2, рТЗ и рТ4 — 53, 39 и 25% соответственно, поскольку чем больше стадия опухоли, тем выше риск метастазирова-ния. Так, на ранних стадиях метастазы в лимфоузлы наблюдаются редко (в 5% случаев), а по мере увеличения стадии их частота возрастает. При опухолях рТЗа она составляет 10-30%, рТЗЬ - 31-35%, рТ4 - 35-64%. При опухолях, ограниченных стенкой мочевого пузыря, прогноз зависит в основном от наличия метастазов в лимфоузлы.
Таблица 21.2. Тактика лечения рака мочевого пузыря
| Опухоль | Лечение |
| Tis | ТУР опухоли и внутрипузырная им |
| мунотерапия БЦЖ | |
| Та (одиночная, неболь- | ТУР опухоли |
| шая, высоко- или уме- | |
| реннодифференцирован | - |
| ная первичная опухоль) | |
| Та (крупная, низкодиф- | ТУР опухоли и внутрипузырная хи- |
| ференцированная или | мио- или иммунотерапия |
| рецидивная опухоль, | |
| мультицентрический | |
| рост) | |
| Т1 | ТУР опухоли и внутрипузырная хи- |
| мио- или иммунотерапия | |
| Т2-4 | Радикальная цистэктомия |
| Неоадъювантная химиотерапия и | |
| радикальная цистэктомия | |
| Радикальная цистэктомия и адъю- | |
| вантная химиотерапия | |
| Химиотерапия, затем одномомент- | |
| ное проведение химио- и лучевой | |
| терапии | |
| Регионарные или отда- | Химиотерапия, затем паллиативна; |
| ленные метастазы | операция или лучевая терапия |
Поверхностные опухоли мочевого пузыря метастази-руютреже инвазивных. Однако это не означает, что они не могут прогрессировать. Разделение поверхностных опухолей по степени дифференцировки и по стадиям вполне оправдано из-за разного риска прогрессирования. Частота прогрессирования опухолей Та не превышает 6%, Т1 —достигает46%. Прогрессируют 10—20% высокодифференцированных опухолей, 19—37% уме-реннодифференцированных и 33—64% низкодиффе-ренцированных. Риск рецидива после лечения зависит от степени дифференцировки опухоли, ее локализации, размеров и течения. Рецидивы чаще всего возникают в течение первых 12 мес после выявления первичной опухоли, хотя проявляться они могут спустя несколько лет. Кроме того, каждый очередной рецидив увеличивает риск последующего. Риск рецидива при поверхностных опухолях особенно высок при опухолях Т1, мультицен-трическом росте (более 4 опухолей), опухолях диаметром более 5 см и низкой степени дифференцировки, а также в тех случаях, когда помимо первичной опухоли имеется рак in situ или тяжелая дисплазия мочевого пузыря.
Молекулярно-генетические маркеры
Традиционные прогностические факторы, в том числе степень дифференцировки и стадия, не всегда могут предсказать поведение опухоли. Дополнительную информацию о прогнозе дают молекулярно-генетические маркеры, которые определяются, как правило, с помощью иммуногистохимических исследований. Некоторые маркеры можно определять в биоптатах, другие — только при исследовании операционного материала после радикальной цистэктомии.
Антигены групп крови — это олигосахариды, связанные с мембранными липидами и белками. Антигены А, В, Н, Lea, Leb, Le" и Ley обнаружены не только на поверхности эритроцитов, но и на эпителиальных клетках, в том числе клетках переходного эпителия мочевых путей. При поверхностных опухолях мочевого пузыря утрата антигенов А, В, Н повышает риск рецидива и инвазив-ной опухоли. Однако при этом нужно знать, присутствуют ли эти антигены на слизистых больного в норме. Если да, то на нормальном эпителии мочевых путей в большом количестве обнаруживаются антигены А, В, Н, Leb и Ley. Между тем у 20% лиц на слизистых и в биологических жидкостях антигены групп крови отсутствуют. Таким образом, говорить об утрате антигенов А, В, Н, Ьеьи Ley опухолевыми клетками можно только у лиц, у которых они имеются в норме. Иммуногистохимиче-ское определение антигена Lex в замороженных или фиксированных формальдегидом препаратах показало, что этот антиген экспрессируют 90% опухолей мочевого пузыря и лишь единичные поверхностные клетки нормального переходного эпителия. Таким образом, определение экспрессии антигена Lex используется не только в диагностике рака мочевого пузыря, но и для оценки прогноза прогрессирования поверхностных опухолей.
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника
Рост опухоли и метастазирование невозможно без образования сосудов — ангиогенеза. Этот процесс стимулируют, в частности, фактор роста фибробластов и фактор роста эндотелия и подавляют тромбоспондин-1 и ангио-статин. Разработаны иммуногистохимические методы количественной оценки ангиогенеза, суть которых заключается в определении плотности микрососудов. Плотность микрососудов — ценный прогностический фактор, уже используемый при ряде злокачественных опухолей, в том числе при раке мочевого пузыря. У больных с инвазивны-ми опухолями, перенесших радикальную цистэктомию, отмечена зависимость между плотностью микрососудов и частотой метастазов в регионарные лимфоузлы, про-грессированием и выживаемостью. Выявлена зависимость между риском рецидива, выживаемостью и экспрессией тромбоспондина-1 при раке мочевого пузыря.
В норме клеточный цикл четко контролируется, в то время как в злокачественных опухолях пролиферация клеток происходит бесконтрольно. Важную роль в регуляции клеточного цикла играют циклины и циклинза-висимые киназы. Они образуют комплексы, которые фосфорилируют ядерные белки, обеспечивающие переход клетки из одного периода клеточного цикла в другой. Одним из таких белков является белок Rb — продукт гена ретинобластомы RB1. Весьма вероятно, что опухолевая трансформация начинается с потери контроля над клеточным циклом. Самый известный моле-кулярно-генетический маркер рака мочевого пузыря — белок р53. Кодирующий его ген ТР53 является геном — супрессором опухолевого роста. Ему принадлежит ключевая роль в регуляции клеточного цикла. Если ДНК повреждена, экспрессия гена ТР53 усиливается и клеточный цикл останавливается для репарации ДНК. При мутациях гена ТР53 синтезируется измененный белок р53 и остановка клеточного цикла не происходит. Т1/2 измененного белка р53 больше, чем нормального, поэтому его легче обнаружить при иммуногистохимиче-ском исследовании. Усиление экспрессии р53 (указывающее на возможные мутации гена ТР53) наблюдается при раке мочевого пузыря поздних стадий и низкодиф-ференцированных опухолях, повышает риск прогрес-сирования и снижает выживаемость. При экспрессии р53 частота прогрессирования опухолей рТ1, рТ2 и рТЗа составляет 62, 56 и 80%, в отсутствие р53 — 7, 12 и 11% соответственно. На основании этих данных недавно было проведено клиническое испытание, в котором адъювантную терапию после радикальной цистэктомии проводили только при опухолях, которые экспрессиро-вали р53. Дополнительную информацию дает исследование экспрессии другого регулятора клеточного цикла белка р21С1Р1, синтез которого, в свою очередь, регулируется белком р53.
Ген ретинобластомы RB1 также является геном — супрессором опухолевого роста. Его экспрессию обнаруживают при ряде злокачественных опухолей, в том числе при переходноклеточном раке мочевого пузыря. Мутации гена RB1, которые выявляют также иммуногисто-
химическими методами, характерны для рака мочевого пузыря поздних стадий и низкодифференцированных опухолей. Наличие мутаций статистически достоверно снижает выживаемость. Присутствие мутаций гена ТР53 или гена RB1 в инвазивных опухолях мочевого пузыря ухудшает прогноз, одновременное наличие мутаций обоих генов делает его еще более неблагоприятным. Среди прочих факторов, которые могут использоваться для оценки прогноза при раке мочевого пузыря, следует отметить пролиферативный индекс и экспрессию некоторых молекул адгезии, например Е-кадгеринов.
Тактика лечения
При поверхностных опухолях мочевого пузыря показана ТУР с последующей внутрипузырной терапией. Если опухоль небольшая и высокодифференцирован-ная, то прогрессирование маловероятно и внутрипу-зырную терапию можно не проводить. Риск прогрессирования высок при опухолях Т1, мультицентрическом росте, крупных или рецидивных опухолях, а также при сопутствующем раке in situ. В таких случаях внутрипу-зырная терапия обязательна. Мнения о тактике лечения опухолей Т1 противоречивы. Некоторые авторы рекомендуют выполнять в этом случае, особенно при низко-дифференцированных опухолях, радикальную цистэктомию. Другие считают, что можно ограничиться ТУР опухоли, поскольку последующая внутрипузырная терапия снижает риск прогрессирования. При рецидивах опухолей Т1 после ТУР и внутрипузырной химиотерапии показано более активное лечение.
При раке мочевого пузыря Т2—ТЗ выполняют резекцию мочевого пузыря или радикальную цистэктомию, проводят лучевую терапию или комбинированное лечение (лучевую терапию или хирургическое лечение в комбинации с химиотерапией). Существует мнение, что при опухолях Т2 можно выполнять ТУР. Однако такой подход нецелесообразен, поскольку в большинстве случаев операцию не удается выполнить радикально. ТУР опухоли и внутрипузырную терапию проводят при дукталь-ном или ацинарном раке in situ предстательной часта мочеиспускательного канала. При переходноклеточном раке предстательной части мочеиспускательного канала и при наличии инвазии показано расширение объема операции. При раке мочевого пузыря Т4Ь проводят системную или реже внутриартериальную регионарную химиотерапию с последующей лучевой терапией или хирургическим лечением. При регионарных или отдаленных метастазах рекомендуется химиотерапия, а затем в зависимости от ее эффективности — лучевая терапия или хирургическое лечение.
Лечение
Внутрипузырная терапия
Поверхностные опухоли мочевого пузыря в большинстве случаев рецидивируют. Опасность состоит в том. что
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника
 рецидивные опухоли бывают менее дифференцированными и могут выявляться на более поздних стадиях. Препараты для иммуно- и химиотерапии можно вводить прямо в мочевой пузырь через катетер, это позволяет избежать побочных эффектов, характерных для системного введения тех же препаратов. Внутрипузыр-ная терапия преследует две цели: устранение остаточных опухолей после нерадикальной ТУР и снижение риска рецидива после радикальной (табл. 21.3). Несмотря на то что внутрипузырная терапия проводится уже давно, сравнивать эффективность разных препаратов трудно, поскольку контролируемых клинических испытаний проведено немного, а в имеющихся исследованиях существенно отличаются показания, дозы препаратов, длительность их воздействия на слизистую и режим лечения. Большинство препаратов применяют 1 раз в неделю в течение 6—8 нед. Риск рецидива можно снизить еще больше с помощью поддерживающей терапии (1 раз в 1—2 мес). Побочные действия, прежде всего симптомы раздражения мочевого пузыря, наблюдаются часто. Системных побочных действий обычно нет, так как слизистой мочевого пузыря противоопухолевые средства почти не всасываются. Риск системных побочных действий повышается при макрогематурии, поэтому внутрипузырную терапию в этом случае лучше не проводить. Эффективность лечения можно повысить, увеличив время воздействия и концентрацию препарата. Для этого перед введением больным рекомендуют не пить, после введения препарата не лежать в одной позе, а поворачиваться и мочиться не ранее чем через 1—2 ч. Кроме того, вместе с раствором в мочевой пузырь не должен попадать воздух. В США для внутрипузырной терапии чаще всего используют митомицин, тиоТЭФ, доксорубицин и БЦЖ. При неэффективности одного препарата для внутрипузырной терапии можно использовать другой.
рецидивные опухоли бывают менее дифференцированными и могут выявляться на более поздних стадиях. Препараты для иммуно- и химиотерапии можно вводить прямо в мочевой пузырь через катетер, это позволяет избежать побочных эффектов, характерных для системного введения тех же препаратов. Внутрипузыр-ная терапия преследует две цели: устранение остаточных опухолей после нерадикальной ТУР и снижение риска рецидива после радикальной (табл. 21.3). Несмотря на то что внутрипузырная терапия проводится уже давно, сравнивать эффективность разных препаратов трудно, поскольку контролируемых клинических испытаний проведено немного, а в имеющихся исследованиях существенно отличаются показания, дозы препаратов, длительность их воздействия на слизистую и режим лечения. Большинство препаратов применяют 1 раз в неделю в течение 6—8 нед. Риск рецидива можно снизить еще больше с помощью поддерживающей терапии (1 раз в 1—2 мес). Побочные действия, прежде всего симптомы раздражения мочевого пузыря, наблюдаются часто. Системных побочных действий обычно нет, так как слизистой мочевого пузыря противоопухолевые средства почти не всасываются. Риск системных побочных действий повышается при макрогематурии, поэтому внутрипузырную терапию в этом случае лучше не проводить. Эффективность лечения можно повысить, увеличив время воздействия и концентрацию препарата. Для этого перед введением больным рекомендуют не пить, после введения препарата не лежать в одной позе, а поворачиваться и мочиться не ранее чем через 1—2 ч. Кроме того, вместе с раствором в мочевой пузырь не должен попадать воздух. В США для внутрипузырной терапии чаще всего используют митомицин, тиоТЭФ, доксорубицин и БЦЖ. При неэффективности одного препарата для внутрипузырной терапии можно использовать другой.
Митомицин — противоопухолевый антибиотик. По механизму действия он относится к алкилирующим средствам, которые блокируют синтез ДНК. Из-за высокого молекулярного веса (329) он почти не всасывается. После внутрипузырной химиотерапии митомицином наступает ремиссия у 39—78% больных с остаточными опухолями, после радикальной ТУР риск рецидива снижается на 2—33%. Побочные действия наблюдаются у 10—43% больных. В основном это учащенное болез-
Таблица 21.3. Внутрипузырная иммуно- и химиотерапия
| Срок проведения | Цель |
| Во время ТУР опухоли | Профилактика имплантации |
| опухолевых клеток | |
| После радикальной ТУР опу- | Профилактика прогрессиро- |
| холи | вания |
| После нерадикальной ТУР | Устранение остаточной опухо- |
| опухоли | ли |
ненное мочеиспускание и императивные позывы. У 6% больных отмечается побочный эффект, присущий только митомицину, — сыпь на ладонях и наружных половых органах. Для ее предупреждения больным рекомендуют, помочившись после введения препарата, сразу вымыть руки и наружные половые органы. ТиоТЭФ — это алкилирующее противоопухолевое средство с молекулярным весом 189. Его применяют в разных дозах, но вполне достаточно 30 мг 1 раз в неделю. Полная ремиссия наблюдается у 55% больных. В большинстве контролируемых клинических испытаний доказано, что тиоТЭФ статистически достоверно снижает частоту рецидивов рака мочевого пузыря по сравнению с плацебо. Цистит после введения тиоТЭФ развивается довольно часто, но протекает легко и лечения не требует. У 9% больных в результате всасывания препарата отмечаются лейкопения и тромбоцитопения, поэтому перед каждым введением обязательно проводят общий анализ крови.
Доксорубицин имеет высокий молекулярный вес (580). Это противоопухолевый антибиотик, который, встраиваясь между нитями ДНК, нарушает транскрипцию. Полная ремиссия после его применения наблюдается в среднем у 38% больных, частота рецидивов снижается на 10—23%. Цистит развивается довольно часто, системные побочные эффекты редки. БЦЖ — это живая вакцина из аттенуированного штамма Mycobacterium bovis. Для приготовления БЦЖ используют разные вакцинные штаммы с различной пато-генностью, жизнеспособностью и иммуногенностью. Механизм противоопухолевого действия БЦЖ не известен, по-видимому, оно связано с активацией противоопухолевого иммунитета. После внутрипузырного введения на слизистой, как правило, образуются бугорки и язвы. В бугорках, представляющих собой гранулемы, находят активированные Т-хелперы, а в моче появляется ИЛ-2. БЦЖ очень эффективна при остаточных опухолях и для профилактики рецидивов рака мочевого пузыря, считается самым эффективным препаратом для внутрипузырной терапии рака in situ. При остаточных опухолях полная ремиссия наблюдается у 36—71% больных. Частота рецидивов после ТУР опухоли в комбинации с внутрипузырной терапией БЦЖ составляет 11—27%, а после ТУР — 70%. Существуют разные схемы применения БЦЖ. Сочетание внутрипузырного введения с нанесением БЦЖ на кожу не повышает эффективность лечения. Результаты последних исследований указывают на эффективность поддерживающей внутрипузырной терапии БЦЖ. Побочные действия наблюдаются довольно часто и в большинстве случаев протекают легко. Обычно это симптомы раздражения мочевого пузыря. Геморрагический цистит развивается у 7% больных, туберкулез — у 2%. При появлении общих симптомов, умеренно выраженных или тяжелых местных побочных действиях назначают изониазид, 300 мг/сут внутрь, и снижают дозу БЦЖ. Изониазид назначают до исчезновения симптомов и затем вновь начинают лечение за су-
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника
 тки до следующего введения БЦЖ. При выраженных общих симптомах лечение прекращают. При длительной лихорадке выше 39,4°С, туберкулезе предстательной железы или других проявлениях туберкулеза назначают изониазид, 600 мг/сут внутрь, и рифампицин, 600 мг/сут внутрь. При сепсисе (высокая лихорадка с ознобами, оглушенность, артериальная гипотония, дыхательная недостаточность, желтуха) дополнительно назначают этамбутол, 1200 мг/сут внутрь. Эффективность лечения увеличивается при добавлении к схеме цикло-серина, 500 мг внутрь 2 раза в сутки, или преднизолона, 40 мг/сут внутрь.
тки до следующего введения БЦЖ. При выраженных общих симптомах лечение прекращают. При длительной лихорадке выше 39,4°С, туберкулезе предстательной железы или других проявлениях туберкулеза назначают изониазид, 600 мг/сут внутрь, и рифампицин, 600 мг/сут внутрь. При сепсисе (высокая лихорадка с ознобами, оглушенность, артериальная гипотония, дыхательная недостаточность, желтуха) дополнительно назначают этамбутол, 1200 мг/сут внутрь. Эффективность лечения увеличивается при добавлении к схеме цикло-серина, 500 мг внутрь 2 раза в сутки, или преднизолона, 40 мг/сут внутрь.
Новые режимы внутрипузырной терапии. Высокодиффе-ренцированный рак мочевого пузыря рецидивирует чаще, чем высокодифференцированный рак других органов, например носоглотки или толстой кишки. Риск рецидива при поверхностных опухолях мочевого пузыря зависит от стадии, степени дифференцировки, числа опухолей, сопутствующей дисплазии и плоидности опухолевых клеток. Рецидив рака мочевого пузыря может быть обусловлен ростом остаточной опухоли, новой опухолью или имплантацией опухолевых клеток, попавших на слизистую во время ТУР. При изучении эффективности однократного внутрипузырного введения противоопухолевых средств во время ТУР отмечено снижение частоты рецидивов, что обусловлено, видимо, снижением вероятности имплантации опухолевых клеток во время операции. В настоящее время проходят клинические испытания, которые позволят сделать окончательное заключение об эффективности интраоперационной внутрипузырной терапии.
Результаты клинических испытаний препаратов интерферона а, бропирамина (иммуномодулятор для приема внутрь) и AD-32 (препарат из группы антрациклинов) продемонстрировали, что эти препараты в виде монотерапии или комбинации с другими лекарственными средствами могут быть эффективны при высоком риске рецидива или при неэффективности 1-й линии терапии. Поскольку воздействовать прямо на опухолевые клетки при раке мочевого пузыря легче, чем при опухолях другой локализации, весьма перспективной может оказаться генотерапия.
Хирургическое лечение
ТУР и лазерная коагуляция опухоли. ТУР опухоли — первый этап лечения всех больных раком мочевого пузыря. Эта операция позволяет довольно точно определить стадию и степень дифференцировки опухоли, а также показания к другим методам лечения. При одиночной высокодифференцированной поверхностной опухоли ТУР, как правило, достаточно. Можно выполнить также лазерную коагуляцию опухоли (гл. 26). Однако опыт ее применения пока невелик. Среди преимуществ этого вмешательства следует отметить снижение риска диссе-минации опухолевых клеток во время вмешательства и, следовательно, рецидива (но не метастазов) рака мочевого пузыря. Кроме того, лазерная коагуляция — отно-
сительно безболезненная операция, поэтому перед ней достаточно ввести только транквилизаторы. Главным недостатком является невозможность получить материал для гистологического исследования, поэтому биопсию приходится выполнять заранее. При раке мочевого пузыря возможна также фотодинамическая терапия. Для этого используют фотосенсибилизирующее средство — гематопорфирин.
Больные раком мочевого пузыря нуждаются в регулярном наблюдении, поскольку поверхностные опухоли рецидивируют в 30—80% случаев. Риск рецидива зависит от степени дифференцировки, стадии и числа опухолей. Его оценивают через 3 мес после ТУР. Если цистоскопия не выявляет рецидива, а первичная опухоль была одиночной и высокодифференцированной, следующее исследование проводят через год. Если же первичная опухоль была низкодифференцированной, или отмечался мультицентрический рост, или больной был оперирован по поводу рецидива рака мочевого пузыря, цистоскопию повторяют каждые 3 мес. Риск рецидива уменьшается по мере увеличения безрецидивного периода. Так, если продолжительность безрецидивного периода 5 лет, то риск рецидива составляет 22%, если -10 лет, то только 2%.
Резекция мочевого пузыря. При одиночной инвазивной опухоли (Т1—ТЗ), исходящей из заднебоковой стенки или верхушки либо из дивертикула мочевого пузыря, возможна резекция. До операции с помощью множественной биопсии исключают рак in situ. Для снижения риска диссеминации опухолевых клеток перед операцией проводят короткий курс лучевой (суммарная очаговая доза 10—16 Гр) или внутрипузырной химиотерапии. При опухолях одинаковой стадии выживаемость после резекции мочевого пузыря и после радикальной цист-эктомии одинакова, однако рецидивы после резекции мочевого пузыря возникают чаще. Поскольку в последнее время значительно усовершенствовались операции по отведению мочи, к резекции мочевого пузыря при раке прибегают редко.
Радикальная цистэктомия подразумевает удаление мочевого пузыря единым блоком с околопузырной клетчаткой и двустороннюю тазовую лимфаденэктомию. У мужчин помимо этого удаляют предстательную железу и семенные пузырьки, у женщин — матку с придатками и передней стенкой влагалища и мочеиспускательный канал. Долгое время при переходе опухоли на предстательную часть мочеиспускательного канала (в том числе при раке in situ) одновременно рекомендовалось удалять мочеиспускательный канал. Однако в последнее время появились данные о том, что это необязательно, поэтому при поражении предстательной части мочеиспускательного канала возможно создание искусственного мочевого пузыря. Аналогичная тактика применима и при раке мочевого пузыря у женщин. В отсутствие поражения шейки мочевого пузыря и опухолевых клеток по краю резекции мочеиспускательного канала создают искусственный мочевой пузырь. Такая операция
Глава 21. Опухоли мочевого пузыря, почечной лоханки и мочеточника



 возможна примерно у 66% женщин, которым выполняется радикальная цистэктомия.
возможна примерно у 66% женщин, которым выполняется радикальная цистэктомия.
В прошлом для снижения риска рецидива было принято проводить предоперационную дистанционную лучевую терапию в суммарной очаговой дозе 20—40 Гр. Преимущества этой схемы лечения были особенно заметны при опухолях с глубокой инвазией (ТЗЬ), а также в тех случаях, когда лучевая терапия приводила к уменьшению опухоли. Более поздние исследования поставили под сомнен ие эффективность предоперационной лучевой терапии. У большинства больных, которым была показана радикальная цистэктомия, предоперационная лучевая терапия не улучшала результаты лечения.
При гистологическом исследовании после радикальной цистэктомии метастазы в тазовые лимфоузлы обнаруживают у 20—35% больных, то есть чаще, чем при обследовании перед операцией. Прогноз при поражении регионарных лимфоузлов неблагоприятный, поскольку у большинства больных появляются отдаленные метастазы. Только в 10—33% случаев при единичных метастазах в регионарные лимфоузлы радикальная цистэктомия излечивает больных. У остальных применяют адъювант-ную химиотерапию (см. ниже). Хирургические методики отведения мочи разнообразны. Следует стремиться к созданию искусственного мочевого пузыря или мочевого резервуара, которые избавляют больных от необходимости носить мочеприемник (гл. 25).
Лучевая терапия
Альтернативу радикальной цистэктомии при раке мочевого пузыря с глубокой инвазией представляет дистанционная лучевая терапия. Суммарная очаговая доза 50—70 Гр подводится за 5—8 нед. Большинство больных хорошо переносят лечение. Однако у 15% развиваются тяжелые лучевые колит, проктит или цистит. Пятилетняя выживаемость при опухолях Т2 и ТЗ составляет 18-41%. К сожалению, у 33—68% больных, получавших только лучевую терапию, возникают рецидивы. Выживаемость после лучевой терапии ниже, чем после комбинированного лечения, включающего предоперационную лучевую терапию и радикальную цистэктомию. Некоторые авторы рекомендуют начинать лечение с лучевой терапии у всех больных раком мочевого пузыря и выполнять радикальную цистэктомию лишь тем больным, у которых лучевая терапия не привела к полной регрессии опухоли. Однако нельзя забывать, что радикальная цистэктомия после полного курса лучевой терапии чаще сопровождается осложнениями и может оказаться технически невыполнимой.
Date: 2016-11-17; view: 346; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |