
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Косвенное титрование
Метод Къельдаля
К косвенному способу титрования следует отнести метод определения азотсодержащих лекарственных веществ, получивший название метода Къельдаля. Метод Къельдаля сочетает процесс получения из лекарственного вещества летучего амина, перегоняемого с водяным паром, который образует с борной кислотой соль, определяемую затем ацидиметрически (вариант вытеснения). Метод Къельдаля может осуществляться в классическом и модифицированном вариантах.
Подробно метод Къельдаля рассмотрен в разделе 8
Вариант присоединения
Этот метод является специфичным для формальдегида. Метод основан на свойстве альдегидов вступать в реакции присоединения по карбонильной группе. Присоединение формальдегидом сульфида натрия протекает стехиометрично, в результате образуется сульфитное производное и эквивалентное количество щелочи, которую оттитровывают раствором кислоты хлористоводородной (индикатор – фенолфталеин).
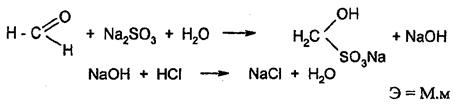
Алкалиметрия
Вариант нейтрализации
Вариант нейтрализации основан на свойстве неорганических и органических кислот взаимодействовать со щелочами с образованием солей. Титрование, за редким исключением, прямое. Конец титрования устанавливают в случае определения слабых кислот (барбитураты, сульфаниламиды), используя тимолфталеин, более сильных – феноловый красный, фенолфталеин или метиловый оранжевый.
По этому варианту определяют:
Сильные неорганические кислоты, например, кислоту хлористоводородную:
HCl + NaOH → NaCl + H2O Э = М.м.
Слабые неорганические кислоты, например, кислоту борную (КДисс = 5,75×10-10). При титровании этой кислоты щелочью образуются сильно гидролизующиеся соли и щелочная реакция в растворе появляется значительно раньше достижения точки эквивалентности.
H3BO3 + NaOH → NaBO2 + 2H2O
NaBO2 + 2H2O 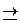 NaOH + H3BO3
NaOH + H3BO3
Для усиления кислотных свойств кислоты борной используют её свойство реагировать с многоатомными спиртами с образованием более сильных, чем борная, комплексных кислот, которые можно точно титровать по фенолфталеину. С этой целью, как правило, используют нейтрализованный глицирин, при этом образуется более сильная глицероборная кислота:
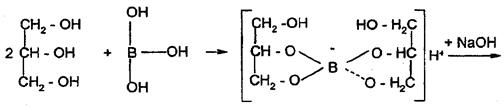
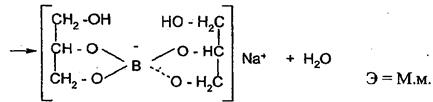
Глицерин вводится в избытке для связывания всей борной кислоты и подавления гидролиза натриевой соли глицероборной кислоты. При недостатке глицерина эта соль может гидролизоваться, вследствие чего среда становится щелочной раньше достижения точки эквивалентности. Учитывая это, в конце титрования после появления розовой окраски индикатора добавляют еще глицерин. Сохранение окраски свидетельствует о конце титрования. Если она исчезает, титрование продолжают до появления устойчивой розовой окраски.
Карбоновые кислоты в большинстве своем относятся к слабым кислотам (Кдисс= 10-5 – 10-4), как правило, нерастворимы в воде, поэтому их предварительно растворяют в спирте или ацетоне, нейтрализованных по применяемому в данном определении индикатору. Так, например, анализируют кислоты: салициловую, бензойную, никотиновую, мефенамовую, ацетилсалициловую, ибупрофен.
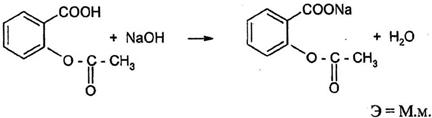
При определении кислоты ацетилсалициловой необходимо учитывать возможность гидролиза по сложноэфирной связи, для предупреждения которого титрование проводят быстро. Навеску растворяют в охлажденном до 8 - 10°С спирте.
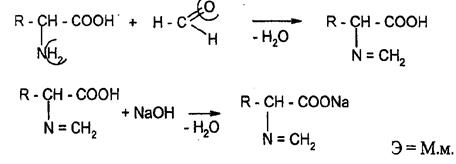
Аминокислоты алифатического ряда. Они являются амфотерными соединениями, так как содержат карбоксильную группу, проявляющую кислотные свойства, и аминогруппу, обладающую основными свойствами. В водных растворах аминокислоты образуют внутренние соли за счет собственных амино- и карбоксильной группы (H3N+-CH2-COO-), поэтому алкалиметрическое определение затруднено. Для анализа аминокислот используют формольный метод Серенса, в котором для связывания (блокирования) аминогруппы к ним добавляют формалин. Образующееся N-метиленовое производное титруют щелочью по фенолфталеину или тимолфталеину. Так определяют аминалон, метионин, цистеин, аминокапроновую кислоту.
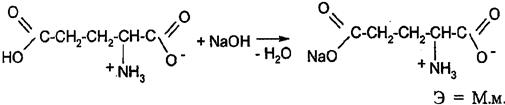
Кислота глютаминовая содержит две карбоксильные группы, поэтому в зависимости от условий анализа может титроваться как одноосновная или как двухосновная. При титровании раствором щелочи в присутствии бромтимолового синего или нейтрального красного (без формалина) во взаимодействие вступает только свободная карбоксильная группа, т.к. рКА этой группы равен 4,25, рКА второй карбоксильной группы равен 2,19.
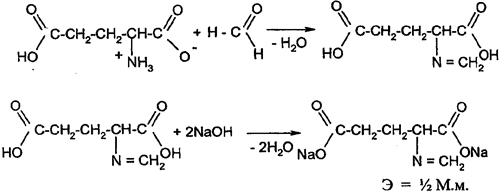
В присутствии формалина или органических растворителей (ацетон) глютаминовая кислота титруется как двухосновная по индикатору фенолфталеину:
Барбитураты, сульфаниламиды. Барбитураты (барбитал, фенобарбитал), вследствие наличия в структуре имидных групп, существуют в растворах в двух таутомерных формах имидной (I) и имидольной (II):
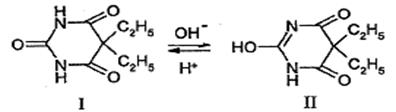
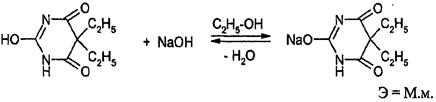
Имидольная форма обладает слабыми кислотными свойствами и может реагировать со щелочами с образованием соли.
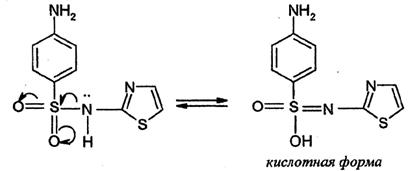
Кислотный характер сульфаниламидов (норсульфазол) обусловлен смещением электронной плотности в сторону электроотрицательных атомов кислорода сульфогруппы, которая приводит к тому, что водород при атоме азота становится подвижным, образуется таутомерная форма, обладающая слабыми кислотными свойствами.


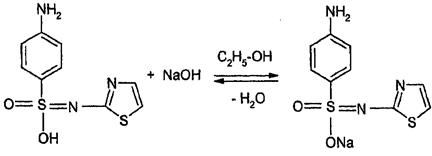
Э = М.м.
Так можно определить норсульфазол, сульфадимезин, сульфален, этазол.
При определении фталазола (обратное титрование) нейтрализация идет по сульфамидной и карбоксильной группам.

Определение проводят в присутствии органического растворителя, индикатор тимолфталеин или смешанный (тимоловый синий и фенолфталеин 1: 1).
Кислые соли многоосновных кислот, например, натрия гидроцитрат.
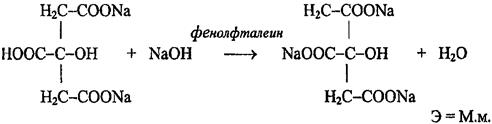
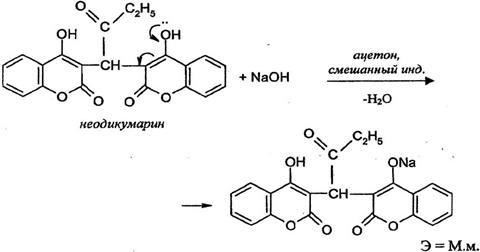
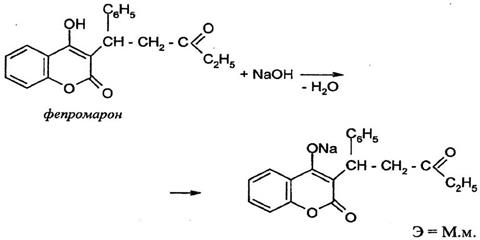
Вещества, содержащие енольный гидроксил (кислота аскорбиновая, бутадион, неодикумарин, фепромарон).
Енольные гидроксилы придают лекарственным веществам кислотные свойства вследствии эффекта сопряжения неподеленных электронных пар кислородного атома с π-электронами двойной связи.
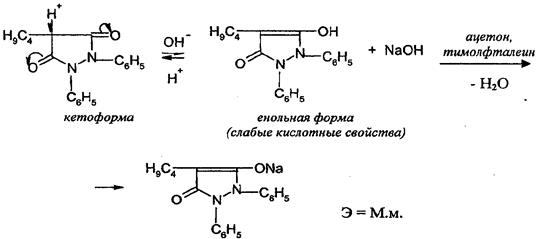
Кислотные свойства бутадиона обусловлены кето-енольной таутомерией.
Кислота аскорбиновая содержит ендиольную группировку в положении 2,3. Сопряжение карбонильной группы с двойной связью усиливает кислотность ендиольных групп. Кислород карбонильной группы (сильно электроотрицательный элемент) образует водородную связь с атомом водорода гидроксильной группы при С2, поэтому взаимодействие с натрия гидроксидом идет только по гидроксилу при С3.
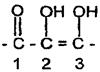
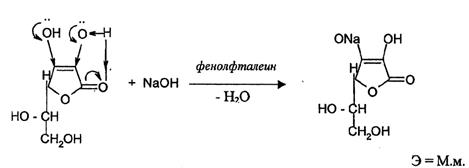
Вариант вытеснения
Вариант вытеснения – основан на свойстве сильных оснований вытеснять слабые основания из их солей. Способ титрования – прямой, индикатор – фенолфталеин.
По этому варианту определяют соли алкалоидов и азотистых оснований
R × HCl + NaOH → R↓ + NaCl + H2O
в органическую
фазу
где R – органическое основание
Определение проводят в присутствии органического растворителя, который выбирают с учетом рКА ≥ 7 (атропина сульфат, новокаин, кодеина фосфат) применяют этанол или спирто-хлороформную смесь; при титровании солей более слабых оснований (папаверина гидрохлорид, дибазол, пилокарпина гидрохлорид) используют, как правило, хлороформ.
Кодеина фосфат является солью трехосновной кислоты, однако при взаимодействии его со щелочью образуются либо монозамещенная, либо двузамещенная соли фосфорной кислоты, что зависит от рН в точке эквивалентности и, соответственно, от используемого индикатора. Средняя соль не образуется, т.к. диссоциация фосфорной кислоты по третьей ступени незначительна.
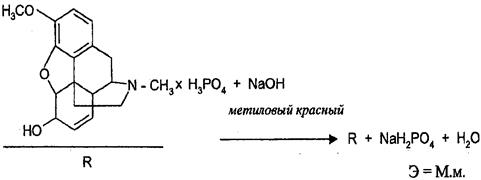
R × H3PO4 + 2NaOH 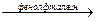 R + Na2HPO4 + 2H2O
R + Na2HPO4 + 2H2O
Э = ½ М.м.
Некоторые лекарственные вещества этой группы содержат фенольный гидроксил, который обладает слабыми кислотными свойствами и может реагировать с титрантом в случае использования в качестве индикаторов фенолфталеина или тимолфталеина, тогда рекомендуется поступать следующим образом.
- Добавлять большой объем спирта, чтобы подавить диссоциацию фенольного гидроксила.
Например, мезатон следует титровать в присутствии спирто-хлороформной смеси (3: 1).
- Выбрать индикатор, при титровании с которым исключается мешающее влияние
фенольного гидроксила. Так, например, поступают в случае титрования пиридоксина
гидрохлорида, используя в качестве индикатора бромтимоловый синий.
- Использовать экстрагент, извлекающий компонент, содержащий фенольный гидроксил.
Например, определение пилокарпина гидрохлорида в присутствии резорцина проводят,
добавляя спиртоэфирную смесь. Эфир извлекает резорцин, что позволяет в этих
условиях титровать пилокарпина гидрохлорид по фенолфталеину.
При алкалиметрическом определении лекарственных веществ, содержащих сложноэфирную группу (атропина сульфат, новокаин) титрование проводят быстро, чтобы исключить возможность гидролитического разложения лекарственного вещества.
Вариант гидролитического разложения
Вариант гидролитического разложения – основан на свойстве лекарственных веществ гидролизоваться в щелочной среде.
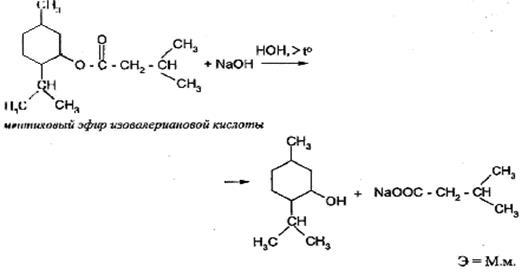
Применяется в количественном анализе сложных эфиров, амидов. Например, фенилсалицилата, метилового эфира изовалериановой кислоты (в валидоле) и других органических неустойчивых соединений (хлоралгидрат).
Реакция гидролитического разложения протекает медленно, поэтому для её ускорения определение проводят при нагревании или кипячении. Используют способ обратного титрования с постановкой контрольного опыта. В качестве индикаторов используют фенолфталеин, бромкрезоловый пурпуровый или смешанный индикатор.
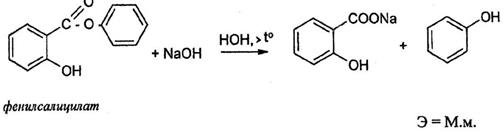
При гидролитическом разложении сложных эфиров образуется соль соответствующей кислоты и спирт или фенол. Например, определение метилового эфира изовалериановой кислоты в валидоле или фенилсалицилата.
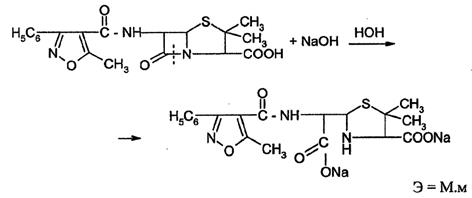
На щелочном гидролизе по β-лактамному циклу основано количественное определение оксациллина натриевой соли (лактам-внутренний амид).
Date: 2015-09-18; view: 3549; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |