
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Переход жидкости в пар
Переход жидкости в парообразное состояние возможен двумя путями:
· посредством испарения;
· посредством кипения.
Испарение жидкости происходит только с поверхности и при любой температуре. Кипение возникает во всей массе жидкости и при строго определенной температуре, зависящей только от рода жидкости и давления, под которым она находится.
Как происходит процесс испарения? Молекулы жидкости связаны между собой силами взаимодействия. Чтобы молекула могла вырваться из жидкости, необходимо, чтобы энергия ее поступательного движения была достаточна для преодоления сил взаимодействия молекул.
Так как в жидкости скорости молекул распределены согласно распределения Максвелла, в ней всегда присутствует определенное число молекул, обладающих достаточно большой кинетической энергией, которые в основном и покидают жидкость при испарении. Этим объясняется охлаждение жидкости при испарении. Таким образом, для превращения жидкости в пар без изменения температуры необходимо затратить определенное количество теплоты. Количество теплоты, необходимое для превращения единицы массы жидкости в пар, называется удельной теплотой парообразования r. Величина r зависит от природы жидкости и температуры; для воды эта величина приведена в табл.3.4.
Если жидкость находится в замкнутом сосуде, число молекул, вылетевших из нее и находящихся в парообразном состоянии вблизи поверхности жидкости, постепенно возрастает. Молекулы пара при своем беспорядочном движении залетают обратно в жидкость. По мере увеличения числа молекул пара возрастает и количество молекул, залетевших обратно в жидкость. В некоторый момент наступит динамическое равновесие: число молекул, вылетевших из жидкости за некоторое время, сделается равным числу молекул, залетевших обратно в жидкость. В этом случае говорят, что пар насытил пространство.
Опыт показывает, что ненасыщающие пары подчиняются газовым законам (т.е.законам идеального газа).
Ненасыщающие пары газовым законам не подчиняются. Давление (упругость) насыщающего пара данной жидкости зависит только от температуры.
При изотермическом сжатии насыщающего пара его давление не изменяется, только часть пара переходит в жидкое состояние; при расширении, наоборот, часть жидкости переходит в пар и давление вновь остается прежним. Для осмысления материала предлагаем вам указать на рис. 3.2 участок изотермы, соответствующий этим процессам (правильный ответ вы можете найти в сноске[6]). Если же в пространстве, где находится пар, нет больше этой жидкости, пар становится ненасыщающим (попробуйте найти такой участок на графике 3.2, а затем проверить правильность ваших понятий, прочитав сноску[7]). При охлаждении насыщающего пара часть его выделяется в виде жидкости, давление же оставшегося пара соответствует той упругости, которую он должен иметь при пониженной температуре (такие процессы Вы можете найти и указать на рис. 3.3 и проверить себя, прочитав сноску[8]). Давление насыщающего водяного пара в зависимости от температуры приведено в табл. 3.4.
Кипение - это парообразование, происходящее во всем объеме жидкости. При заданном давлении жидкость кипит при определенной температуре, которая повышается, если внешнее давление увеличить.
Сравнивая температуры кипения воды у подножия горы и на ее вершине, можно заметить, что вода кипит при различных температурах. Если в сосуде над поверхностью воды, взятой при комнатной температуре, постепенно разрежать воздух, можно добиться того, что вода закипит. При достаточном вакууме вода может закипеть при 0˚C. Таким образом, вода закипает при такой температуре, при которой упругость ее насыщающих паров становится равной внешнему давлению. Такой же вывод можно сделать и для всякой другой жидкости.
Как это можно объяснить? В воде всегда имеется растворенный воздух, который выделяется в виде мельчайших пузырьков, обычно оседающих на стенках и дне сосуда. Пузырьки наполнены насыщающим водяным паром. Если нагревать жидкость до такой температуры, при которой упругость пара в пузырьке сделается хотя бы на ничтожную долю больше внешнего давления, пузырек начинает расти, наполняться насыщающим паром и затем всплывает на поверхность воды; начинается кипение.
Влажность воздуха определяется содержанием в воздухе водяного пара. Это понятие часто встречается на практике, и поэтому мы перечислим здесь смысл основных терминов, связанных с этим понятием.
Абсолютная влажность характеризует массу водяного пара в единице объема воздуха и на практике часто измеряется в г/м3.
Т а б л и ц а 3.4
Давление водяного пара, насыщающего пространство при разных температурах
| t, ˚C | pн, Па | t, ˚C | pн, Па | t, ˚C | pн, Па |
| -5 |
Упругость водяного пара p (или его парциальное давление) измеряется в ех же единицах, что и давление воздуха – pв. При расчете влажности атмосферного воздуха температура газа практически всегда бывает заметно меньшей критической температуры для воды (Tк=374˚C). В этом случае максимальное давление Ван-дер-Ваальсовского пара p1 (см. рис. 3.3) достаточно сильно отличается от давления насыщающего пара pн. С другой стороны добавочные члены, введенные в уравнение состояния газа Ван-дер-Ваальсом, становятся существенными на участке 2-2', вблизи точки максимума изотермы (см. рис. 3.3). На участке изотермы 1-2 влияние поправок Ван-дер-Ваальса для атмосферного пара мало и, следовательно, параметры даже насыщающего водяного пара при атмосферных температурах можно с достаточной точностью рассчитывать, используя уравнение состояния идеального газа.
Относительная влажность (w) - это отношение упругости водяного пара к упругости пара (pн), насыщающего воздух при данной температуре:
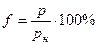 (измеряется в процентах).
(измеряется в процентах).
Температура точки росы (τ)} - это температура, при которой влажный воздух, если его изобарически охладить, становится насыщенным водяным паром. На поверхности любого тела, имеющего температуру, меньшую или равную температуре точки росы окружающего воздуха, происходит конденсация водяного пара (стекла очков запотевают при входе в теплое помещение в морозную погоду).
Влажность воздуха измеряется приборами, которые называются гигрометрами и психрометрами. Простейший психрометр состоит из двух термометров, один из которых имеет увлажненную поверхность. Вследствие зависимости интенсивности испарения от степени насыщения воздуха парами воды разность показаний сухого и влажного термометров тем больше, чем меньше влажность. Величину влажности определяют при этом по разности этих температур с помощью специальной психрометрической таблицы. В настоящее время имеется ряд радио- и лазерных методов измерения влажности воздуха.
Date: 2015-05-09; view: 1175; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |