
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Реакции второго порядка
Рассмотрим реакцию, протекающую по уравнению:  . Скорость реакции можно выразить по основному закону кинетики через концентрации СА и СВ.
. Скорость реакции можно выразить по основному закону кинетики через концентрации СА и СВ.
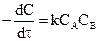 .
.
В данном уравнении три переменные. Для исключения одной из них выразим СА и СВ через количество прореагировавших веществ за время τ:
При 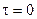
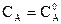 ;
; 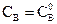
При 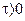
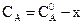 ;
; 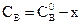 , где х – количество молей А и В, прореагировавших к моменту времени τ.
, где х – количество молей А и В, прореагировавших к моменту времени τ.
В этом случае основной постулат кинетики: 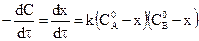 .
.
После интегрирования в пределах от 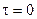 до τ, от
до τ, от 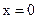 до х, получим:
до х, получим:
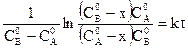 .
.
Решив данное уравнение относительно k, найдем:
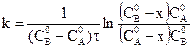 .
.
Из данного уравнения следует, что размерность k в уравнении скорости второго порядка [время-1×концентрация-1]. Следовательно, числовые значения константы скорости в реакциях второго порядка будут зависеть от того, в каких единицах выражаются время и концентрация реагирующих веществ.
Из данного уравнения всегда можно определить количество прореагировавшего х:
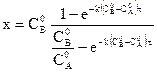 .
.
Если начальные концентрации 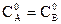 , уравнение
, уравнение 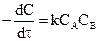 принимает вид:
принимает вид:
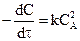 или
или 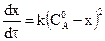 ,
,
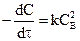 или
или 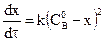 .
.
 При записи в общем виде индексы у концентраций реагентов можно опустить
При записи в общем виде индексы у концентраций реагентов можно опустить 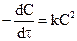 или
или  .
.
Интегрируя в пределах от 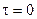 до τ, получим:
до τ, получим:
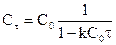 .
.
В этом случае константу скорости можно определить:
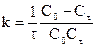 .
.
Данное выражение можно представить в виде:
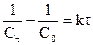 или
или 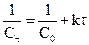 .
.
Отложив на оси ординат 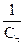 , а на оси абсцисс время τ, получим прямую, тангенс угла которой равен k.
, а на оси абсцисс время τ, получим прямую, тангенс угла которой равен k.
Период полураспада реакции второго порядка определяется по формуле:
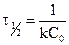 .
.
В отличие от реакции первого порядка время половинного превращения для реакции второго порядка обратно пропорционально С0.
Date: 2015-05-09; view: 792; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |