
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Энергетика химический процессов. Элементы химической термодинамики. Первое начало термодинамики. Внутренняя энергия и энтальпия
Химическая термодинамика изучает переходы одних форм энергии в другие, имеющие место в химических реакциях, процессах растворения, кристаллизации, электронных процессах и т.д. или вообще − в химических системах.
Термодинамической системой называется комплекс взаимодействующих между собой физических тел, мысленно обособленный от окружающей среды.
Химическая система – это частный случай термодинамической системы. Химическая система может быть:
- гомогенной (однофазной) – все составляющие компоненты системы находятся в одной фазе (например, жидкие).
- гетерогенной (многофазной) – все составляющие компоненты системы находятся в разных фазах (напр., жидкость + газ и др.)
Всякое тело (система) содержит в скрытом виде энергию - так называемую внутреннюю энергию U, которая обусловлена различными формами движения частиц (молекул, атомов, электронов, ядер) и межчастичным взаимодействием, т.е. это сумма кинетической и потенциальной энергии всех частиц в системе.
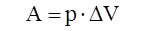
где p – внешнее давление; ∆V – изменения объёма системы.
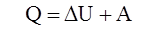 (5.2)
(5.2)
Первое начало термодинамики. Приращение внутренней энергии какой-либо системы равно количеству сообщаемой системе теплоты за вычетом работы, совершаемой системой.
Приращение внутренней энергии какой-либо системы равно количеству сообщаемой системе теплоты за вычетом работы, совершаемой системой.
Обозначим: 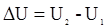 ,
,
Энтальпия – это функция состояния. Она характеризует полную энергию системы в условиях p=const и t=const и равна сумме внутренней энергии и работы против внешних сил.
Date: 2015-09-22; view: 468; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |