
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения задач. Пример 1. Вычислить изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли после добавления к 1 л раствора 0,1 моль соляной
Пример 1. Вычислить изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли после добавления к 1 л раствора 0,1 моль соляной кислоты.
Решение. 1. вычислим рН данного буферного раствора по формуле (112)
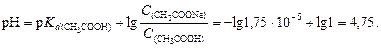
2. После добавления к буферному раствору соляной кислоты концентрация ацетата натрия уменьшится, концентрация уксусной кислоты увеличится вследствие протекания реакции:
CH3COONa + HCl ® CH3COOH + NaCl на величину 0,1 моль/л.
3. Вычислим рН нового раствора:
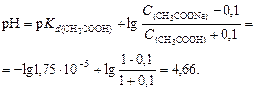
4. Найдем изменение рН: ΔрН = 4,75 - 4,66 = 0,09.
Пример 2. К 0,8 л 0,5 М раствора НСООН (Kd = 1,8×10-4) добавили 0,2 л 0,4 М раствора NaOH. Вычислить рН образовавшегося формиатного буфера и его буферную емкость по кислоте и щелочи.
Решение. 1. Вычислим количество вещества НСООН и NaOH:
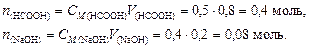
2. Объем буферного раствора V равен:
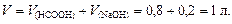
3. Определим количество вещества формиата натрия, образующегося по реакции NaOH+HCOOH®HCOONa+H2O:
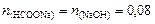 моль.
моль.
Найдем молярную концентрацию формиата натрия в буферном растворе:
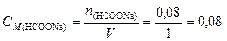 моль/л.
моль/л.
4. Найдем остаточное количество вещества муравьиной кислоты:
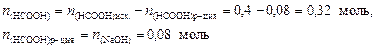
и ее молярную концентрацию в буферном растворе
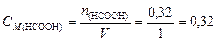 моль/л.
моль/л.
5. Определим рН буферного раствора
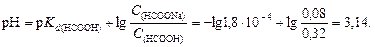
6. Буферную емкость по кислоте определим при помощи уравнения (120):
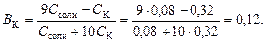
Буферную емкость по щелочи определим при помощи уравнения (119):
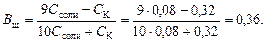
Пример 3. Сколько граммов твердого формиата натрия HCOONa надо добавить к 100 мл 0,2 М раствора соляной кислоты, чтобы получить буферный раствор с рН = 4,3?
Решение. 1. При добавлении к раствору соляной кислоты формиата натрия образуется муравьиная кислота по реакции: HCOONa + HCl ® HCOOH + NaCl,
С (HCOOH) = С (HCl) = 0,2 моль/л.
2. Для образования формиатного буферного раствора необходима определенная концентрация формиата натрия, которую найдем исходя из формулы (114):
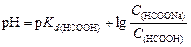
откуда  моль/л.
моль/л.
3. Определим количество вещества формиата натрия, необходимого для получения данного буферного раствора:  моль и его массу
моль и его массу 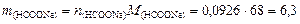 г.
г.
Date: 2015-09-24; view: 1986; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |