
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретическое обоснование. Для определения концентрации вещества A можно применять термометрическое титрование, которое основано на использовании теплоты
Для определения концентрации вещества A можно применять термометрическое титрование, которое основано на использовании теплоты, выделяющейся (или поглощающейся) при химических реакциях. Для этого подбирают вещество B (титрант), который вступает в идущую до конца реакцию с веществом A. К титруемому раствору приливают постепенно титрант. В ходе добавления титранта в результате взаимодействия веществ A и B выделяется или поглощается теплота и температура реакционной смеси меняется до тех пор, пока вещество A не прореагирует полностью. По достижении стехиометрического соотношения A и B дальнейшее приливание титранта не изменяет температуры реакционной смеси и она остаётся постоянной или плавно меняется за счёт теплообмена с окружающей средой. На кривой зависимости изменения температуры реакционной смеси от количества добавленного раствора B появляется точка перегиба, позволяющая определить стехиометрическое количество вещества B.
Термометрическое титрование применяется и тогда, когда другие методы титрования неприменимы. При удачном подборе титрующего реагента метод можно применять для титрования окрашенных, вязких веществ и систем, содержащих смолистые или твёрдые примеси. Термометрическое титрование можно применять для следующих типов реакций:
1) взаимодействие кислот и оснований:
NaOH+HCl=NaCl+H2O; NH4OH+HCl=NH4Cl+H2O.
Концентрация титруемого раствора не должна быть меньше 0,05…0,5 н (при низких концентрациях мало изменение температуры) и не превышать 1 н, так как смешение концентрированных растворов кислот и щелочей кроме теплоты нейтрализации сопровождается выделением теплоты разбавления;
2) реакции, при которых одним из конечных продуктов является практически нерастворимый осадок:
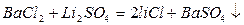 ;
;
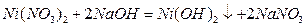 .
.
Чем меньше растворимость осадка, тем выше точность результатов титрования. Произведение растворимости вышеприведённых гидроксидов составляет:
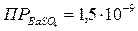 ;
; 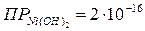 .
.
Незначительная растворимость этих осадков позволяет с достаточной точностью (±1%) определить концентрации ионов Li+ и Na+ в 0,05…0,5 н раствора;
3) реакции, при которых одним из продуктов является растворимое устойчивое комплексное соединение:
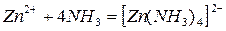
Устойчивость комплексного соединения определяется константой нестойкости:
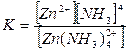 .
.
В данной работе следует определить концентрацию соляной кислоты по тепловому эффекту реакции нейтрализации.
Date: 2015-09-19; view: 300; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |