
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глава 3. Термохимия
3.1. Энтальпия.
Если система характеризуется только одним внешним параметром V, т.е. может совершаться только работа расширения, тогда первый закон может быть записан в виде
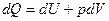
Если 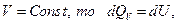 т.е. тепловой процесс эффекта равен изменению функции состояния. Найдем такую функцию состояния, изменение которой равно тепловому эффекту при постоянном давлении. Для этого выражение для I закона необходимо преобразовать так, чтобы давление находилось под знаком дифференциала. Обратим внимание, что
т.е. тепловой процесс эффекта равен изменению функции состояния. Найдем такую функцию состояния, изменение которой равно тепловому эффекту при постоянном давлении. Для этого выражение для I закона необходимо преобразовать так, чтобы давление находилось под знаком дифференциала. Обратим внимание, что
d (pV) = pdV + Vdp и pdV = = d (pV) – Vdp, а подстановка в выражение для I закона дает
dQ = dU + d (pV) – Vdp = d (U + pV) – Vdp = dH -Vdp
| H ≡ U + pV | -функция состояния называется энтальпией. |
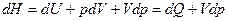
При 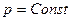
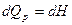
Выберем в качестве независимых переменных Т и р, тогда
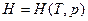
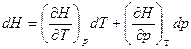
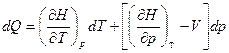
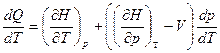
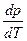 - отношение приращения независимых переменных является неопределенной величиной, чтобы избежать этого нужно указать конкретный процесс. Если
- отношение приращения независимых переменных является неопределенной величиной, чтобы избежать этого нужно указать конкретный процесс. Если
p = Const, то
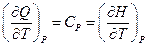
Очевидно есть определенная симметрия между U и H
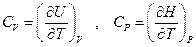
3.2. Теплоты химических реакций. Закон Гесса.
При химических реакциях происходит изменение U, поскольку U продуктовреакцииотличается от U исходных веществ. Пусть
U2 – внутренняя энергия продуктов реакции
U1 – внутренняя энергия исходных веществ
ΔU = U2 –U1 - изменение U в результате химического процесса. Аналогично для энтальпии.
Изучением теплот химических реакций занимается термохимия.
Q -теплота химической реакции зависит от способа проведения химической реакции.
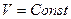
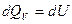
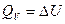
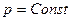
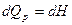
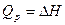
Т. о. в этих случаях Q равна изменению функции состояния и поэтому не зависит от пути процесса, а лишь от начального и конечного состояния.
Закон Гесса (1836). Если из данных исходных веществ можно получить заданные конечные продукты разными путями, то суммарная теплота процесса (при 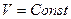 или при
или при 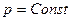 ) на одном каком-нибудь пути равна суммарной теплоте процесса на любом другом пути, т.е. не зависит от пути перехода от исходных вществ к продуктам реакции.
) на одном каком-нибудь пути равна суммарной теплоте процесса на любом другом пути, т.е. не зависит от пути перехода от исходных вществ к продуктам реакции.
3.3. Термохимические уравнения.
Date: 2015-09-18; view: 301; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |