
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

IV. Кислородные соединения углерода
Углекислый газ СO2 как типичный кислотный оксид взаимодействует с щелочами (например, вызывает помутнение известковой воды), с основными оксидами и водой. Он не горит и не поддерживает горения и потому применяется для тушения пожаров. Однако магний продолжает гореть в углекислом газе с образованием оксида и выделением углерода в виде сажи:
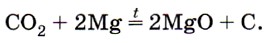
Угольная кислота и её соли
При растворении углекислого газа в воде образуется очень слабая угольная кислота Н2СО3.
Угольная кислота – слабая неустойчивая кислота, которую в свободном состоянии из водных растворов выделить нельзя.
Проявляет свойства слабых кислот. Будучи двухосновной, образует два типа солей карбонаты и гидрокарбонаты.
Свойства солей
1. Карбонаты двухвалентных металлов трудно растворимы в воде, но их растворимость повышается в присутствии углекислого газа за счет образования гидрокарбонатов:
СаСО3 + СО2 + Н2О = Са(НСО3)2.
2. Карбонаты металлов (кроме щелочных металлов) при нагревании декарбоксилируются с образованием оксида:
CuCO3 = CuO + CO2.
карбонаты щелочных металлов не разлагаются.
3. Гидрокарбонаты разлагаются до карбонатов:
2NaHCO3 = Na2CO3 + H2O + CO2.
Качественной реакцией на карбонат и гидрокарбонат ионы является их взаимодействие с сильной кислотой, наблюдается образование углекислого газа с характерным вскипанием:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑;
CO32- + 2H+ = CO2 + H2O.
Кремний
Общая характеристика кремния
Si …3s2 3p2
Возможные степени окисления:
Si0 – 4e → Si+4
Восстановитель
Si0 + 4e → Si-4
Окислитель
Date: 2015-08-07; view: 349; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |