
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основные свойства железа
ЖЕЛЕЗО - переходный ферромагнитный металл. Порядковый номер-26, атомная масса-55, 85, плотность-7784 кг/м3, (7,784 г/см3), температура плавления - 1539°С.
Чистое железо (99,9917%) имеет твердость по Бринеллю 490МПа (49 НВ). Технически чистое железо (99,9 - 99,8%) имеет твердость около 90 НВ, σВ = 300 - 350 МПа (30-35 кгс/мм2), δ = 35 - 40%.
Особо важным свойством железа является его аллотропия, т. е. наличие нескольких кристаллических модификаций.
Низкотемпературное α железо (ниже 910о С) и высокотемпературное δ - железо (выше 1392оС и до температуры плавления) имеют одинаковую объемно центрированную кубическую решетку (ОЦК). В интервале температур 910 – 1392оС стабильным является γ - железо с гранецентрированной кубической решеткой (ГЦК). Feβ является немагнитной разновидностью Feα (при превращении α↔β в точке Кюри А2 при температуре 768о пространственная решетка не меняется).
С металлами железо образует твердые растворы замещения, а с углеродом, азотом, бором, водородом (имеющими малый радиус атомов) - твердые растворы внедрения.
Наиболее широкое применение в различных отраслях промышленности получили железоуглеродистые сплавы - стали и чугуны.
УГЛЕРОД - порядковый номер 6, атомная масса 12,011, имеет плотность 2300 кг/м3, температуру возгонки около 3500 °С, может находиться в двух аллотропических модификациях: графит и алмаз.
Углерод в сплавах с железом может существовать в виде цементита (карбида железа Fe3C) и в виде графита (свободный углерод). Цементит (800 НВ) является неустойчивым химическим соединением, имеет сложную орторомбическую кристаллическую решетку. При высокой температуре и продолжительной выдержке цементит распадается с образованием графита и аустенита. Этот процесс имеет важное практическое значение для высокоуглеродистых сплавов - чугунов. В сталях, где концентрация углерода сравнительно невысока, цементит имеет большую устойчивость.
Графит- углерод, выделяющийся в железоуглеродистых сплавах в свободном состоянии. Имеет гексагональную кристаллическую решетку. Графит электропроводен, химически стоек, малопрочен, мягок.
Диаграмма фазового равновесия «железо - углерод»
Среди диаграмм состояния металлических сплавов самое большое значение имеет диаграмма состояния системы Fe-С. Это объясняется тем, чтог в технике наиболее широко применяются железоуглеродистые сплавы. Современный вариант диаграммы состояния «железо - углерод» приведен на рис. 6.1. Характерной особенностью этой диаграммы является то, что на ней нанесены две системы одновременно:система Fe – Fe3C (железо - цементит)-метастабильная - и (железо - графит)-стабильная. Большое практическое значение имеет метастабильная диаграмма, т.к. с помощью этой диаграммы объясняют превращения, происходящие в сталях и белых чугунах. Диаграмма является основой для рационального выбора оптимальных режимов термической обработки железоуглеродистых сплавов.
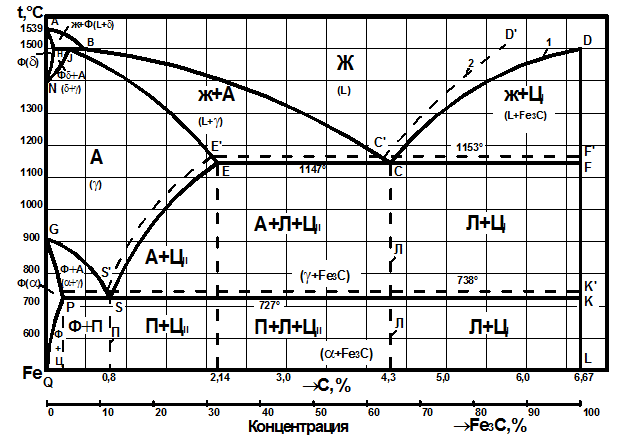 Рис 6.1. Диаграмма состояния «железо-углерод»: I - метастабильная; 2 - стабильная
Рис 6.1. Диаграмма состояния «железо-углерод»: I - метастабильная; 2 - стабильная
Date: 2015-07-24; view: 871; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |