
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Радиочувствительность тканей, органов, организмов
Закономерности поражения целостного организма определяются двумя факторами: 1) радиочувствительностью тканей, органов и систем, существенных для выживания организма; 2) величиной поглощенной дозы облучения и ее распределением в пространстве и времени.
Каждый в отдельности и в сочетании друг с другом эти факторы определяют преимущественный тип лучевых реакций (местные или общие), специфику и время проявления (непосредственно после облучения, вскоре после облучения или в отдаленные сроки) и их значимость для организма.
Следует иметь в виду, что при переходе от изолированной клетки к ткани, к органу и организму все явления усложняются. Эго происходит потому, что не все клетки поражаются в равной степени, а тканевой эффект не равен сумме клеточных эффектов: ткани, а тем более органы и системы нельзя рассматривать как простую совокупность клеток. Находясь в составе ткани, клетки в значительной степени зависимы и друг от друга, и от окружающей среды. Митотическая активность, степень дифференцированности, уровень и особенности метаболизма, а также другие физиологические параметры отдельных клеток не безразличны для их непосредственных «соседей», а, следовательно, и для всей популяции в целом. Общеизвестно, например, что заживление раны происходит вследствие временного ускорения размножения оставшихся клеток, обеспечивающего рост ткани и замещение вызванных травмой тканевых утрат, после чего тип клеточного деления нормализуется.
В механизме таких стимулирующих и ингибирующих влияний, испытываемых клетками, принимают участие не только локальные факторы, но и регулирующие системы, поддерживающие состояние гомеостаза в организме. Нет оснований сомневаться в важной роли тех же процессов в реализации тканевых и системных реакций на облучение. Кроме того, на тканевую радиочувствительность оказывают большое влияние и другие факторы: степень кровоснабжения, величина облучаемого объема и др. Таким образом, радиочувствительность ткани нельзя рассматривать только с позиций составляющих ее клеток без учета морфофизиологических факторов. Например, эритробласты изменяют свою радиочувствительность в зависимости от места их нахождения в организме — в селезенке или костном мозге. Разную радиочувствительность имеют также одна и та же опухоль, привитая в разные органы, и ее метастазы, в зависимости от их локализации.
Все это усложняет оценку радиочувствительности тканей, органов и целого организма, но не отвергает принципиального и ведущего значения цитокинетических параметров, определяющих тип и выраженность лучевых реакций на всех уровнях биологической организации.
Самый типичный пример радиационного поражения организма животных и человека — острая лучевая болезнь, возникающая после равномерного тотального однократного внешнего облучения. В этом случае одновременно подвергаются радиационному воздействию все системы, органы, ткани и клетки в одинаковой дозе. Наилучшее понимание основных проявлений лучевого поражения организма может быть достигнуто сопоставлением их с поглощенной дозой в «критических органах».
Под критическими органами понимают жизненно важные органы или системы, первыми выходящие из строя в исследуемом диапазоне доз облучения, что обусловливает гибель организма в определенные сроки после облучения.
Таким образом, между величиной поглощенной дозы в организме и средней продолжительностью жизни существует строгая зависимость, определяемая различиями в радиочувствительности отдельных жизненно важных (критических) систем.
Еще в 40-х годах исследованиями Б. Раевского и Г. Квастлера было обнаружено, что в определенных диапазонах, несмотря на увеличение дозы, средние сроки гибели мышей не меняются. Соответствующая кривая, описывающая зависимость средней продолжительности жизни мышей от дозы облучения, состоит из трех участков (рис. III.38). Начальный участок охватывает период от нескольких недель до нескольких дней и соответствует дозам до 10 Гр. Далее следует плато, где средняя продолжительность жизни не изменяется, несмотря на увеличение дозы от 10 до 100 Гр. На третьем участке показано, что при последующем увеличении дозы средняя продолжительность жизни снова резко укорачивается от нескольких дней до нескольких часов. Рассмотренные участки кривой отражают основные клинические синдромы - костномозговой (кроветворный), желудочно-кишечный и церебральный, развивающиеся вследствие необратимого поражения соответствующих критических систем организма — кроветворной, кишечника и ЦНС.
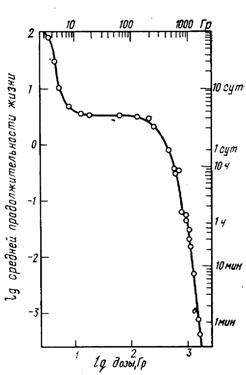
Рис. III.38. Зависимость средней продолжительности жизни мышей после однократного рентгеновского облучения от дозы (двойная логарифмическая шкала) (по Б. Раевскому, 1954)
Ступенчатый характер отмирания, связанный с выходом из строя критических систем, к настоящему времени обнаружен для самых разнообразных живых объектов (рис. III.39).
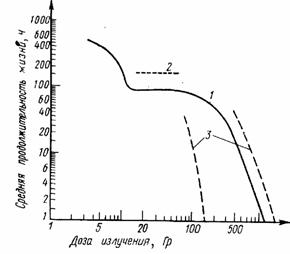
Рис. III.39. Зависимость средней продолжительности жизни млекопитающих от дозы облучения (1) и ее отклонения (2, 3), полученные разными авторами на мышах, крысах, хомячках, морских свинках и обезьянах (по В. Бонду и др., 1971)
Показано (И. Б. Бычковская, 1970) наличие такой закономерности для земноводных (лягушки), насекомых (амбарные долгоносики, бокоплавы, дрозофилы), червей и даже растений.
Таким образом, ступенчатая зависимость времени наступления гибели самых разнообразных объектов от дозы, отражающая многосистемность в реакции на облучение, — общебиологическая закономерность. Разрыв между дозами, начинающими вызывать определенные формы гибели, указывает на разницу в радиочувствительности ответственных систем (по критерию поражения, несовместимого с жизнью).
Наличие плато на кривой (рис. III.39) свидетельствует о пороговости регистрируемого эффекта, поэтому несовместимое с жизнью повреждение той или иной системы наступает по достижении определенного уровня поражения, т. е. имеет пороговый характер. Области перегиба кривой соответствуют дозам, при которых возможны те или другие формы гибели вследствие индивидуальных вариаций радиочувствительности смежных систем.
Аналогичное изменение средней продолжительности жизни, определяемое дозой облучения, показано и для человека. На рис. III.40 хорошо видны три области насыщения эффекта. Основываясь на клинической картине поражения, их связывают с теми же тремя патогенетическими механизмами поражения, приводящими организм к гибели. При дозах облучения, когда средняя продолжительность жизни не превышает 40 сут, на первый план выступает нарушение гемопоэза; при больших дозах (продолжительность жизни около 8 сут) ведущими становятся проявления поражения кишечника, а при еще больших (> 30 Гр; продолжительность жизни ~ 2 сут и менее) развиваются церебральные симптомы.
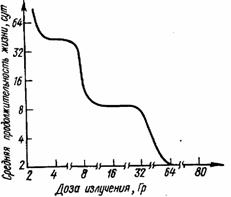
Рис. III.40. Зависимость средней продолжительности жизни человека и обезьян от дозы облучения (полулогарифмическая шкала) (по Р. Аллену и др., 1960)
Состояние устойчивого динамического равновесия любой клеточной популяции в живом организме, необходимое для нормальной жизнедеятельности, поддерживается системами обновления клеток; любая потеря клеток (вследствие их гибели или миграции) в системе количественно восполняется возникновением новых клеток, что обеспечивает неизменность функции. Клетки каждого типа имеют свою характерную для них продолжительность жизненного цикла и соответственно различаются темпом обновления.
Таким образом, взрослый организм постоянно находится в состоянии строго сбалансированного клеточного самообновления, происходящего непрерывно в ряде его жизненно важных систем.
Ежеминутно в каждой из них отмирают десятки и сотни тысяч «отслуживших» клеточных элементов, заменяясь новыми, заведомо готовыми «пожертвовать» собой через строго определенный срок - и так до конца жизни организма. Такое устойчивое равновесие в системах клеточного самообновления, являющееся необходимым условием надежности поддержания жизнеспособности организма, получило название клеточного гомеостаза.
Применительно к рассмотренным выше основным радиационным синдромам две из таких самообновляющихся систем (в основном определяющие выживание или гибель облучаемого организма) — кроветворная и желудочно-кишечная — характеризуются большой скоростью клеточного обновления. В третьей — ЦНС — у половозрелых животных и у взрослого человека клеточного обновления практически не происходит.
Костный мозг обладает крайне высокой радиочувствительностью, в связи с чем поражение системы кроветворения всегда наблюдается в той или иной степени при общем облучении как его типичное проявление. Поэтому на примере костного мозга будут рассмотрены общие принципы функционирования самообновляющейся системы, которые в полной мере сохраняют свое значение для любой другой системы клеточного обновления.
Основное назначение костного мозга — продукция зрелых высокодифференцированных клеток крови. В нормальных условиях гибель или исчезновение каждого клеточного элемента в периферической крови или в другом участке организма компенсируется образованием в среднем одной клетки в костном мозге.
По меткому выражению В. Бонда, костный мозг представляет собой «фабрику», производящую клетки, а периферическая кровь - «службу сбыта» организмом уже зрелых элементов.
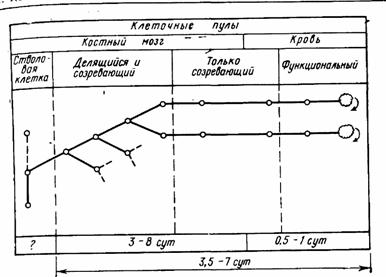
Рис. III.41. Модель системы клеточного обновления (по В. Бонду и др., 1971)
Время, указанное в нижней части рисунка, отражает порядок величин, характерных для гранулоцитопоэза млекопитающих, в том числе и человека
На рис. III.41 изображена упрощенная модель системы клеточного обновления применительно к мнелопоэзу, состоящая, как и любая система клеточного обновления, из нескольких пулов. Прежде всего, это самоподдерживающийся фонд недифференцированных предшественников — стволовых (клоногонных) клеток, способных обеспечить постоянную скорость клеточного обновления в системе. При делении стволовых клеток часть их потомства предназначается для последующей дифференциации в специфические клеточные линии, а оставшиеся служат новыми стволовыми клетками.
Пройдя одно или несколько делений, клетка постепенно дифференцируется, затем, утратив способность делиться, входит в непролиферирующий пул, где окончательно созревает и становится функционально полноценной. Ясно, что цитокинетика той или иной системы обновления предопределяется уровнем митотической активности и продолжительностью отдельных фаз клеточного цикла.
Общий принцип, обеспечивающий устойчивую работу любой системы клеточного обновления (имеется в виду поддержание ее в состоянии количественного и качественного динамического равновесия), состоит в том, что по мере отмирания и удаления зрелых клеток из функционального пула вместо каждой из них поступает новая, находящаяся в этот момент на стадии максимальной подготовленности.
Таким образом, функционирующая система самоподдерживается из-за необходимости восполнения постоянно происходящих утрат, являющихся своеобразным стимулом к активации всех предшествующих пулов, в результате чего и осуществляется перманентное клеточное обновление.
Под действием излучения в любой клеточной системе обновления происходят резкие нарушения динамического равновесия между отдельными пулами, приводящие к тяжелым функциональным расстройствам в самой системе, а в зависимости от ее значения для жизнедеятельности и к соответствующим последствиям в организме.
Качественное представление о механизме этих нарушений следует из анализа реакций облученных клеток, закономерности которых в целом сохраняются и для тканевых систем в живом организме. Это основные радиобиологические реакции клеток, определяющие типичные нарушения в любой системе обновления.
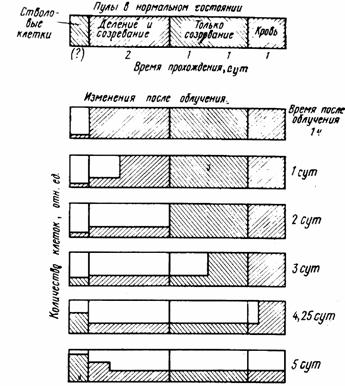
Рис. III.42. Эффекты, возникающие в системе клеточного обновления вследствие внезапного опустошения самых ранних пролиферирующих компонентов в результате облучения (по В. Бонду и др., 1971)
- Временное прекращение деления всех клеток независимо от того, какая из них выживет в последующем.
- Гибель молодых, малодифференцированных и делящихся клеток.
- Минимальные изменения продолжительности процесса клеточного созревания, а также времени жизни большинства зрелых клеток и скорости притока их в функциональный пул.
В результате три первых пула начинают опустошаться сразу и в ближайшие дни после облучения, а число соответствующих зрелых функционирующих клеток уменьшается значительно позднее, когда их естественная убыль перестает восполняться из-за опустошения предшествующих пулов (рис. III.42). Эта задержка определяется временем, необходимым клетке для прохождения пути от самых ранних стадий до выхода в функциональный пул. Количественные характеристики указанных нарушений определяются конкретными цитокинетическими параметрами той или иной системы обновления и дозой облучения.
Радиационные нарушения мнелопоэза мыши, качественно аналогичные изменениям, происходящим в последовательно связанных пулах у любой системы клеточного обновления (для случая, если опустошены более ранние компартменты), схематически показаны на рис. III.42.
С этих позиций следует несколько подробнее проанализировать радиационные изменения в системе кроветворения, так как именно с ними наиболее часто приходится встречаться на практике: при облучении в дозах до 10 Гр в организме развивается типичный костномозговой синдром.
Основная причина катастрофического опустошения костного мозга, происходящего в самые ранние сроки после облучения, состоит в резком торможении процессов клеточного деления при продолжающемся с неизменной скоростью поступлении зрелых элементов на периферию.
Внешне парадоксален, но несомненен тот факт, что на кинетике этого процесса не сказывается доля летально поврежденных клеток, увеличивающаяся с дозой облучения. Определяется это тем, что скорость клеточного опустошения костного мозга в первые сутки при всех дозах изучения одинакова, вследствие чего она описывается одной экспонентой (рис. III.43). Очевидно, вследствие сохранения скорости выхода клеток на периферию в общем «потоке» с жизнеспособными клетками выходят в кровь и летально поврежденные.
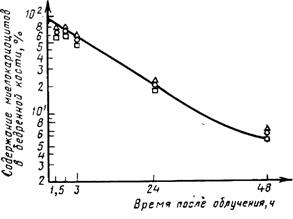
Рис. III.43. Изменение общего числа клеток костного мозга крысы после облучения в дозах 3—10 Гр
Опустошение «фабрики», отражающее, по существу, нормальную скорость выхода зрелой «продукции», сохраняет экспоненциальный характер лишь до начала регенерации. Наблюдающееся затем восстановление происходит с различной скоростью, обратной величине дозы (см. рис. III.43). Здесь-то и сказывается разная степень клеточной деструкции, определяющая глубину лейкопении, а, следовательно, течение и исход лучевого поражения организма.
Рассмотренная схема дает лишь общее представление о цитокинетике изменений в обоих компартментах кроветворения на основе принципиальных механизмов саморегуляции, типичных для систем клеточного обновления. В зависимости от объекта и дозы облучения параметры кривых имеют свои количественные характеристики и некоторые качественные особенности.
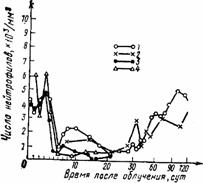
Рис. III.44. Число нейтрофилов периферической крови свиньи в разное время после облучения (по В. Бонду, 1974):
цифрами обозначены дозы облучения:
1 - 2 Гр, 2 - 3 Гр, 3 - 4 Гр, 4 — 6 Гр;
следует обратить внимание на начальное «плечо», быстрый спад, временный абортивный подъем и затем постепенное окончательное восстановление
Для примера на рис. III.44 приведены изменения в наиболее ответственном звене — гранулоцитах — у подвергнутых тотальному облучению свиней. Кривую, отражающую наблюдения в течение 120 сут, можно разделить на три участка: 1) фазу дегенерации, характеризующуюся небольшим порогом и быстрым спадом; 2) фазу абортивного подъема с последующим еще большим спадом; 3) фазу восстановления до исходного уровня.
Особенности фазы дегенерации связаны с рассмотренными выше радиобиологическими закономерностями. Протяженность «плеча» определяется временем от последнего деления в пуле делящихся (созревающих) клеток костного мозга (см. рис. III.42) до выхода зрелых элементов в периферическую кровь. Отсюда следует, что созревание клеток, оставшихся жизнеспособными (по крайней мере, при среднелетальных дозах), происходит с нормальной скоростью. Наклон экспоненциального участка кривой определяется временем исчезновения нормальных клеток из периферической крови, что совпадает с быстрым и почти полным прекращением поступления нормальных клеток из костного мозга вследствие его глубокого опустошения.
Клетки, остающиеся в периферической крови, элиминируются с нормальной скоростью. С увеличением дозы облучения наклон этого участка кривой все более приближается к характеристикам исчезновения из крови нормальных клеток; при меньших дозах небольшое количество клеток продолжает выходить на периферию, имея различные повреждения, так как они — потомки не летально поврежденных делящихся и созревающих элементов. Следовательно, в фазе дегенерации в крови находятся только поврежденные клетки.
Фаза абортивного подъема позволяет организму жить в течение более длительного времени, чем можно было бы ожидать. Механизм абортивного подъема еще неясен. Наиболее вероятно, что он связан с размножением в разной степени поврежденных радиацией клеток пролиферативного (усиливающего) пула, обладающих ограниченной способностью к самоподдержанию, и отчасти полипотентных стволовых клеток. По степени повреждения клетки этих пулов могут полностью сохранить пролиферативную способность, иметь сниженные пролиферативные потенции или оказаться необратимо поврежденными.
Абортивный подъем вероятнее всего обеспечивается клетками со сниженной пролиферативной способностью, продолжающими деление еще некоторое время. Лишь, после того как ограниченный потенциал пролиферации этих клеток будет исчерпан (они сами и все их потомки погибнут), число зрелых элементов вновь снизится до минимального уровня. Окончательная регенерация в основном осуществляется клетками, сохранившими неизменной пролиферативную способность.
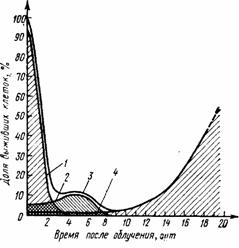
Рис. III.45. Объяснение абортивного подъема числа клеток (по В. Бонду. 1971):
1 — отмирающие (сильно поврежденные) клетки, быстро исчезающие из системы; 2 — «поврежденные» клетки (некоторое время пролиферируют, но через несколько делений вымирают и они и их потомство); 3 — общее количество клеток; 4 — выжившие клетки, способные пролиферировать неограниченно долго
На рис. III.45 схематически представлено изображение абортивного подъема, соответствующее возможному объяснению этого явления. Правильное понимание его механизмов весьма важно, ибо аналогичные явления встречаются и при облучении других клеточных популяций.
В частности, такую природу имеет временно продолжающийся рост опухолей после облучения в дозах, вызывающих гибель практически всей клеточной массы.
Фаза восстановления обеспечивается лишь небольшим количеством стволовых клеток, сохранившихся в костном мозге после глубокого начального опустошения и обладающих способностью к неограниченному размножению. Они должны не только продуцировать увеличенное количество подобных себе элементов, необходимых для репопулирования пула костномозговых стволовых клеток, но и производить дифференцирующиеся клетки, предназначенные для последующего созревания и поступления в кровь. Эти требования к небольшому числу оставшихся неповрежденными стволовых клеток объясняют причину задержки поступления зрелых элементов на периферию, несмотря на то, что в период резкой нейтропении в кровь поступает очень небольшое количество нейтрофилов. Только когда пул стволовых клеток существенно разовьется, ощутимая его часть может быть направлена на созревание. В результате в начале фазы восстановления число клеток крови увеличивается медленно, затем скорость выхода зрелых клеток в кровь нарастает, достигая нормальной величины в разгар восстановления.
Выше были рассмотрены основные радиационные синдромы и проанализирована цитокинетика поражений в критических системах клеточного обновления, из которых кроветворная система и кишечник - типичные примеры радиочувствительных тканей со свойственной им активностью физиологической пролиферации, а ЦНС — яркий пример непролиферирующих высокодифференцированных клеточных систем, являющихся, поэтому радиорезистентными.
Проведенный анализ позволяет следующим образом связать изменения, происходящие на уровне клеточных популяций, с исходом острого лучевого поражения после тотального облучения. Общая реакция млекопитающих как функция дозы и времени после облучения определяется четырьмя кардинальными параметрами клеточных популяций: величиной пула стволовых клеток, радиочувствительностью клеток и способностью их к восстановлению (определяющими характер дозовых кривых), клеточной пролиферацией и длительностью функционирования зрелых элементов.
С этих позиций достаточно надежно могут быть предсказаны события, которые произойдут при облучении различных областей тела, если известны клеточно-кинетические параметры облучаемых тканей, что весьма важно для оценки эффектов локального облучения, а также при планировании курса лучевой терапии опухолей и прогнозировании ее последствий.
Эндокринные железы. Железы внутренней секреции относят к радиорезистентным, хотя реакции эндокринной системы на общее облучение общеизвестны. Так же как в отношении нервной системы, очень трудно отдифференцировать, являются ли эти реакции результатом непосредственного повреждения эндокринных желез или отражением воздействия излучения на другие системы и весь организм. Можно предположить, что наблюдаемые после общего облучения нарушения баланса гормонов, особенно щитовидной железы, надпочечников и гонад, могут быть следствием реакции гипоталамо-гипофизарной системы, учитывая тесную взаимосвязь между тирео-, адрено- и гонадотропными факторами гипофиза.
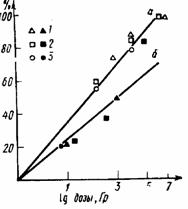
Рис. III.46. Зависимость числа клеток с хромосомными аберрациями (%) от дозы облучения:
а - в костном мозге мышей, б - в печени крыс; 1 - рентгеновское излучение 180 кВ, 2 - γ-излучение 60Со, 3 - протоны 600 МэВ
Следствием таких скрытых повреждений, возникающих в клетках любых малообновляющихся тканей (в отличие, например, от костного мозга), не элиминируемых в процессе деления, являются, в частности, и различные осложнения лучевой терапии. К их числу относятся миетиты, циститы, ректиты, пульмониты, перихондриты, поражения почек, сердца, печени, а возможно и злокачественные опухоли.
Сравнивая радиочувствительность отдельных тканей, следует применять только адекватные критерии. Например, для таких, казалось бы, разных по радиочувствительности органов, как костный мозг и печень, индукция хромосомных аберраций, возникающих под действием эквивалентных доз облучения, почти одинакова (рис. III.46). Если же в качестве показателя лучевого поражения использовать не непосредственные, а отдаленные последствия, то для этих органов они будут сильно различаться. Следовательно, понятие радиочувствительности применительно к той или иной ткани, органу или системе весьма относительно.
Сравнение радиочувствительности различных тканей свидетельствует о том, что радиочувствительность организма млекопитающих можно связать с радиочувствительностью костного мозга, ибо именно его аплазии, возникающей при тотальном облучении, вполне достаточно для гибели организма.
Под радиочувствительностью организма обычно понимают диапазон доз, вызывающих гибель животного при явлениях костномозгового синдрома.

Рис. III.47. Кривая смертности мышей, подвергнутых общему рентгеновскому облучению (каждая точка получена для 20 животных) (по И. Томсону, 1964)
Для количественного изучения радиочувствительности организма используют кривые выживания или смертности, при построении которых на оси абсцисс откладывают дозы облучения, а на оси ординат — процент гибели в определенного срока наблюдения (чаще всего за 30 сут).
(Сравнение критериев радиочувствительности клеточной популяции и животных показало, что параметры, обычно используемые для характеристики клеток (D 0 и n), можно формально применить и для целого организма. Однако в этом случае они теряют первоначальное смысловое значение. К этому заключению пришел В. Бонд в результате анализа кривой выживания, построенной по данным опытов с облучением 4300 мышей в дозах 2—34 Гр.)
Для всех видов млекопитающих такая кривая всегда имеет S-образную форму. Это объясняется тем, что при облучении в начальном диапазоне доз гибели не наблюдается (вплоть до так называемой «минимально летальной дозы» — на рис. III.47 это 4 Гр), а, начиная с некоторой дозы («минимальной абсолютно летальной дозы» — на рис. III.47 это 9 Гр) погибают все животные. Так как вся смертность регистрируется в интервале между этими дозами, на этом отрезке кривая круто поднимается вверх, приближаясь к 100%. В качестве примера на рис. III.47 приведена кривая смертности, характеризующая радиочувствительность мышей линии CF1.
По кривой выживания можно оценить дозы, вызывающие гибель любой доли животных. Неправомерно лишь согласно теории использовать термин ЛД100, ибо гибель конкретного животного зависит от вероятности многих событий, а потому в принципе выживание отдельных особей возможно и при «абсолютно летальных» дозах.
Наиболее пригодным и чаще всего употребляемым показателем радиочувствительности организма является ЛД50, которую легко определить по графику; видно (рис. III.47), что в этой области данные наиболее точны из-за большой крутизны кривой.
Из данных рис. III.47 видно, что, несмотря на большую статистическую нагруженность эксперимента (более 500 животных) наблюдается достаточно большой разброс значений выживаемости при одинаковых дозах облучения. Это определяется высокой вариабельностью индивидуальной радиочувствительности (даже для животных одной линии) и влиянием неконтролируемых условий эксперимента. Приведенный пример показывает, насколько весомым должен быть экспериментальный материал для того, чтобы сделать уверенное заключение о таком интегральном показателе, как радиочувствительность организма.
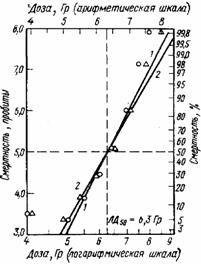
Рис. III.48. Обработка данных, приведенных на рис. III.47, в координатах пробит - логарифм дозы (кривая 1, кружки) и пробит - доза в арифметической шкале (кривая 2, треугольники):
как и на рис. III.47, данные но дозам, вызывающим гибель 50% животных, более точны, чем по дозам, вызывающим большую или меньшую смертность
Рис. III.48 иллюстрирует результат сравнительной обработки данных, приведенных на рис. III.47, в двух системах координат. Видно, что между установленными значениями ЛД50, разница весьма незначительна.
Из рассмотренных представлений о костном мозге как системе клеточного обновления, состояние которой определяет исход поражения в диапазоне среднелетальных доз, следовало ожидать, что общая радиочувствительность организма коррелирует с радиочувствительностью пула стволовых клеток и их способностью к репопуляции, ответственной за репопуляцию всей кроветворной системы.
В многочисленных исследованиях, проведенных разными авторами, это предположение не подтвердилось. В частности, получена достоверная количественная корреляция между характером восстановления пула стволовых клеток мышей и восстановлением организма, определяемым по критерию выживания (см. рис.?).
Подобная корреляция является не единственным доводом в пользу представлений о том, что выжившие после общего облучения стволовые клетки критических систем являются своеобразными детерминантами выживаемости организма. Так, показано, что лечебный эффект костного мозга или клеток других гемопоэтических органов при трансплантации их летально облученным животным полностью определяется содержанием в нем стволовых клеток. Например, для достижения одинакового с костным мозгом лечебного эффекта надо брать в 10 раз больше клеток селезенки, которые содержат в своей популяции в 10 раз меньше стволовых кроветворных клеток. Клетки лимфоузлов или тимуса, среди которых практически нет стволовых кроветворных клеток, неэффективны при лечении острого лучевого поражения.
Как показали Д. Тилл и Е. МакКуллох (1961), радиочувствительность элементов костного мозга, определяющих его терапевтическое действие, и радиочувствительность так называемых кроветворных колониеобразующих единиц (КОЕ), обладающих всеми свойствами стволовых кроветворных клеток, одинакова. Радиозащитное действие многих препаратов по тесту числа КОЕ и по 30-дневной выживаемости животных также довольно близко. Одинаковые изменения в выживаемости стволовых клеток и организма отмечены и при модификациях воздействия, например при изменении мощности дозы, фракционировании (см. рис.?), использовании излучений, различных по ЛПЭ.
Таким образом, клеточным субстратом, ответственным за выживание организма, является пул стволовых клеток системы клеточного обновления, критической в данном интервале доз.
Рассматривая с этих позиций наиболее вероятные причины вариабельности индивидуальной радиочувствительности животных, можно предположить, что они связаны либо со статистической вероятностью поражения, а, следовательно, и выживания большего или меньшего числа стволовых клеток, либо с различиями в их числе, либо, наконец, определяются различиями в собственной радиочувствительности стволовых клеток.
Кроме индивидуальных, существуют половые (самки, как правило, менее чувствительны к облучению) и возрастные различия в радиочувствительности организма.
На рис. III.49 приведены данные о ЛД50 у мышей в течение жизни; радиочувствительность в первые 2-3 недели после рождения наиболее высока, затем снижается, выходя на плато в половозрелом состоянии, и вновь повышается в последний период жизни.
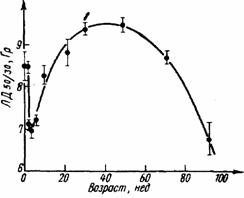
Рис. III.49. Зависимость величины ЛД50/50 от возраста мышей линии SAS/4 (по М. Кроссфилу и др., 1959)
Таблица 7. Величины среднелетальных доз при средней продолжительности жизни 30, 8, 5 и 2 дня для животных различных видов и человека (по В. Бонду и др., 1971)
| Объект исследования | Вид излучения и энергия, кэВ | Среднелетальные дозы облучения | |||
| ЛД50/20 | ЛД50/8 | ЛД50/5 | ЛД50/2 | ||
| Мышь | X[1], 200 | 6,4 | - | 12,5 | 180-400 |
| Мышь (стерильная) | X, 250 | 7.0 | — | — | |
| Крыса | X, 250 | 7,1 | - | 8,0 | 200-300 |
| Морская свинка | X, 200 | 4,5 | — | ||
| Хомяк | X, 200 | 6,1 | — | ||
| X, 250 | 8,6 | — | — | — | |
| Кролик | X, 250 | 7,5 | - | — | — |
| Козел | X, 200 | 2,4 | - | — | — |
| γ-Нейтронный источник | — | - | |||
| Свинья | X, 103 | 2,5 | - | - | |
| Осел | Х, 103 | 2,5 | — | — | — |
| γ-Нейтронный источник | 3,7 | — | — | — | |
| Собака | X, 250 | 2,5 | - | - | |
| Macaco mulatu | γ, 103 | - | - | ||
| Macaco rhesus | γ, 103 | - | - | ||
| Человек | γ-Излучение | 3,0 | - | - | - |
Таким образом, в основе различий в выраженности двух основных радиационных синдромов, вызванных редко- и плотно ионизирующим излучениями, в конечном счете, лежат свойственные стволовым клеткам критических систем различия в способности репарировать радиационные повреждения.
Функционирование соответствующих детерминантных клеточных элементов показано и в других системах клеточного обновления — коже, сперматогенном эпителии и в некоторых опухолях. Лучевая реакция этих систем, особенно на этапе восстановления популяции, во многом определяется фондом жизнеспособных стволовых клеток. Все это дает основание свести межвидовые и индивидуальные различия в радиочувствительности организма млекопитающих к особенностям кинетики клеточных популяций критических систем, детерминантами, поражения которых в основном являются соответствующие стволовые клетки.
На одном из недавних международных симпозиумов, специально посвященных сравнительной клеточной и видовой радиочувствительности было подчеркнуто, что пока еще не удается установить ясные и определенные причины различий в радиочувствительности, которая даже среди млекопитающих различается в 10 раз. (Последнее десятилетие не внесло ничего принципиально нового в этот вопрос). В заключительном слове крупнейшего специалиста в этой области В. Бонда были подчеркнуты три обстоятельства.
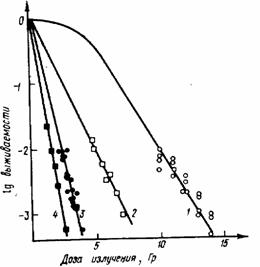
Рис. III.50. Кривые выживания стволовых клеток кишечника (1) и стволовых кроветворных клеток (2) мышей при γ-облучении; 3 и 4— то же, при облучении нейтронами (по А. Г. Коноплянникову. 1982)
- Необходимость тщательного изучения различий в размерах пулов клеток, кинетики и механизмов регуляции клеточной пролиферации у организмов различных видов, а также определения физиологических параметров, особенно длительности жизни зрелых функциональных клеток у облученных животных по сравнению с нормальными.
- Важность изучения возможной роли изменения кровеносных сосудов, стромы пролиферирующих органов, а также других соматических тканей, повреждения которых также могут приводить организм к гибели или способствовать ее наступлению.
- Важность учета пространственного распределения доз в тканях. Видимые различия в радиочувствительности могут быть просто результатом различий дозиметрических параметров облучения (т.е. ситуации, приведенной в табл. 6).
Нельзя потушить пламя, если лить воду только в середину огня.
Г. Ришар
Date: 2016-05-25; view: 1365; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |