
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Количественная характеристика электролиза выражается двумя законами Фарадея
1. Масса вещества, выделяющегося на электродах, прямо пропорциональна количеству прошедшего через электролит электричества.
2. При электролизе различных химических соединений равные количества электричества выделяют на электродах массы веществ, пропорциональные молярным массам их эквивалентов.
Согласно этим законам:
1. m = Kэ Q или m = Kэ I t, где m – масса выделившегося вещества
Q – количество электричества в кулонах / Кл /
I - сила тока в амперах / А /
t - время в секундах / с /
Kэ - коэффициент пропорциональности, называемый электрохимическим эквивалентом
Если I = 1 A, t = 1 c и, следовательно Q = 1 Кл, то m = Kэ , т.е. электрохимический эквивалент – это масса вещества, выделившегося на электроде током силой в 1 А в течение 1 с или количеством вещества 1 Кл,
Kэ = 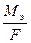 , тогда m =
, тогда m = 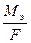 I t, а Мэ =
I t, а Мэ = 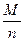 , где М- молярная масса вещества, а n – число электронов, перемещаемых при окислении или восстановлении
, где М- молярная масса вещества, а n – число электронов, перемещаемых при окислении или восстановлении
2. 96500 Кл или 26,8 А / ампер-час / выделяют на электродах молярную массу эквивалента данного вещества. Это количество электричества называют числом или постоянной Фарадея F / Кл/моль или А час/ моль /
Вследствие параллельных побочных процессов масса вещества, получаемого при электролизе, оказывается меньше той, которая соответствует количеству прошедшего электричества. Отношение массы реально выделенного вещества на электроде к теоретической и умноженной на 100, называют выходом по току:
Вт = 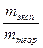 100. Так как m = Kэ I t или m =
100. Так как m = Kэ I t или m = 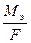 I t; Вт =
I t; Вт =  100%
100%
Date: 2016-01-20; view: 608; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |