
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Идеальный газ. Законы идеального газа
Идеальный газ – это газ точечных молекул, взаимодействующих по законам упругого
столкновения, то есть между его молекулами отсутствуют силы взаимодействия на расстоянии.
В теплоэнергетических установках зачастую технические расчеты в первом приближении можно проводить на основе закономерностей, присущих идеальному газу.
Уравнение состояния идеального газа (уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. pVм=RT,
по другому можно pV=vRT
p=nKT, где n=N/V - концентрация атомов, k-постоянная Больцмана=1.38*10-23Дж/К
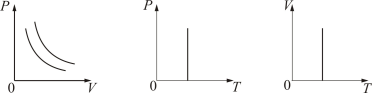
1. Изохорический процесс. Закон Шарля. V = const.
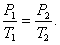
|
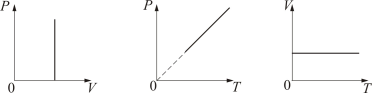
2. Изобарический процесс. Закон Гей-Люссака. Р = const.
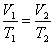
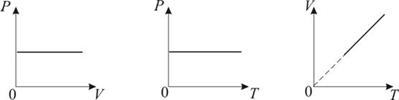
3. Изотермический процесс. Закон Бойля – Мариотта. T = const.
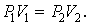
4. Адиабатический процесс (изоэнтропийный):
Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой.
5. Политропический процесс. Процесс, при котором теплоёмкость газа остаётся постоянной. Политропический процесс – общий случай всех перечисленных выше процессов.
6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA =6,02·1023 молекул (число Авогадро).
7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов:
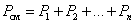
| (1.4.6) |
Парциальное давление Pn – давление, которое оказывал бы данный газ, если бы он один занимал весь объем.
При 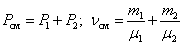 , давление смеси газов:
, давление смеси газов:
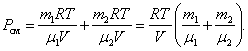
| (1.4.7) |
8. Объединённый газовый закон (Закон Клапейрона).
В соответствии с законами Бойля – Мариотта (1.4.5) и Гей-Люссака (1.4.3) можно сделать заключение, что для данной массы газа
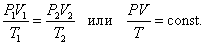
|
Date: 2015-09-24; view: 754; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |