
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изомерия
Соответственно, для алкинов характерны 2 вида изомерии:
1. Структурная — изомерия положения тройной связи и изомерия радикалов
2. Межклассовая — алкины изомерны акладиенам.
Химические свойства алкинов:
1. Тройная связь, как и двойная, все присоединяет, разрывается, образует двойную связь, если реагент дан в избытке, то реакция может идти до образования одинарной связи:
· галогенирование,
· гидрогалогенирование,
· гидрирование:
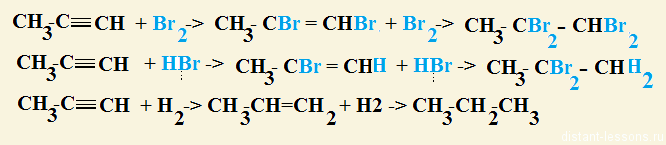
2. Гидратация — взаимодействие с водой — реакция Кучерова:
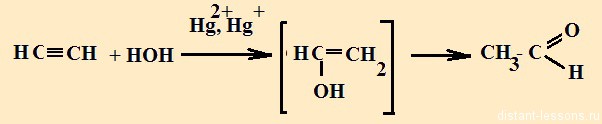
3. Качественные реакции алкинов:
Ацетилениды серебра и меди (I) легко образуются и выпадают в осадок при пропускании ацетилена через аммиачный раствор оксида серебра или хлорида меди (I). Эта реакция служит для обнаружения алкинов с тройной связью на конце цепи:
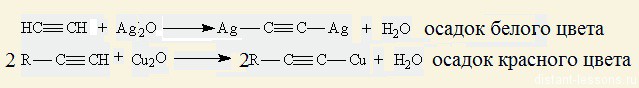
4. Реакции окисления:
Алкины окисляются различными окислителями, в частности перманганатом калия. При этом раствор перманганата калия обесцвечивается, что служит указанием на наличие тройной связи. При окислении обычно происходит расщепление тройной связи и образуются карбоновые кислоты, перманганат восстанавливается до Mn(2+) — в кислой среде, MnO2 — в щелочной:
С4H6 + [O] → 2CH3COOH
5. Реакции горения: как и все органические вещества, алкины сгорают с образованием углекислого газа и воды:
СnH2n-2 + (3n-1)\2 O2 → nCO2 + (n-1) H2O
Здесь записано уравнение в общем виде, т.к. во многих задачах требуется определить состав углеводорода — в таких случаях любые реакции лучше записывать в таком — общем виде.
Получение алкинов:
· Из неорганических соединений: CaC2 + H2O → 2Ca(OH)2 + C2H2
· дегидрогалогенирование: СH3-СHBr2 +2KOH (этанол, t) →C2H2 + 2KBr + 2H2O
Алкадиены
Алкадиены — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода и соответствующие общей формуле СnН2n-2.
В зависимости от взаимного расположения двойных связей различают три вида диенов:
• алкадиены с кумулированным расположением двойных связей
СН2=С=СН2
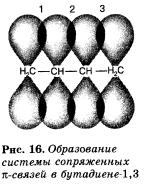
• алкадиены с сопряженными двойными связями
CH2=CH—CH=CH2
• алкадиены с изолированными двойными связями
CH2=CH—CH2—CH=CH2
Изомерия и номенклатура
Для алкадиенов характерна как структурная изомерия, так и цис-транс-изомерия. Структурная изомерия:
• изомерия углеродного скелета:
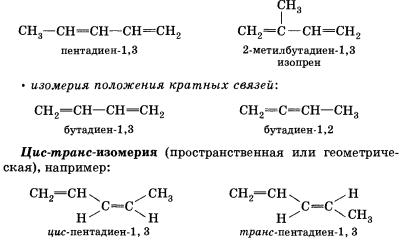
· Межклассовая (Алкадиены изомерны соединениям классов алкинов и циклоалкенов (см. «Алкины»).
При формировании названия алкадиена указывают номера двойных связей. Главная цепь должна обязательно содержать обе кратные связи.
Получение
1. Метод Лебедева. В 1932 г. в нашей стране было налажено производство бутадиена из этилового спирта методом, разработанным С. В. Лебедевым. В основе метода лежит реакция
425 °С, Аl2O3, ZnO
2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2
Серге́й Васи́льевич Ле́бедев
(1874-1934)

Советский химик, академик. Основные научные исследования посвящены полимеризации, изомеризации и гидрогенизации непредельных углеводородов. Получил (1928) синтетический каучук полимеризацией 1,3-бутадиена под действием натрия.
Этиловый спирт одновременно претерпевает и дегидратацию, и дегидрирование.
2. Способ дегидрирования. Одним из самых распространенных способов получения бутадиена-1,3 является двухстадийное каталитическое дегидрирование н -бутана:
СН3—СН2—СН2—СН3 —> CH2=CH—СН=СН2 + 2Н2
На первой стадии этого процесса образуется как бутен-1, так и бутен-2.
3. Способ дегидрогалогенирования.
При действии на дибромалканы спиртового раствора щелочи происходит отщепление двух молекул галогеноводорода и образование двух двойных связей:
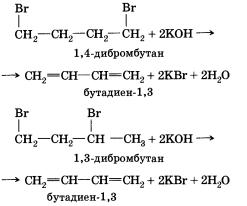
Существенным является расположение галогенов в молекуле дига-логенида. Так, например, в случае 2,3-дибромбутана или 2,2-ди-бромпропана образуются соответствующие алкины (см. § 13 «Алкины»).
Физические свойства
В обычных условиях пропадиен-1,2, бутадиен-1,3 — газы, 2-метилбутадиен-1,3 — летучая жидкость. Алкадиены с изолированными двойными связями (простейший из них — пен-тадиен-1,4) — жидкости. Высшие диены — твердые вещества.
Химические свойства
свойства алкадиенов с изолированными двойными связями мало отличаются от свойств алкенов. Алкадиены с сопряженными связями обладают некоторыми особенностями.
1. Реакции присоединения. Алкадиены способны присоединять водород, галогены, галогеноводороды.
Особенностью присоединения к алкадиенам с сопряженными двойными связями является способность присоединять молекулы как в положения 1 и 2 (1,2-присоединение), так и в положения 1 и 4 (1,4-присоединение):
Вr Вr
| |
СН2=СН—СН=СН2 + Вг2 —> CH2—CH—CH=CH2
1,2-присоединение
Вг Вг
| l
CH2=CH—СН=СН2 + Вг2 —> CH2—CH=CH—CH2
1,4-присоединение
Соотношение продуктов зависит от условий и способа проведения соответствующих реакций.
2. Реакции полимеризации. Важнейшим свойством диенов является способность полимеризоваться под воздействием катионов или свободных радикалов. Полимеризация этих соединений является основой получения синтетических каучуков. Полимеризация сопряженных диенов протекает как 1,4-присоединение.
В этом случае двойная связь оказывается центральной в элементарном звене, а элементарное звено, в свою очередь, может принимать как цис-, так и тракс-конфигурацию:

Натуральный и синтетический каучуки. Резина
До конца 1930-х гг. в промышленности использовали натуральный каучук, выделяемый из млечного сока (латекса) некоторых растений-каучуконосов. Наиболее ценным каучуконосом является гевея, растущая в Латинской Америке. Исследования показали, что натуральный каучук представляет собой цис-полиизопрен, т. е. полимер, элементарные звенья которого соответствуют изопрену (2-метилбутадиену-1,3) и находятся в цис-конфигурации.
Каучук, в котором все элементарные звенья находятся или в цис-, или в транс-конфигурации, называется стереорегулярным.
Обнаружено, что при нагревании каучука с серой (до 8%) образуется резина — эластичный материал, технические свойства которого гораздо лучше, чем у каучука. При нагревании с серой (вулканизации) происходит сшивание полимерных цепей за счет сульфидных мостиков, что приводит к увеличению прочности, устойчивости к истиранию, к действию органических растворителей и других веществ.
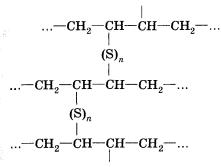
Впервые технологически удобный способ синтеза полибутадиенового каучука был разработан русским химиком С. В. Лебедевым. В его основе лежала полимеризация бутадиена-1,3 с использованием катализатора — металлического натрия.
Арены
Арены – это непредельные углеводороды, которые можно рассматривать как производные простейшего из них — бензола С 6Н 6. Общая формула углеводородов гомологического ряда бензола С nН 2n- 6(при n >= 6).
В молекуле бензола все атомы углерода находятся в sр 2-гибридизации, каждый атом углерода соединен в одной плоскостиперпендикулярно г.), а единая шестицентровая (С 6)
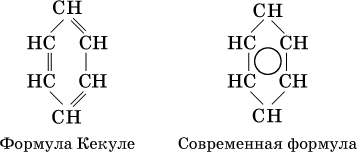
Формула Кекуле часто применяется в тех случаях, когда необходимо более наглядно представить протекание реакции с участием бензольного кольца С 6; его изображение:
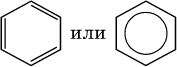
В обеих формулах атомы С кольца и не участвующие в реакции атомы Н опускаются (для краткости). Некоторые простейшие гомологи бензола:
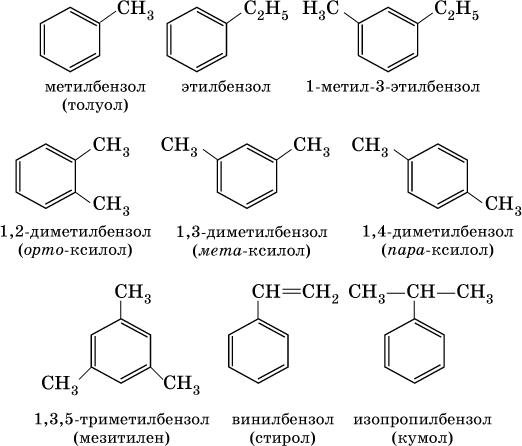
Радикал бензола С 6Н 5называется фенил, радикал толуола С 6Н 5СН 2— бензил.
Бензол и его ближайшие гомологи – жидкости без цвета, но с характерным запахом, имеют широкий интервал жидкого состояния. Практически не растворяются в воде, но хорошо смешиваются между собой и с другими органическими растворителями. Пар бензола сильно ядовит.
Несмотря на формальную непредельность, бензол отличается высокой устойчивостью к нагреванию и окислению (в гомологах бензола окисляется только боковая цепь). Характерными для бензола являются реакции замещения:
а) нитрование в присутствии концентрированной серной кислоты на холоду:
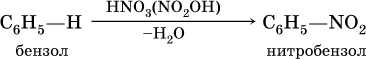
б) галогенирование в присутствии галогенидов железа (III):
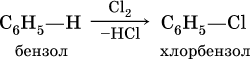
в) алкилирование в присутствии хлорида алюминия:
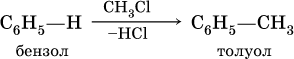
Особый характер ненасыщенности бензола и его гомологов иллюстрируется этими химическими свойствами и называется «ароматическим» характером.
В производных бензола атом или группа, заместившие водород кольца, и само бензольное кольцо влияют друг на друга. По характеру влияния различают:
1) заместители I рода – CI, Br, I, СН 3, С nН 2n+1, ОН и NH 2. Они облегчают реакции дальнейшего замещения и направляют второй заместитель по отношению к себе в орто- (о-, или 2-) положение и в пара- (п -, или 4-) положение [для запоминания: орто – около, пара – против], например:
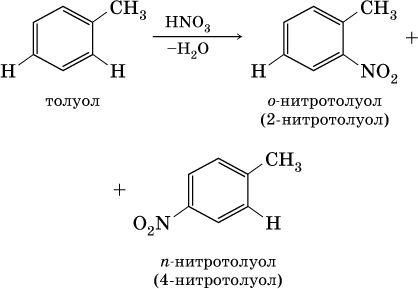
2) заместители II рода – NO 2, С(Н)O, СООН и CN. Они затрудняют реакции дальнейшего замещения и направляют второй заместитель в мета- (м -, или 3-) положение, например:
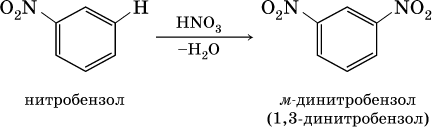
Ранее уже отмечалось, что бензол стоек к окислению даже при действии сильных окислителей. Гомологи бензола с одним боковым радикалом вступают в реакции окисления только за счет радикала; при этом, какова бы ни была его длина, отщепляется вся цепь, кроме ближайшего к кольцу атома углерода (он создает карбоксильную группу):
В жестких условиях бензол вступает в реакции присоединения:
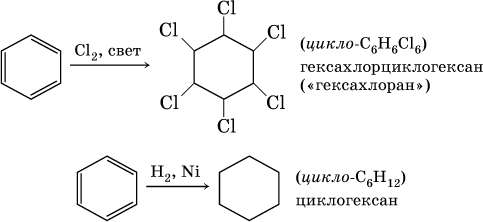
Стирол C 6H 5—CH=CH 2, как этилен, легко полимеризуется:
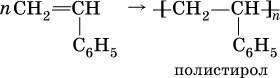
Полистирол – термопластичная пластмасса (термопласт), прозрачный материал, размягчающийся при температуре выше 80 °C. Используется для изготовления изоляции электропроводов, посуды разового употребления, упаковочной массы (пенопласт).
Получение аренов – ароматизация алифатических и алициклических углеводородов, содержащихся в нефтяных или буроугольных бензиновых фракциях:
1) дегидрирование:

2) дегидроциклизация:
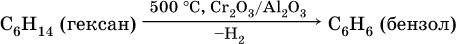
3) тримеризация ацетилена (устаревший способ):
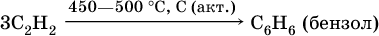
Бензол и его гомологи используются в качестве малополярных растворителей (для каучука, лаковых смол, полимеров), сырье в органическом синтезе.
Date: 2015-08-22; view: 883; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |