
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Общие пути катаболизма аминокислот. Токсичность и пути обезвреживание аммиака
1. Источники аминокислот в организме человека. Пути использования аминокислот в тканях. Общие пути катаболизма аминокислот.
Организм может получить аминокислоты из двух источников.
Из внешней среды (экзогенные источники).
1. Это белки и аминокислоты пищи.
Или из эндогенных источников. Гидролаз собственных белков различных органов и тканей под влиянием тканевых гидролаз. Либо путем биосинтеза заменимых аминокислот.
Пути использования:
1. Главным образом для биосинтеза простых и сложных белков, общее содержания которых в организме около 15 кг. Например: для биосинтеза гема, ДНК, РНК, глутиона и др.;
2. Для биосинтеза БАА (биологически активных аминов).
3. Биосинтез углеводов. Глюконеогенез – это как бы альтернативный источник энергии.
4. Биосинтез ВЖК и липидов.
Общие пути катаболизма аминокислот в тканях идут в три этапа:
1. Декарбоксилирование и образование БАА.
2. Дезаминирования и трансаминирование.
3. Окисление углеводородного скелета до СО2 и Н2О и другие превращения.
2. Декарбоксилирование аминокислот: ферменты, коферменты, продукты. Биогенные амины (гистамин, триптамин, серотонин, ГАМК, катехоламины, холин и проч.).
Декарбоксилирование аминокислот – это процесс окислительного декарбоксилирования (удаление СО2) из аминокислот. Ферменты - декарбоксилазы. Их простетическая группа представлена пиридоксальфосфатом – это активная форма витамина В6.
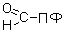
В реакциях декарбоксилирования участвует альдегидная группа пиридоксальфосфата
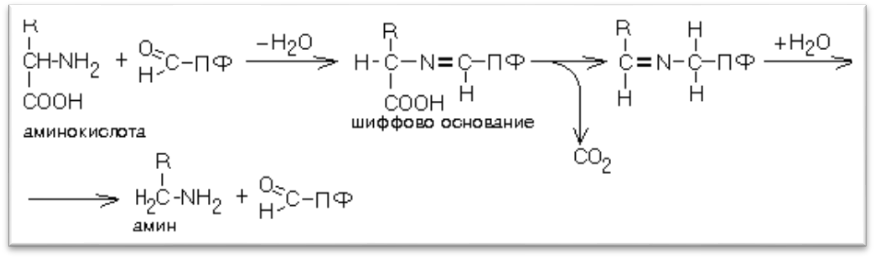 .
.
Аминокислота соединяется с активным центром фосфата, в состав которого входит альдегидная группа ПФ. Образуются Шиффовы основания (альдимины и кетимины). В результате СООН- группа становиться лабильной и отщепляется в виде СО2. Далее происходит гидролиз до соответствующего амина (БАА). Эта реакция необратима. Отнятие СО2 происходит без окисления.
Каждый фермент имеет свое название, в зависимости от реакции в которой он участвует (субстратная специфичность декарбоксилаз).
Триптофан (фермент – триптафандекарбоксилаза) à триптамин. Повышает тонус сосудов;
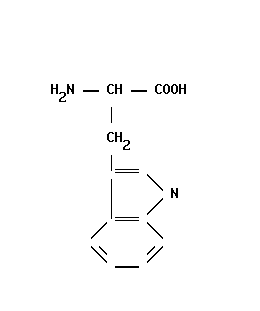
5-окситриптофан (фермент – 5-окситриптафандекарбоксилаза) à серотонин (нейромедиатор) – участвует в регуляции АД, температуры тела, дыхания, почечной фильтрации, перистальтики кишечник и др.
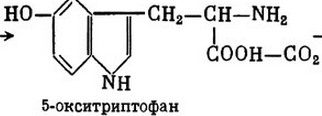
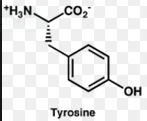
Тирозин à катехоламины (адреналин, дофамин, норадреналин). Участвуют в реакциях мобилизации из депо гликогена и липидов, повышают тонус сосудов периферических сосудов, являются медиаторами проведения нервных импульсов в пре-и постсинаптическую мембрану.
Гистидин (фермент – гистидиндекарбоксилаза) à гистамин. Нейромедиатор, стимулирует выделение желудочного сока, повышает проницаемость капилляров, увеличивая их проницаемость (при этом будут наблюдаться отёки), снижает АД, сокращает гладкую мускулатуру легких (вызывая удушье), участвует в развитии реакции воспаления, играет важную роль в развитии аллергических реакций и т.д.
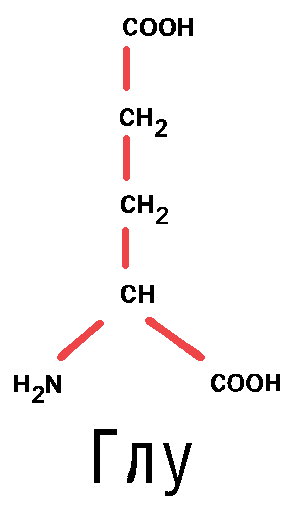
Глутаминовая кислота (фермент – глутаматдекарбоксилаза) à гамма-аминомасляная кислота. Является медиатором тормозным импульсов в нервной системе. ГАМК и её аналоги применяются в медицине как нейротропные вещества для лечения эпилепсии и других заболеваний. Понижает активность ЦНС.
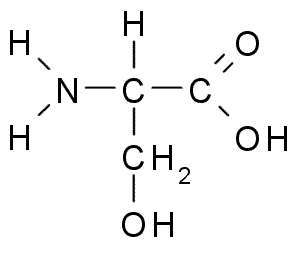
Серин à коламин à холин – участвует в биосинтезе фосфолипидов и ацетилхолина.
Инактивация биогенных аминов.
Если биогенные амины обладают высокой биологической функцией, то они должны быстро разрушаться после выполнения своей функции.
В организме имеются механизмы, позволяющие разрушать БАА.
Механизмы инактивации – окисление под действием оксидаз с отщеплением аминогруппы. Метилирование аминов. В результате исчезает биологическая активность амина.

Оксидазы отнимают два протона и два электрона и передают их сразу на кислород. Образуется перекись водорода, а амин превращается в имин. Этот имин легко гидролизуется без участия фермента и превращается в альдегид. Простетической группой ферментов оксидаз является ФАД или ФМН, т.е. они являются флавопротеинами.
*Биогенные амины инактивируются под действием окислительных ФАД–зависимых ферментов - моноамино–оксидаз (МАО). Происходит окислительное дезаминирование аминов до альдегидов.
Вторая реакция (гидролиз) необратима. Образовавшийся в итоге альдегид легко окисляется до карбоновой кислоты, которая распадается до СО2 и H2O. МАО в клетке больше, чем ДАО.
Аминокислоты декарбоксилируются в цитоплазме, а окисление аминов происходит в наружной мембране митохондрий. Поскольку реакция декарбоксилирования аминокислот и разрушение биогенных аминов происходят не одновременно, то биогенные амины могут некоторое время существовать и выполнять свою биологическую функцию
Date: 2015-08-06; view: 1199; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |