
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Механизм возникновения электродного потенциала
Электродные потенциалы
Если пластинку металла, например цинка, погрузить в воду, то расположенные на поверхности катионы металла гидратируются полярными молекулами воды, при этом выделяется энергия гидратации, которая идет на разрыв связи ионов в кристаллической решетке металла. Часть ионов цинка, расположенных на поверхности, перейдет в воду. Сама пластинка при этом зарядится отрицательно. Ионы Zn2+ из раствора электростатически притягиваются к пластинке, образуется двойной электрический слой (ДЭС). (рис.1):
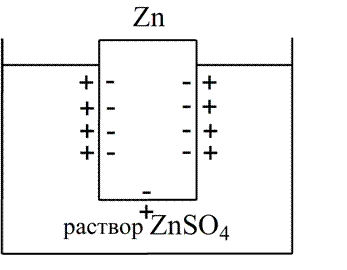 |
Если же металл помещен в раствор собственной соли, например, ZnSO4, то в раствор поступит меньше ионов Zn2+ из металла.
Пластинка металла заряжается отрицательно, если энергия гидратации больше, чем энергия кристаллической решетки (учебник Ершова, с.469; учебник Ленского, с.234).
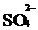 Если же медную пластинку погрузить в раствор CuSO4, то ионы Сu2+ осаждаются на ней. Пластинка заряжается положительно, в растворе создается избыток анионов. Ионы электростатически притягиваются к пластинке, образуется двойной электрический слой.
Если же медную пластинку погрузить в раствор CuSO4, то ионы Сu2+ осаждаются на ней. Пластинка заряжается положительно, в растворе создается избыток анионов. Ионы электростатически притягиваются к пластинке, образуется двойной электрический слой.
 (рис.2)
(рис.2)
Металлы, стоящие в электрохимическом ряду напряжений правее водорода, заряжаются положительно, левее водорода - отрицательно.
Система, состоящая из двух токопроводящих тел: проводников 1 - го рода (металлов), погруженных е растворы собственных солей (проводник 2-го рода) — называется электродом.
Условное обозначение электрода в общем виде Me | Меn+. Вертикальная черта показывает границу раздела между проводником 1-го рода и проводником 2-го рода.
Условное обозначение цинкового электрода: Zn | ZnSO4 или Zn | Zn2+; медного электрода: Си | CuSO4 или Сu | Сu2+.
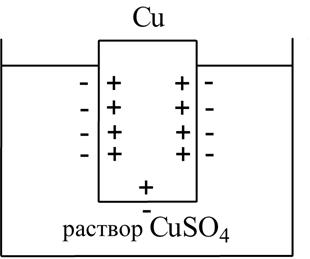
Скачок потенциала, возникающий на границе раздела металл-раствор его соли, называется электродным потенциалом.
Он обозначается 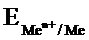 , например:
, например: 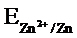 .
.
Гидратированные катионыметалла в растворе, одноименные с металлом электрода, влияющие на величину его потенциала, называются потенциалопределяющими.
Чтобы можно было сравнить значения электродных потенциалов различных металлов, следует работать в стандартных условиях: Т = 298 К;
концентрация ионов 1 моль/л; Р = 1 атм.
Date: 2015-07-17; view: 1374; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |