
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Примеры решения задач. ЗАДАЧА 6.1.1 Найти эффективный диаметр молекулы азота, если для азота критическая температура –147,10С; критическое давление 3,5·105 Па
ЗАДАЧА 6.1.1 Найти эффективный диаметр молекулы азота, если для азота критическая температура –147,10С; критическое давление 3,5·105 Па.
Дано: tкр = –147,10С; ркр =33,5·105 Па.
Найти: s -?
Решение
Постоянная b в уравнении Ван-дер-Ваальса приближенно равна учетверенному собственному объему молекул. Поэтому для одного моля газа имеем
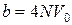 , (16)
, (16)
где N – число Авогадро;
V0 – объем одной молекулы, который равен 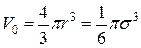 ,
,
где s -эффективный диаметр молекулы азота.
Подставляя значения V0 в (16), получим, что постоянная b равна 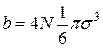 .
.
Откуда  .
.
Чтобы определить b, воспользуемся уравнениями, связывающими поправки Ван-дер-Ваальса с критической температурой и давлением
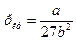 ;
; 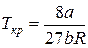 .
.
Решая эти уравнения относительно b, получим
.
Подставим значение b в уравнение для эффективного диаметра молекулы, получим
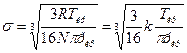 , (17)
, (17)
где 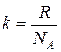 - постоянная Больцмана.
- постоянная Больцмана.
Подставляя численные значения в (17)в системе СИ, найдем
s» 3.12·10-10 м.
ЗАДАЧА 6.1.2. Моль кислорода расширяется адиабатически в пустоту, в результате чего объём газа увеличивается от 1 л до 10 л. Определить приращение температуры газа.
Дано:V1 = 1 л=10-3 м; V2 = 10 л= 10 -2м 3; а =0,136 Па·м6/моль2.
Найти: 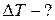
Решение
Расширяясь в пустоту, газ работы не совершает (А = 0). При адиабатическом процессе 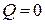 . Тогда согласно первому началу термодинамики
. Тогда согласно первому началу термодинамики 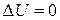 . Внутренняя энергия моля Ван-дер-Ваальсовского газа с двухатомными жёсткими молекулами определяется выражением:
. Внутренняя энергия моля Ван-дер-Ваальсовского газа с двухатомными жёсткими молекулами определяется выражением:
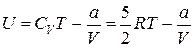 .
.
Приравнивая значения этого выражения для начального и конечного состояний газа, получим, что
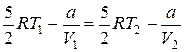 , откуда
, откуда 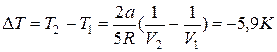 .
.
Газ охладился на 5,9 К.
6.2 Задачи к теме «Реальные газы»
458. Вычислить критическую температуру Т кр: 1) кислорода, 2) воды. Поправки Ван-дер-Ваальса:
1) для кислорода а = 0,136 Н×м4/моль2, в = 3,17×10-5 м3/моль;
2) для воды: а = 0,545 Н×м4/моль2, в = 3,04×10-5 м3/моль.
459. Найти критический объем Vкр кислорода массой m=0,5 кг. Поправки
Ван-дер-Ваальса: для кислорода а=0,163 Н∙м4/моль2, в=3,17∙10-5 м3/моль.
460. В баллоне емкостью 4 л находится кислород массой m=0,15 кг при температуре 300К. Определить отношение внутреннего давления р1 к давлению газа р на стенки сосуда. Поправки Ван-дер-Ваальса:
а=0,136 Н∙м4/моль2, в=3,04∙10-5 м3/моль.
461. В баллоне емкостью V=8 л находится кислород массой 3 кг при температуре Т=300 К. Найти, какую часть емкости занимает собственный объем молекул газа. Поправки Ван-дер-Ваальса:
а=0,136 Н∙м4/моль2, в=3,17∙10-5м3/моль.
462. Вычислить критическое давление Ркр : 1) кислорода; 2) воды. Поправки Ван-дер-Ваальса:
1) для кислорода: а=0,136 Н· м 4 /моль2, в=3,17· 10-5 м3 /моль;
2) для воды: а=0,545 Н·м4 /моль2, в=3,04·10-5 м3/моль.
463. В сосуде вместимостью V=10 л находится азот массой = 0,156 кг. Определить: 1) внутреннее давление р1 ’ газа; 2) собственный объем V 1 молекул. Рассматривать как идеальный газ. Поправки Ван-дер-Ваальса: а=0,135 Н∙м4/моль2, в=3,86∙10-5 м3/моль.
464. Доказать, что теплоемкость Cv газа, подчиняющего уравнению Ван-дер-Ваальса, не зависит от объема, а является функцией только температуры. Найти выражение для внутренней энергии газа Ван-дер-Ваальса, теплоемкость которого не зависит от температуры.
465. Моль азота расширяется в пустоту от начального объема 1 л до конечного 10 л.Найти понижение температуры Т при таком процессе, если постоянная a в уравнении Ван-дер-Ваальса для азота равна
1,36∙106 атм∙см6 / моль2.
466. Азот при критической температуре Tкр=147°С имеет критический объем Vкр=0,12 л/моль. Считая, что азот подчиняется уравнению Ван-дер-Ваальса, найти понижение температуры 7г азота при расширении в пустоту объема V1=5 л до объема V2 =50 л.
467. Моль кислорода расширяется адиабатический в пустоту, в результате чего объём газа увеличивается от 1 л до 10 л. Определить приращение температуры газа.
468. Объем 1г азота увеличивается от 1 л до 5 л. Рассматривая газ как реальный, найти работу внутренних сил при этом расширении.
469. В баллоне емкостью 8 л находится 0,3 кг кислорода при температуре 27˚С. Определить: какую часть объема сосуда составляет собственный объем молекул; какую часть давления газа на стенки сосуда составляет внутреннее давление, обусловленное силами притяжений молекул.
470. Как изменилось бы давление газа в сосуде, если бы внезапно силы притяжения между молекулами исчезли при неизменной температуре?
471. Какое количество тепла надо подвести к одному молю газа Ван-дер-Ваальса, чтобы при расширении в пустоту от объема V1 до объема V2 его температура не изменилась?
472. Найти эффективный диаметр молекулы азота, если для азота критическая температура -147,1 0С, критическое давления 33,5∙105 Па.
473. Найти постоянные уравнения Ван-дер-Ваальса для азота, если tкр азота равна -146˚С, pкр=33 атм.
474. Найти критическую плотность воды, если критическое давление для воды ркр=195 атм, а критическая температура Tкр=374˚С, предполагая, что вода подчиняется уравнению Ван-дер-Ваальса.
475. Принимая постоянную a Ван-дер-Ваальса для воды равной 5,47∙106атм∙см6/моль2, найти внутреннее давление воды p.
476. Имеется три непрозрачных цилиндра, закрытых подвижными поршнями. Известно, что в первом цилиндре находится газ при температуре выше критической, во втором – насыщенный пар, а в третьем ненасыщенный пар. Как определить, что находится в каждом из цилиндров?
477. Моль азота охлаждается до -100 ˚С. Определить давление, оказываемое газом на стенки сосуда, если занимаемый газом объем 0,100 л. Сравнить p с pид , которое имел бы азот, если бы сохранил при рассматриваемых условиях свойства идеального газа.
478. Два сосуда с объемами V1 и V2 соединены трубкой с краном. В каждом из них при закрытом кране находится по одному молю одного и того же газа, подчиняющегося уравнению Ван-дер-Ваальса. До открытия крана температура газа в обоих сосудах была одинакова и равна T. Нагреется или охладится газ, если открыть кран? На сколько при этом изменится температура газа? Определить давление газа после открытия крана. Стенки сосуда и соединяющей их трубки считать адиабатическими, а теплоемкость Cv – не зависящей от температуры.
479. Два баллона с объемами V1=V2=V=1 л соединены трубкой с краном. В объеме V1 находится воздух под атмосферным давлением, а объем V2 откачен до предельного вакуума. Считая, что воздух подчиняется уравнению Ван-дер-Ваальса, а стенки баллонов и трубки адиабатические, определить, на сколько изменится температура газа после открытия крана. Начальная температура T=290 K, для воздуха a=1,39·106 атм·см6/моль2.
480. Критическая температура углекислого газа СО2 равна 31˚С, критическое давление 73 атм. Определить критический объем Vкр моля СО2.
481. Поправки для воды в уравнении Ван-дер-Ваальса равны
a=0,566 H×м4/моль2, b=3,06×10-5 м3/моль. Определить критический объем для 1 кг воды.
482. Найти критические параметры неона, если его постоянные в уравнении Ван-дер-Ваальса a=0,209 H×м4/моль2, b=1,7×10-5м3/моль.
483. Азот массой 14 кг занимает объем 0,5 м3 при температуре 0˚С. Пользуясь уравнением Ван-дер-Ваальса, найти, на сколько нужно изменить температуру газа, чтобы его давление увеличилось вдвое.
484. В сосуде, объем которого 10 л, находится 360 г водяного пара при температуре 470 К. Вычислить давление пара, используя уравнение Ван-дер-Ваальса.
485. Определить эффективный диаметр молекулы газа, для которого критическая температура равна 282,7 К, поправка в уравнении Ван-дер-Ваальса: a=45,3×10-2 H×м4/моль2.
486. По уравнению Ван-дер-Ваальса определить давление, под которым находится 1 моль азота в сосуде объемом 2,5 м3, если его температура 310 К.
487. Найти постоянные в уравнении Ван-дер-Ваальса для углекислого газа, если критическая температура 304 К, а критическое давление 7370 кПа.
Date: 2015-07-17; view: 8163; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |