
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Групповой реагент, общие и фармакопейные реакции катионов III аналитической группы.
БИЛЕТ №30
1.Реакция идёт по уравнению:4NH3(Г)+5O2(Г)=> 4NO(Г)+6H2O(ж)
Как изменится скорость реакции если увеличить давление в 2 раза?
Согласно закону действующих масс начальная скорость реакции равна:
V₁ = K ·C4(NH4) · C5(O2)
После увеличения давления:
V2 = K [2C(NH4)]4 · [2C(O₂)]⁵
 =
= 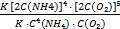 = 512
= 512
Ответ: в 512 раз
2.Напишите характерные реакции на ион B4O72-.
Окрашивание пламени газовой горелки сложными эфирами борной кислоты (фармакопейный тест). Борат-ионы или борная кислота образуют с этанолом C2H5OH в присутствии серной кислоты сложный этиловый эфир борной кислоты (C2H5O)3B, который окрашивает пламя в зеленый цвет. Реакцию образования сложных эфиров борной кислоты можно описать схемой:
B4O72- + 2H+ + 5H2O = 4H3BO3
H3BO3 + 3 C2H5OH = (C2H5O)3B + 3H2O.
Групповой реагент, общие и фармакопейные реакции катионов III аналитической группы.
Групповым реагентом на катионы третьей аналитической группы является раствор серной кислоты.
Реакции катиона бария Ba2+
1. Реакция окрашивания пламени
Летучие соли бария окрашивают пламя спиртовки или горелки в желто-зеленый цвет. Реакция является фармакопейной.
Разбавленная серная кислота H2SO4 и растворимые сульфаты
Выделяют даже из очень разбавленных растворов осадок сульфата бария:
BaCl2 + H2SO4 = Ba2SO4 ↓ + 2HCl
Ba2+ + SO42- = BaSO4 ↓
Осадок не растворяется в кислотах и щелочах.
Карбонат аммония (NH4)2CO3 или другой растворимый карбонат с солями
бария дает осадок карбоната бария:
BaCl2 + (NH4)2CO3 = BaCO3 ↓ + 2NH4Cl
Ba2+ + CO32+ = BaCO3↓
Осадок растворим в разбавленных минеральных кислотах и в уксусной кислоте. Осаждение следует вести в слабощелочной среде, лучше в аммиачной, т.к. в кислотах он растворим.
Хромат калия K2CrO4 или натрия Na2CrO4 осаждает из нейтральных или уксусно-кислых растворов бариевой соли хромат бария желтого цвета:
BaCl2 + K2CrO4 = BaCrO4 ↓ + 2KCl
2Ba2+ + CrO42- + H2O = 2BaCrO4 ↓ + 2H+
Выполнение реакции.
Реакцию следует проводить в слабокислой среде ацетата натрия (1 капля).
К 1 капле раствора бариевой соли добавляют 1 каплю раствора хромата калия.
Оксалат аммония (NH4)2C2O4 образует с солями бария осадок:
BaCl2 + (NH4)2C2O4 = BaC2O4 ↓ + 2NH4Cl
Ba2+ + C2O42- = BaC2O4↓
Выполнение реакции.
К 2 каплям раствора соли бария добавляют 2 капли раствора оксалата аммония.
Реакции катиона Ca2+
Реакция окрашивания пламени.
Летучие соли кальция окрашивают пламя спиртовки в кирпично-красный цвет. Реакция является фармакопейной.
Разбавленная серная кислота H2SO4 образует с ионами кальция белый осадок сульфата кальция:
CaCl2 + H2SO4 = CaSO4 ↓ + 2HCl
Ca2+ + SO42- = CaSO4↓
Оксалата аммония (NH4)2C2O4 дает на холоде в нейтральных, уксуснокислых или слабощелочных растворах белый мелко-кристаллический осадок оксалата кальция:
CaCl2 + (NH4)2C2O4 = CaC2O4 = CaC2O4 ↓ + 2NH4Cl
Cа2+ + C2O42- = CaC2O4↓
Это наиболее важная качественная реакция иона Cа2+ и является фармакопейной.
Гексацианоферрат (II) калия (желтая кровяная соль) K4[Fe(CN)6] с солями кальция образуют в слабощелочной среде белый кристаллический осадок, нерастворимый в уксусной кислоте:
CaCl2 + K2[Fe(CN)6] + NH4Cl = CaKNH4[Fe(CN)6]↓ + 3KCl
Ca2+ + K+ + NH4+ + [Fe(CN)6]4- = CaKNH4[Fe(CN)6]↓
В присутствии значительных количеств иона Ba2+ не рекомендуется применять эту реакцию для открытия ионов Ca2+, т.к. ион Ba2+при достаточном количестве может дать осадок K2[Fe(CN)6]/
Микрокристаллоскопическая реакция. Разбавленная серная кислота образует с солями кальция иглообразные кристаллы CaSO42H2O.
| <== предыдущая | | | следующая ==> |
| | | Как кродировать официально? |
Date: 2016-07-22; view: 515; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |