
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Уравнение состояния идеального газа. Газ называется идеальным, если выполняются следующие условия: 1) молекулы газа на расстоянии не взаимодействуют
Газ называется идеальным, если выполняются следующие условия: 1) молекулы газа на расстоянии не взаимодействуют, а при непосредственном контакте молекул взаимодействие между ними можно считать абсолютно упругим соударением; 2) объем, занимаемый самими молекулами, пренебрежимо мал по сравнению с объемом сосуда, занятого газом.
Оба условия идеальности газа выполняются тем лучше, чем больше среднее расстояние между молекулами, т.е. чем меньше число молекул, находящихся в единице объема. Число молекул, находящихся в единице объема, называется концентрацией молекул n:
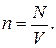 (1.6)
(1.6)
В СИ концентрация измеряется в единицах, деленных на кубический метр (1/м3 или м-3). Газ достаточно хорошо соответствует определению идеального при концентрации 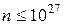 м-3.
м-3.
Совокупность макроскопических величин (p, V, T), характеризующая свойства данной массы газа в некоторый момент времени, называется состоянием газа. Если при неизменных внешних условиях газ может оставаться в каком-либо состоянии сколь угодно долго, оно называется равновесным. Изменение состояния газа называется процессом. Процесс, который протекает настолько медленно, что в каждый момент времени состояние газа можно считать равновесным, называют равновесным или квазистатическим. Равновесные процессы являются обратимыми, т.е. они могут протекать как в прямом, так и в обратном направлениях, при этом в обоих направлениях газ проходит одну и ту же последовательность равновесных состояний. В дальнейшем все рассматриваемые процессы мы «по умолчанию» будем считать равновесными.

Рис. 1.3
Уравнение, связывающее между собой основные макроскопические характеристики системы – давление, температуру и объем - называется уравнением состояния.
Выведем уравнение состояния идеального газа. Для этого рассмотрим газ, заполняющий горизонтальный цилиндрический сосуд с площадью основания S (рис. 1.3). Пусть температура газа равна T, масса молекулы m 0, концентрация молекул n, среднеквадратичная скорость молекул vкв, средняя величина проекции скорости молекул на ось Ох v x. В предыдущей лекции было показано, что величина давления газа или жидкости не зависит от ориентации в пространстве площадки, на которую действует сила давления. Следовательно, мы можем ограничиться рассмотрением давления на какую-либо одну часть внутренней поверхности сосуда. Найдем давление газа на правое основание цилиндра.
Из основного уравнения динамики материальной точки (3.3) следует, что средняя величина силы F, действующей со стороны газа на основание цилиндра, равна 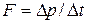 , где D p – модуль изменения импульса молекул газа, испытавших соударение с основанием за время D t. Полагая, что соударения молекул со стенками сосуда являются абсолютно упругими, мы можем записать
, где D p – модуль изменения импульса молекул газа, испытавших соударение с основанием за время D t. Полагая, что соударения молекул со стенками сосуда являются абсолютно упругими, мы можем записать 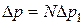 , где N – число соударений,
, где N – число соударений, 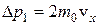 - величина изменения импульса одной молекулы. За время D t дойти до правого основания цилиндра могут только те молекулы, которые в начальный момент находились от него на расстоянии, не превышающем
- величина изменения импульса одной молекулы. За время D t дойти до правого основания цилиндра могут только те молекулы, которые в начальный момент находились от него на расстоянии, не превышающем 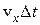 , и двигались в положительном направлении оси Ох. Таким образом, число N равно половине числа молекул, оказавшихся в цилиндре с площадью основания S и высотой
, и двигались в положительном направлении оси Ох. Таким образом, число N равно половине числа молекул, оказавшихся в цилиндре с площадью основания S и высотой 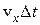 , т.е.
, т.е. 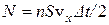 . Давление газа на основание цилиндра
. Давление газа на основание цилиндра
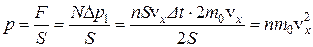 .
.
Учтем, что все направления движения для молекул равнозначны, и, следовательно, средние квадраты проекций скоростей молекул на координатные оси должны быть одинаковыми. Имеем: 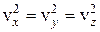 ;
; 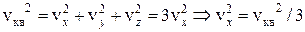 ;
;
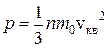 или
или 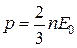 . (1.7)
. (1.7)
Используя формулу (1.4), полученное выражение можно переписать в виде
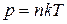 . (1.8)
. (1.8)
Уравнение (1.8) и есть искомое уравнение состояния, которое называют также основным уравнением молекулярно-кинетической теории идеального газа.
Задача 1.2. Идеальный газ массы m = 5 г находится в сосуде объемом V = 3 л под давлением 500 кПа. Определите среднеквадратичную скорость vкв молекул газа.
Date: 2015-05-08; view: 920; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |