
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Высокий уровень сложности. 67. (С3)Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
67. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
бутан 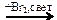 Х1
Х1 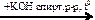 Х2
Х2 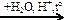 Х3
Х3 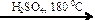 Х2
Х2 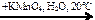 X4
X4
68. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
пропан → пропен 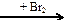 Х1
Х1  Х2
Х2 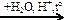 Х3
Х3 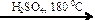 Х2
Х2
Укажите условия протекания первой реакции.
69. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
C2H4 → С2Н5Сl → н-бутан 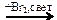 Х1
Х1 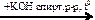 Х2
Х2 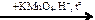 Х3
Х3
Укажите условия протекания реакций.
70. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
СО → C3H8 → пропен 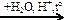 Х1 → пропен
Х1 → пропен 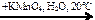 Х2
Х2
Укажите условия протекания реакций.
71. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
СН3СН2СН3 → СН2=СНСН3  Х1
Х1 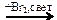 Х2 → СН2=СНСН3
Х2 → СН2=СНСН3 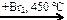 Х3
Х3
Укажите условия протекания реакций.
72. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
СН2=СНСН2СН3 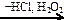 Х1
Х1 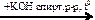 X2
X2 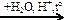 Х3 → бутен-2
Х3 → бутен-2 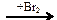 Х4
Х4
Укажите условия протекания реакций.
73. (С4) Этен, полученный при внутримолекулярной дегидратации 200 мл этанола (плотность 0,8 г/мл) с выходом 80%, сожгли. Определите минимальный объем 18,3%-ного раствора гидроксида натрия (плотность 1,2 г/мл), который необходим для полного поглощения углекислого газа, полученного при сгорании этена.
74. (С4) Определите массу 5%-ного водного раствора перманганата калия, которую способен обесцветить этилен, полученный в результате внутримолекулярной дегидратации 17,25 мл этанола (плотность 0,8 г/мл). Выход этилена составляет 80%.
75. (С4) Смесь этена и пропена массой 1,12 г может обесцветить 150 г бромной воды с массовой долей брома 3,2%. Определите объемную долю этена в исходной смеси газов.
76. (С4) Для полного обесцвечивания 5%-ного водного раствора перманганата калия потребовалось 672 мл (н.у.) этилена. Определите массовую долю щелочи в полученном растворе.
77. (С4) Через горячий 15%-ный раствор перманганата калия в сернокислой среде пропускали бутен-2 до полного обесцвечивания раствора. Объем бутена-2 составил 1,12 л (н.у.). Определите массовую долю уксусной кислоты в полученном растворе.
78. (С4) Через горячий 15%-ный раствор перманганата калия в сернокислой среде пропускали пропен до полного обесцвечивания раствора. Объем пропена составил 336 мл (н.у.). Определите массовую долю уксусной кислоты в полученном растворе.
79. (С5) Относительная плотность паров алкена по азоту равна 3,5. Установите молекулярную формулу алкена.
80. (С5) Алкен массой 12,6 г может присоединить 6,72 л (н.у.) водорода. Установите молекулярную формулу алкена.
81. (С5) Алкен массой 2,24 г может обесцветить 200г бромной воды, массовая доля брома в которой равна 3,2%. Установите молекулярную формулу алкена.
82. (С5) В результате взаимодействия алкена массой 8,4 г с бромом в темноте получили 40,4 г дибромпроизводного. Установите молекулярную формулу алкена.
83. (С5) Одинаковое количествоалкена в результате присоединения хлора и брома образует соответственно 7,05 г дихлоралкана и 11,5 г дибромалкана. Установите молекулярную формулу алкена.
84. (С5) Одинаковое количествоалкена в результате присоединения хлороводорода и бромоводорода образует соответственно 12,9 г хлорпроизводного и 21,8 г бромпроизводного. Установите молекулярную формулу алкена.
85. (С5) При сгорании органического вещества массой 4,2 г получили 13,2 г углекислого газа и 5,4 г воды. Плотность паров вещества по азоту равна 3. Установите молекулярную формулу вещества.
Date: 2015-05-05; view: 22835; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |