
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Скорости молекул газа
Каковы скорости, с которыми движутся молекулы, в частности молекулы газов? Этот вопрос естественно возник тотчас же, как были развиты представления о молекулах. Долгое время скорости молекул удавалось оценить только косвенными расчетами, и лишь сравнительно недавно были разработаны способы прямого определения скоростей газовых молекул.
Прежде всего уточним, что надо понимать под скоростью молекул. Напомним, что вследствие беспрестанных столкновений скорость каждой отдельной молекулы все время меняется: молекула движется то быстро, то медленно, и в течение некоторого времени скорость молекулы принимает множество самых различных значений. С другой стороны, в какой-либо определенный момент в громадном числе молекул, составляющих рассматриваемый объем газа, имеются молекулы с самыми различными скоростями. Очевидно, для характеристики состояния газа надо говорить о некоторой средней скорости. Можно считать, что это есть средняя величина скорости одной из молекул за достаточно длительный промежуток времени или что это есть средняя величина скоростей всех молекул газа в данном объеме в какой-нибудь момент времени.
Остановимся на рассуждениях, которые дают возможность подсчитать среднюю скорость газовых молекул.
Давление газа пропорционально птv2, где т — масса молекулы, v — средняя скорость, а п — число молекул в единице объема. Более точный расчет приводит к формуле
 (12)
(12)
Из формулы (12) можно вывести ряд важных следствий. Перепишем формулу (12) в таком виде:

где e — средняя кинетическая энергия одной молекулы. Обозначим давление газа при температурах Т1 и Т2 буквами р1 и р2 а средние кинетические энергии молекул при этих температурах e1 и e2. В таком случае
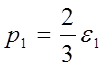 ,
,  и
и 
Сравнивая это соотношение с законом Шарля 
найдем:

Итак, абсолютная температура газа пропорциональна средней кинетической энергии молекул газа. Так как средняя кинетическая энергия молекул пропорциональна квадрату средней скорости молекул, то наше сопоставление приводит к выводу, что абсолютная температура газа пропорциональна квадрату средней скорости молекул газа и что скорость молекул растет пропорционально корню квадратному из абсолютной температуры.
Таблица 4- Средние скорости молекул некоторых газов
| Газ | Масса молекулы, г | Средняя скорость, м/сек |
| Водород | 0,33*10-23 | |
| Кислород | 5,3*10-23 | |
| Азот | 4,6*10-23 | |
| Углекислый газ | 7,3*10-23 | |
| Пары воды | 3,0*10-23 |
Как видно, средние скорости молекул весьма значительны. При комнатной температуре они обычно достигают сотен метров в секунду. В газе средняя скорость движения молекул примерно в полтора раза больше, чем скорость звука в этом же газе.
На первый взгляд этот результат кажется очень странным. Кажется, что молекулы не могут двигаться с такими большими скоростями: ведь диффузия даже в газах, а тем более в жидкостях, идет сравнительно очень медленно, во всяком случае гораздо медленнее, чем распространяется звук. Дело, однако, в том, что, двигаясь, молекулы очень часто сталкиваются друг с другом и при этом меняют направление своего движения. Вследствие этого они двигаются то в одну, то в другую сторону, в основном толкутся на одном месте. В результате, несмотря на большую скорость движения в промежутках между столкновениями, несмотря на то, что молекулы нигде не задерживаются, они продвигаются в каком-либо определенном направлении довольно медленно.
Таблица показывает также, что различие в скоростях разных молекул связано с различием их масс. Это обстоятельство подтверждается рядом наблюдений. Например, водород проникает сквозь узкие отверстия (поры) с большей скоростью, чем кислород или азот. Можно обнаружить это на таком опыте.
Стеклянная воронка закрыта пористым сосудом или заклеена, бумагой и опущена концом в воду. Если воронку накрыть стаканом, под который впустить водород (или светильный газ), то увидим, что уровень воды в конце воронки понизится и из нее начнут выходить пузырьки. Как это объяснить?

|
Рисунок 4- Опыт с водородом
Сквозь узкие поры в сосуде или в бумаге могут проходить и молекулы воздуха (изнутри воронки под стакан), и молекулы водорода (из-под стакана в воронку). Но быстрота этих процессов различна. Различие в размерах молекул не играет при этом существенной роли, ибо различие это невелико, особенно по сравнению с размерами пор: молекула водорода имеет “длину” около 2,3*10-8 см, а молекула кислорода или азота—около 3*10-8 см, поперечник же отверстий, которые представляют собой поры, в тысячи раз больше. Большая скорость проникновения водорода через пористую стенку объясняется большей скоростью движения его молекул. Поэтому молекулы водорода быстрее проникают из стакана в воронку. В результате в воронке получается накопление молекул, давление увеличивается и смесь газов в виде пузырьков выходит наружу.
Подобными приборами пользуются для обнаружения примеси рудничных газов к воздуху, могущих вызвать взрыв в рудниках.
Теплоемкость газов
Предположим, что мы имеем 1 г газа. Сколько надо сообщить ему теплоты для того, чтобы температура его увеличилась на 1°С, другими словами, какова удельная теплоемкость газа? На этот вопрос, как показывает опыт, нельзя дать однозначного ответа. Ответ зависит от того, в каких условиях происходит нагревание газа. Если объем его не меняется, то для нагревания газа нужно определенное количество теплоты; при этом увеличивается также давление газа. Если же нагревание ведется так, что давление его остается неизменным, то потребуется иное, большее количество теплоты, чем в первом случае; при этом увеличится объем газа. Наконец, возможны и иные случаи, когда при нагревании меняются и объем, и давление; при этом потребуется количество теплоты, зависящее от того в какой мере происходят эти изменения. Согласно сказанному газ может иметь самые разнообразные удельные теплоемкости, зависящие от условий нагревания. Выделяют обычно две из всех этих удельных теплоемкостей: удельную теплоемкость при постоянном объеме (Сv) и удельную теплоемкость при постоянном давлении (Cp).
Для определения Сv надо нагревать газ, помещенный в замкнутый сосуд. Расширением самого сосуда при нагревании можно пренебречь. При определении Cp нужно нагревать газ, помещенный в цилиндр, закрытый поршнем, нагрузка на который остается неизменной.
Теплоемкость при постоянном давлении Cp больше, чем теплоемкость при постоянном объеме Cv. Действительно, при нагревании 1 г газа на 1° при постоянном объеме подводимая теплота идет только на увеличение внутренней энергии газа. Для нагревания же на 1° той же массы газа при постоянном давлении нужно сообщить ему тепло, за счет которого не только увеличится внутренняя энергия газа, но и будет совершена работа, связанная с расширением газа. Для получения Сp к величине Сv надо прибавить еще количество теплоты, эквивалентное работе, совершаемой при расширении газа.
Заключение
Природный газ - одно из важнейших горючих ископаемых, занимающие ключевые позиции в топливно-энергетических балансах многих государств, важное сырьё для химической промышленности.
Почти на 90% он состоит из углеводородов, главным образом метана СН4.Содержит и более тяжёлые углеводороды- этан, пропан, бутан, а так же меркаптаны и сероводород (обычно эти примеси вредны),азот и углекислый газ (они в принципе бесполезны, но и не вредны),пары воды, полезные примеси гелия и других инертных газов.
Энергетическая и химическая ценность природного газа определяется содержанием в нём углеводородов. Очень часто в месторождениях он сопутствует нефти. Разница в составе природного и попутного нефтяного газа имеется. В последнем, как правило, больше сравнительно тяжёлых углеводородов, которые обязательно отделяются, прежде чем использовать газ.
Метан, содержавшийся в природном газе, представляет немалую ценность для химической промышленности. При неполном сгорание его образуется водород, оксид углерода СО, ацетилен, а от них начинаются разнообразные цепи химических превращений, приводящих к образованию альдегидов, спиртов, ацетона, уксусной кислоты, амиака...Природный газ, а не вода, является главным
источником промышленного получения водорода. И всё же в основном метан идёт на сжигание. Синтетические возможности других углеводородов, содержащихся в природном газе, более богатые, чем метана. Эти углеводороды превращают прежде всего в этилен и пропилен -важнейшее сырьё для производства пластических масс.
Хранят природный газ в подземных газохранилищах, нередко используя для этого прежние выработки и огромные естественные пещеры. В газгольдерах же (держателях) хранится лишь минимально необходимый запас газа.
Date: 2015-11-13; view: 1834; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |