
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

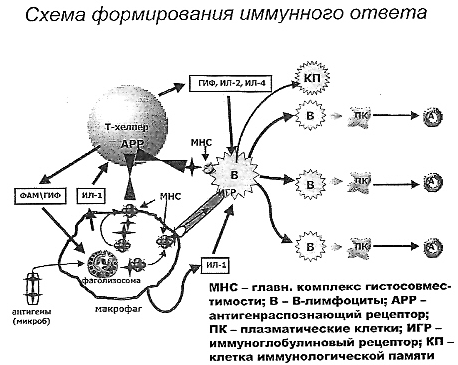
Формирование иммунного ответа
В процессе формирования и реализации иммунного ответа можно выделить несколько этапов.
1.
Распознавание и процессинг антигена.
Первой клеткой, участвующей в распознавании антигена, является фагоцит. Роль последнего заключается не только в уничтожении патогенного микроорганизма, но и в запуске многокомпонентной иммунной реакции, заканчивающейся выработкой антител, предназначенных для антигена (антигенов), которых несет данный микроорганизм.
После захвата и погружения микробной клетки в протоплазму фагоцита, вокруг нее образуется фагосома, в которую лизосомы «вспрыскивают» соответствующие ферменты, под влиянием которых вещество микробной клетки разрушается до отдельных пептидов. Учитывая участие лизосом в этом процессе, фагосому часто называют еще и «фаголизосомой». Нужно подчеркнуть, что подобному процессу обработки подвергаются не только целые микробные клетки, но и вирусные частицы, токсины микробов, высокомолекулярные белки и полисахариды (например, поступающие в организм при вакцинации).
«Разборка» высокомолекулярных веществ в фагоците на отдельные составляющие (полипептиды) и дальнейшее использование их в формировании иммунного ответа, получило название «процессинга».
Одновременно с процессингом антигена в фагоците начинается синтез молекул главного комплекса гистосовместимости (МНС), которые, окруженные специальной вакуолью, проникают в фагосому. В фагосоме происходит объединение молекулы МНС с бактериальным пептидом. Созданный комплекс экспрессируется на поверхности макрофага. Кроме того, процессированный антиген может быть экспрессирован на поверхности макрофага и вне связи с молекулами МНС.
2.
^ Распознавание антигена Т-хелпером.
Представление процессированного антигена Т-хелперу (фактически – запуск программы дальнейшей деятельности Т-хелпера) осуществляется за счет контакта комплекса: молекула МНС фагоцита – процессированный антиген с антигенраспознающим рецептором Т-хелпера. В процессе распознавания антигена принимают участие и корецепторы Т-клеток: CD4 у Т-хелперов или CD8 у Т-супрессеров и других цитотоксических лимфоцитов.
Активированный Т-хелпер способен передать сигнал далее – на В-лимфоцит. Передача сигнала осуществляется через антигенраспознающий рецептор Т-хелпера и МНС В-лимфоцита.
3.
^ Активация В-лимфоцита и подготовка его к клонированию.
Запуск этого процесса возможен только в том случае, если В-лимфоцит получает двойной сигнал: от Т-хелпера через его антигенраспознающий рецептор и МНС В-лимфоцита, и от своего иммуноглобулинового рецептора, распознавшего экспрессированный на поверхности макрофага антиген.
4.
^ Клонирование В-лимфоцитов и выработка антител.
В-лимфоцит, получивший двумя путями информацию о качестве и структуре антигена (через Т-хелпер и через свой иммуноглобулиновый рецептор), начинает процесс клонирования. После трансформации клона в плазматические клетки, последними начинается синтез огромного количества антител, имеющих специфическое сродство к распознанному антигену.
5.
^ Роль цитокинов в формировании и реализации иммунного ответа.
В процессах активации иммунокомпетентных клеток большую роль играют многие цитокины. К ним можно отнести интерлейкины 1, 2, 4 (ИЛ-1, ИЛ-2, ИЛ-4), фактор активации макрофагов (ФАМ), гамма-интерферон и некоторые другие. Цитокины по принципу прямой и обратной связи активируют иммунокомпетентные клетки и способствуют передаче информации о процессированном антигене от фагоцитов (макрофагов) к конечным исполнителям иммунного ответа – плазматическим клеткам.
Воспаление может выражаться образованием микроскопического очага или обширного участка, иметь не только очаговый, но и диффузный характер. Иногда воспаление возникает в системе тканей, тогда говорят о системных воспалительных поражениях (ревматические болезни при системном воспалительном поражении соединительной ткани, системные васкулиты и др.).
Иногда провести грань между локализованным и системным воспалительным процессом бывает трудно.
Воспаление развивается на территории гистиона и складывается из следующих последовательно развивающихся фаз:
1) альтерация;
2) экссудация;
3) пролиферация гематогенных и гистиогенных клеток и, реже, паренхиматозных клеток (эпителия).
Альтерация - повреждение ткани, является инициальной фазой воспаления и проявляется различного вида дистрофией и некрозом. В эту фазу воспаления происходит выброс биологически активных веществ - медиаторов воспаления. Это - пусковой механизм воспаления, определяющий кинетику воспалительной реакции.
Медиаторы воспаления могут быть плазменного (гуморального) и клеточного (тканевого) происхождения. Медиаторы плазменного происхождения - это представители калликреин-кининовой (кинины, калликреины), свертывающей и противосвертывающей (12 фактор свертывания крови, или фактор Хагемана, плазмин) и комплементарной (компоненты Сз - СБ) систем. Медиаторы этих систем повышают проницаемость микрососудов, активируют хемотаксис полиморфно-ядерных лейкоцитов, фагоцитоз и внутрисосудистую коагуляцию.
Эффекторными клетками, продуцирующими медиаторы воспаления, являются и клетки иммунных реакций - макрофаги, выбрасывающие свои монокины (интерлейкин 1), и лимфоциты, продуцирующие лимфокины (интерлейкин 2). С медиаторами клеточного происхождения связано не только повышение проницаемости микрососудов и фагоцитоз; они обладают бактерицидным действием, вызывают вторичную альтерацию (гистолиз), включают иммунные механизмы в воспалительную реакцию, регулируют пролиферацию и дифференцировку клеток на поле воспаления, направленные на репарацию, возмещение или замещение очага повреждения соединительной тканью. Дирижером клеточных взаимодействий на поле воспаления является макрофаг.
Медиаторы плазменного и клеточного происхождения взаимосвязаны и работают по принципу аутокаталитической реакции с обратной связью и взаимной поддержкой. Действие медиаторов опосредовано рецепторами на поверхности эффекторных клеток. Из этого следует, что смена одних медиаторов другими во времени обусловливает смену клеточных форм на поле воспаления - от полиморфно-ядерного лейкоцита для фагоцитоза до фибробласта, активируемого монокинами макрофага, для репарации.
Экссудация - фаза, быстро следующая за альтерацией и выбросом медиаторов. Она складывается из ряда стадий: реакция микроциркуляторного русла с нарушениями реологических свойств крови; повышение сосудистой проницаемости на уровне микроциркуляторного русла; экссудация составных частей плазмы крови; эмиграция клеток крови; фагоцитоз; образование экссудата и воспалительного клеточного инфильтрата.
Реакция микроциркуляторного русла с нарушениями реологических свойств крови - один из ярких морфологических признаков воспаления. Изменения микрососудов начинаются с рефлекторного спазма, уменьшения просвета артериол и прекапилляров, которое быстро сменяется расширением всей сосудистой сети зоны воспаления и прежде всего посткапилляров и венул. Воспалительная гиперемия обусловливает повышение температуры (calor) и покраснение (rubor) воспаленноrо участка. При начальном спазме ток крови вартериолах становится ускоренным, а затем замедленным. В лимфатических сосудах, как и в кровеносных, вначале происходит ускорение лимфотока, а затем его замедление. Лимфатические сосуды переполняются лимфой и лейкоцитами.
В бессосудистых тканях (роговица, клапаны сердца) в начале воспаления преобладают явления альтерации, а затем происходит врастание сосудов из соседних областей (это происходит очень быстро) и включение их в воспалительную реакцию.
Изменения реологических свойств крови состоят в том, что в расширенных венулах и посткапиллярах при замедленном токе крови нарушается распределение в кровяном потоке лейкоцитов и эритроцитов. Полиморфно-ядерные лейкоциты (нейтрофилы) выходят из осевого тока, собираются в краевой зоне и располагаются вдоль стенки сосуда. Краевое расположение нейтрофилов сменяется их краевым стоянием, которое предшествует эмиграции за пределы сосуда.
Изменения гемодинамики и сосудистого тонуса в очаге воспаления приводят к стазу в посткапиллярах и венулах, который сменяется тромбозом. Те же изменения возникают и в лимфатических сосудах. Таким образом, при продолжающемся притоке крови в очаг воспаления отток ее, а также лимфы нарушается. Блокада отводящих кровеносных и лимфатических сосудов позволяет очагу воспаления выполнять роль барьера, предупреждающего генерализацию процесса.
Повышение сосудистой проницаемости на уровне микроциркуляторного русла является одним из существенных признаков воспаления. Вся гамма тканевых изменений, своеобразие форм воспаления в значительной мере определяются состоянием сосудистой проницаемости, глубиной ее повреждения. Большая роль в осуществлении повышенной проницаемости сосудов микроциркуляторного русла принадлежит поврежденным ультраструктурам клеток, что приводит к усилению микропиноцитоза. С повышенной сосудистой проницаемостью связаны экссудация в ткани и полости жидких частей плазмы, эмиграция клеток крови, образование экссудата (воспалительного выпота) и воспалительного клеточного инфильтрата.
Экссудация составных частей плазмы крови рассматривается как проявление сосудистой реакции, развивающейся в пределах микроциркуляторного русла. Она выражается в выходе за пределы сосуда жидких составных частей крови: воды, белков, электролитов.
Эмиграция клеток крови, т. е. выход их из тока крови через стенку сосудов, осуществляется с помощью хемотаксических медиаторов. Как уже было сказано, эмиграции предшествует краевое стояние неЙтрофилов. Они прилипают к стенке сосуда (главным образом в посткапиллярах и венулах), затем образуют отростки (псевдоподии), которые проникают между эндотелиальными клетками - межэндотелиальная эмиграция. Базальную мембрану нейтрофилы преодолевают, вероятнее всего, на основе феномена тиксотропии (тиксотропия - изометрическое обратимое уменьшение вязкости коллоидов), т. е. перехода геля мембраны в золь при прикосновении клетки к мембране. В околососудистой ткани нейтрофилы продолжают свое движение с помощью псевдоподий. Процесс эмиграции лейкоцитов носит название лейкодиапедеза, а эритроцитов - эритродиапедеза.
| <== предыдущая | | | следующая ==> |
| Оформление границ на политических, политико-административных и административных картах | | | Ехидна |
Date: 2015-08-15; view: 944; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |