
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Расчеты горения
Расчеты горения ведут по химическим уравнениям реакций, используя законы газового состояния: Бойля – Мариотта 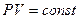 , Гей-Люссака
, Гей-Люссака 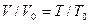 , Шарля
, Шарля 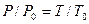 и Клапейрона – Менделеева
и Клапейрона – Менделеева 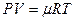 . Используется также закон Авогадро, согласно которому один грамм-моль любого газа при нормальных условиях (Т = 273 К, Р = 760 мм рт. ст.) занимает одинаковый объём – 22,4 дм3. Соответственно один кг-моль – 22,4 м3.
. Используется также закон Авогадро, согласно которому один грамм-моль любого газа при нормальных условиях (Т = 273 К, Р = 760 мм рт. ст.) занимает одинаковый объём – 22,4 дм3. Соответственно один кг-моль – 22,4 м3.
Рассмотрим реакцию горения водорода в кислороде: 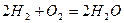 . Из уравнения следует, что при нормальных условиях для полного сгорания 2 × 22,4 = 44,8 м3 водорода требуется 22,4 м3 кислорода. Обычно для простоты и удобства расчеты ведут на один кубометр сжигаемого газа, т.е. для сгорания 1 м3 водорода требуется 0,5 м3 кислорода.
. Из уравнения следует, что при нормальных условиях для полного сгорания 2 × 22,4 = 44,8 м3 водорода требуется 22,4 м3 кислорода. Обычно для простоты и удобства расчеты ведут на один кубометр сжигаемого газа, т.е. для сгорания 1 м3 водорода требуется 0,5 м3 кислорода.
Рассмотрим реакцию горения метана в кислороде: 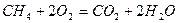 . Из уравнения следует, что для полного сгорания 22,4 м3 метана требуется 2 × 22,4 = 44,8 м3 кислорода. Следовательно, для сгорания 1 м3 метана необходимо 2 м3 кислорода.
. Из уравнения следует, что для полного сгорания 22,4 м3 метана требуется 2 × 22,4 = 44,8 м3 кислорода. Следовательно, для сгорания 1 м3 метана необходимо 2 м3 кислорода.
В практических условиях сжигание газа осуществляется в воздухе. Примем состав сухого воздуха: О2 – 21 %, N2 – 79%. Следовательно, 1 м3 кислорода содержится в 100/21 = 4,76 м3 воздуха. Или на 1 м3 кислорода приходится 3,76 м3 азота. Отсюда условная формула воздуха: (О2 + 3,76N2).
Запишем реакцию горения водорода в воздухе:
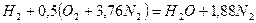 .
.
Из уравнения следует, что при нормальных условиях для полного сгорания 1 м3 водорода требуется 0,5 × 4,76 = 2,38 м3 воздуха. Таким образом, для сгорания 1 м3 водорода требуется 2,38 м3 воздуха. В результате образуются продукты сгорания: 1 м3 воды в виде пара и 1,88 м3 азота.
Запишем реакцию горения метана в воздухе:
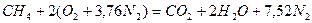 .
.
Из уравнения следует, что для полного сгорания 1 м3 метана необходимо 2 × 4,76 = 9,52 м3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м3 метана требуется 9,52 м3 сухого воздуха. Продукты сгорания содержат 1 м3 диоксида углерода, 2 м3 паров воды и 7,52 м3 азота.
Запишем реакцию горения пропана в воздухе:
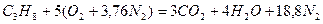 .
.
Из уравнения видно, что для полного сгорания 1 м3 пропана необходимо 5 × 4,76 = 23,8 м3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м3 пропана требуется 23,8 м3 сухого воздуха.
Приведенные расчеты выполнены для стехиометрических уравнений и полученные соотношения воздуха и газа называются стехиометрическими. Например, для горения метана в воздухе стехиометрическое соотношение – 9,52. В реальных условиях воздуха может не хватать для полного сгорания газа или, напротив, воздух подается в избыточном количестве. Для характеристики реальных соотношений воздуха и газа в процессе горения введена безразмерная величина: коэффициент избытка воздуха (окислителя) – коэффициент α. Для стехиометрического соотношения α = 1. Если имеет место недостаток воздуха, то α < 1, а при избытке воздуха α > 1. Например, в процессе горения израсходовано 23 м3 воздуха и 2 м3 метана. Подсчитываем коэффициент α. Реальное соотношение воздуха и газа 23/2 = 11,5. Отсюда α = 11,5/9,52 = 1,2.
Выше показано, как можно подсчитывать необходимое количество воздуха для сгорания и определять объем продуктов сгорания для индивидуальных газов. Но обычно используемый газ – смесь различных газов. В этом случае расчет теоретически необходимого объема воздуха (воздуха сухого) ведется по формуле:
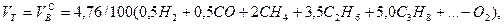 нм3/нм3, (10.4)
нм3/нм3, (10.4)
где 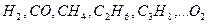 – соответственно объемное процентное содержание данных газов в исходной смеси.
– соответственно объемное процентное содержание данных газов в исходной смеси.
Используемый для сжигания атмосферный воздух содержит влагу, поэтому расчет объема влажного воздуха производят по формуле:
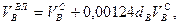 нм3/нм3, (10.5)
нм3/нм3, (10.5)
где 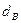 – влагосодержание воздуха, г/нм3;
– влагосодержание воздуха, г/нм3;
0,00124 – объем 1 г водяного пара.
И, наконец, определяется объем воздуха действительный с учетом величины коэффициента α по формуле:
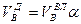 . (10.6)
. (10.6)
Пример. Имеется газ состава СН4 – 95%, С3Н8 – 5%. Определить объем воздуха действительного для сжигания данного газа при α = 1,1 и 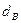 = 10 г/м3.
= 10 г/м3.
Производим расчеты:
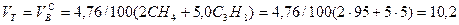 , нм3/нм3,
, нм3/нм3,
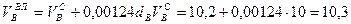 , нм3/нм3,
, нм3/нм3,
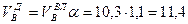 , нм3/нм3.
, нм3/нм3.
Объем продуктов сгорания газовой смеси определяется по следующим формулам.
Объем диоксида углерода
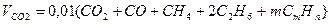 , нм3/нм3. (10.7)
, нм3/нм3. (10.7)
Объем водяных паров
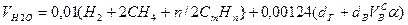 , нм3/нм3. (10.8)
, нм3/нм3. (10.8)
Объем азота
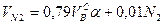 , нм3/нм3. (10.9)
, нм3/нм3. (10.9)
где N 2 – процентное содержание азота в газовой смеси.
Объем кислорода
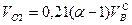 , нм3/нм3. (10.10)
, нм3/нм3. (10.10)
Суммарный объем продуктов сгорания
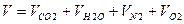 , нм3/нм3. (10.11)
, нм3/нм3. (10.11)
Date: 2015-07-27; view: 580; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |