
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Реакции, используемые для электролитического накопления
Для накопления вещества могут быть использованы различные электрохимические и химические реакции, например: восстановление катионов до соответствующего металла, образование амальгамы или малорастворимого соединения, адсорбция. Для определения веществ различных классов существуют определенные типы реакций и в соответствии с природой образующегося осадка подбираются остальные условия, и, прежде всего рабочий электрод. Чаще всего используются перечисленные ниже типы реакций.
2. Металлы, способные образовывать достаточно концентрированные амальгамы, могут быть сконцентрированы на стационарном ртутном электроде. Металл, образовавшийся из ионов при их электровосстановлении, растворяется в ртутном электроде; затем он анодно растворяется из амальгамы; регистрируется анодный ток.
3. Ионы металла могут быть восстановлены до металла и накоплены на подходящем инертном электроде (благородный металл, графит) в виде пленки. Этот процесс наиболее часто используется для определения ртути, благородных металлов и металлов, не образующих амальгам. Определяемое вещество можно сконцентрировать на электроде в виде малорастворимого соединения. По способу образования последнего реакции подразделяют еще на два типа:
а) Малорастворимое соединение образуется при взаимодействии с ионами материала электрода. Такое соединение концентрируется на электроде при потенциале, соответствующем окислению электродного материала, затем регистрируется катодное растворение пленки (например, определение хлорид-иона на ртутном, или серебряном электроде). Подобные реакции можно использовать для косвенного определения некоторых металлов. Косвенное определение серебра или золота с применением стационарного электрода можно проводить в растворе, содержащем сульфид-ион. После добавления ионов серебра или золота регистрируемый первоначальный пик, соответствующий катодному растворению сульфида, уменьшается, так как часть сульфид-иона осаждается в виде малорастворимого сульфида серебра или золота.
б) Малорастворимое соединение образуется в виде пленки на электроде при взаимодействии с некоторыми компонентами основного электролита или с реагентом, добавляемым в раствор. Во время электродной реакции ионы определяемого вещества восстанавливаются или окисляются до степени окисления, в которой они участвуют в химической реакции, приводящей к образованию осадка. Таким образом, в химической реакции с реагентом принимают участие только ионы, полученные в результате электродной реакции; кроме того, образование осадка должно происходить быстрее, чем перенос продукта электродной реакции от электрода в объем раствора. Только при этих условиях количество образовавшегося осадка пропорционально концентрации вещества в растворе. Самым простым примером применения этой реакции является определение некоторых элементов, образующих малорастворимые оксиды, например определение марганца или свинца после окисления ионов Мn2+ и Рb2+ до МnО2 и РbО2.
4. Для предварительного концентрирования некоторых ионов можно использовать поверхностно-активные вещества. Эти вещества могут адсорбироваться на поверхности электрода и реагировать с определяемым ионом с образованием комплекса (тип 4а), или комплекс иона с поверхностным веществом образуется в растворе и затем адсорбируется на поверхности электрода (тип 4б). Электродная реакция при растворении сводится к восстановлению или окислению адсорбированного на электроде комплекса. Важно, что при этом типе реакций можно достичь накопления даже в отсутствие электролитического тока, хотя количество адсорбированного вещества часто зависит от наложенного на электрод потенциала.
Кроме этих четырех основных типов описаны различные косвенные определения, основанные, например, на вытеснении электроактивного металла из его комплекса электронеактивным металлом или на реакциях осаждения (примеры приведены при рассмотрении третьего способа).
Таблица 1.2. Реакции, используемые в методе инверсионной вольтамперометрии
| Тип реакции | Вещество в растворе | ПРЕДВАРИТЕЛЬНОЕ НАКОПЛЕНИЕ | РАСТВОРЕНИЕ |
| Mn+ | 
| 
| |
| Mn+ | 
| 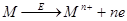
| |
| 3а | An- | 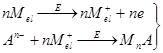
| 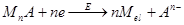
|
| 3б | Mn+ | 
| 
|
| 4а | Mn+ | 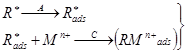
| 
|
| 4б | Mn+ | 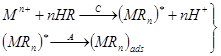
| 
|
| Mn+ | 
| 
| |
| · | An- | 
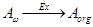
| 
|
| Mn+ | 
| 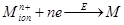
|
*  - материал электрода; А – адсорбция; * - поверхностно-активные вещества; Е – электродная реакция; Ех – экстракция; С – химическая реакция; I – ионный обмен; индексы: w - водный; org – органический; ads – адсорбированный; ion – сорбированный на ионообменнике.
- материал электрода; А – адсорбция; * - поверхностно-активные вещества; Е – электродная реакция; Ех – экстракция; С – химическая реакция; I – ионный обмен; индексы: w - водный; org – органический; ads – адсорбированный; ion – сорбированный на ионообменнике.
Экстракция адсорбированного на поверхности электрода вещества в малый объем растворителя.
Концентрирование на ионообменной мембране, размещенной непосредственно на поверхности электрода.
В табл. 1.2 кратко приведены рассмотренные выше реакции. Уравнения представляют собой только схемы процессов.
Предел обнаружения инверсионных методов можно улучшить при использовании каталитических реакций. В этом случае соединение, электродная реакция которого катализируется накопленным веществом, находится в растворе, и его каталитический ток измеряется в стадии растворения [3].
Date: 2016-02-19; view: 427; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |