
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Украина, Киев, ул. Владимирская, 60; e-mail: [email protected]
Киевский национальный университет им. Тараса Шевченко
аИнститут органической химии НАН Украины
бХимбиоцентр при Киевском национальном университете им. Тараса Шевченко,
Украина, Киев, ул. Владимирская, 60; e-mail: [email protected]
При взаимодействии 6,7,8,9-тетрагидро-5Н-[1,2,4]триазоло[4,3-а]азепинил-3-илацетонитрила с ангидридами и хлорангидридами карбоновых кислот в зависимости от условий проведения реакции и природы ацилирующего агента были получены продукты ацилирования как по атому азота гетероцикла, так и по атому углерода метиленовой группы. При нагревании N-ацилпроизводных происходит миграция ацильного остатка с образованием С-ацилпроизводных.
Ацилирование азолилацетонитрилов ангидридами [1-4] и хлорангидридами [5-7] карбоновых кислот хорошо изучено. Известно, что практически всегда образуются С-ацилпроизводные, лишь в случае ацилирования 2-бензимидазолилацетонитрила были выделены N-ацилированные продукты [8,9]. Ацилирование замещенных триазолилацетонитрилов не изучалось.
Нами найдено, что взаимодействие 6,7,8,9-тетрагидро-5 Н -[1,2,4]триазоло[4,3-а]азепинил-3-ацетонитрила (I) [10] с ацилирующими агентами идет неоднозначно, а именно: либо по атому азота триазольного цикла, либо по атому углерода метиленовой группы. Мы предположили, что N-ацилирование предшествует С-ацилированию триазолоазепинилацетонитрила (I). В мягких условиях (20-25ºC) при использовании ангидридов алифатических кислот были выделены N-ацилпроизводные (IIIа, б ). В спектрах ЯМР 1Н полученных соединений наблюдается однопротонный синглет при 5.34 м.д., соответствующий протону метиновой группы, в спектрах ЯМР 13С виден сигнал углерода амидной карбонильной группы при 170.06 м.д. (IIIа) и 173.27 м.д. (IIIб). В ИК спектрах наблюдаются интенсивная полоса валентных колебаний связи амидной карбонильной группы в области 1710–1690 см-1, слабоинтенсивные полосы валентных колебаний связи С–Н метиновой группы при 3092 см-1 и нитрильной группы в области 2160-2140 см-1. Эти данные подтверждают строение полученных соединений. Кроме того, структура N-ацилпроизводных (IIIa, б ) была доказана химическим путем. Так, при нагревании в бензоле с эквимолярным количеством бензиламина соединение(IIIа ) выступает в роли ацилирующего агента. Это приводит к образованию N-бензилацетамида и исходного соединения (I ). N-ацилированные продукты представляют собой кристаллические вещества, но неустойчивые при длительном хранении, вследствие постепенного их превращения в С-ацилпроизводные.
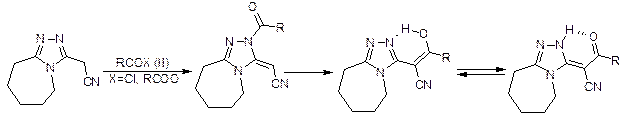 A Б
A Б
I III a, б, IV a-е
III a R = CH3, б R= C2H5, IV a R = CH3, б R= C2H5, в R = CF3, г R = C6H5,
д R = 4-NO2C6H5, е R = 4-CH3C6H5
Таким образом, N-ацилирование предшествует С-ацилированию триазолоазепинилацетонитрила (I). Действительно, при кратковременном нагревании соединений (IIIa, б ) в ДМФА происходит миграция ацильной группы от атома азота гетероцикла к атому углерода енаминового фрагмента с образованием С-ацилпроизводных (IVa, б ), которые могут существовать в двух таутомерных формах А и Б. В спектрах ЯМР 1Н полученных соединений (IVa, б ) виден уширенный сигнал протона при 13.86 м.д. (IVa) и 14.23 м.д. (IVб), включенного в хелатное кольцо, в спектрах ЯМР 13С сигнал углерода карбонильной группы находится при 189.46 м.д. (IVa) и 193.03 м.д. (IVб). В ИК спектрах наблюдается интенсивная полоса валентных колебаний в области 3200–3100 см-1, соответствующие внутримолекулярной водородной связи хелатного типа, но отсутствуют полосы поглощения амидной группы в области 1800–1650 см-1.
При ацилировании соединения (I) ангидридами трифторуксусной и бензойной кислот в условиях, аналогичным получению IIIa, б, были выделены лишь С-ацилированные продукты (IVв, г ). В спектрах ЯМР 1Н полученных соединений наблюдается уширенный однопротонный сигнал при 14.17 м.д. (IVг) и14.87 м.д. (IVв ) хелатированного протона. В ИК спектрах присутствует интенсивная полоса валентных колебаний в области 3200-3100 см-1. С-ацилпроизводные (IVa, б ) также образуются при кратковременном кипячении соединения (I) в избытке соответствующих алифатических ангидридов. Структура полученных нами соединений доказана с помощью ЯМР- и ИК-спектров, а также смешанной пробой на температуры плавления.
При взаимодействии соединения (I) с хлорангидридами карбоновых кислот в зависимости от природы ацилирующих агентов и условий проведения реакции были получены продукты различного строения. Так, при кратковременном кипячении триазолоазепинилацетонитрила (I) (30-60 мин) в бензоле с п-толуилхлоридом в присутствии эквимолярного количества триэтиламина была выделена смесь N и С-ацилированных продуктов, причем состав смеси зависит от продолжительности проведения реакции, а именно: при более длительном нагревании реакционной смеси увеличивается выход С-ацилпроизводного, соответственно количество N-ацилпроизводного уменшается. В случае бензоилхлорида, п-нитробензоилхлорида в аналогичных условиях преимущественно образуются продукты ацилирования по атому углерода метиленовой группы (IVг,д). При проведении данной реакции в диоксане при длительном нагревании в присутствии эквимолярного количества триэтиламина были выделены только С-ацилпроизводные (IVa, г, д, е ).
Date: 2015-05-22; view: 345; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |