
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Спектр атома водорода. Правило отбора
КВАНТОВАЯ ФИЗИКА И ФИЗИКА АТОМА
-----------------------------------------------------------------------
СПЕКТР АТОМА ВОДОРОДА. ПРАВИЛО ОТБОРА
-----------------------------------------------------------------------
1. Закон сохранения момента импульса накладывает ограничения на возможные переходы электрона в атоме с одного уровня на другой (правило отбора). В энергетическом спектре атома водорода (см. рис.) запрещенным является переход …
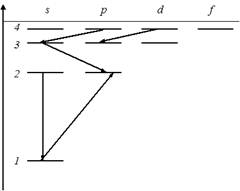

| 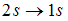
| |
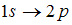
| ||
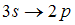
| ||
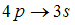
|
-----------------------------------------------------------------------
Решение:
Для орбитального квантового числа l существует правило отбора 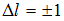 . Это означает, что возможны только такие переходы, в которых l изменяется на единицу. Поэтому запрещенным переходом является переход
. Это означает, что возможны только такие переходы, в которых l изменяется на единицу. Поэтому запрещенным переходом является переход 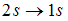 , так как в этом случае
, так как в этом случае 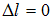 .
.
-----------------------------------------------------------------------
2. Закон сохранения момента импульса накладывает ограничения на возможные переходы электрона в атоме с одного уровня на другой (правило отбора). В энергетическом спектре атома водорода (рис.) запрещенным переходом является …


| 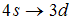
|
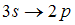
| |
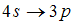
| |
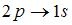
|
-----------------------------------------------------------------------
Решение:
Для орбитального квантового числа l существует правило отбора 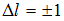 . Это означает, что возможны только такие переходы, в которых l изменяется на единицу. Поэтому запрещенным является переход
. Это означает, что возможны только такие переходы, в которых l изменяется на единицу. Поэтому запрещенным является переход 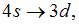 так как в этом случае
так как в этом случае 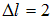 .
.
-----------------------------------------------------------------------
3. Собственные функции электрона в атоме водорода 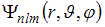 содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет …
содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет …

| проекцию орбитального момента импульса электрона на некоторое направление |
| энергию электрона в атоме водорода | |
| модуль орбитального момента импульса электрона | |
| модуль собственного момента импульса электрона |
-----------------------------------------------------------------------
Решение:
Магнитное квантовое число m определяет проекцию орбитального момента импульса электрона на некоторое направление: 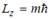 , причем
, причем 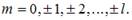 .
.
-----------------------------------------------------------------------
4. Спиновое квантовое число s определяет …

| собственный механический момент электрона в атоме |
| орбитальный механический момент электрона в атоме | |
| энергию стационарного состояния электрона в атоме | |
| проекцию орбитального момента импульса электрона на заданное направление |
-----------------------------------------------------------------------
Решение:
Собственные функции электрона в атоме водорода 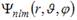 содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Четвертое квантовое число s называется спином и определяет собственный механический момент электрона в атоме.
содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Четвертое квантовое число s называется спином и определяет собственный механический момент электрона в атоме.
-----------------------------------------------------------------------
5. На рисунке схематически изображены стационарные орбиты электрона в атоме водорода, согласно модели Бора, а также показаны переходы электрона с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, в инфракрасной – серию Пашена:
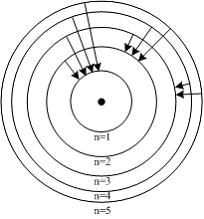
Наименьшей частоте кванта в серии Бальмера соответствует переход …

| 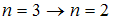
|
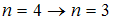
| |
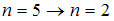
| |
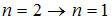
|
-----------------------------------------------------------------------
Решение:
Серию Бальмера дают переходы на второй энергетический уровень, при этом энергия испускаемого кванта, а следовательно, и его частота зависят от разности энергий электрона в начальном и конечном состояниях. Поэтому наименьшей частоте кванта в серии Бальмера (для переходов, представленных на рисунке) соответствует переход 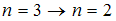 .
.
-----------------------------------------------------------------------
6. Главное квантовое число n определяет …

| энергию стационарного состояния электрона в атоме |
| орбитальный механический момент электрона в атоме | |
| собственный механический момент электрона в атоме | |
| проекцию орбитального момента импульса электрона на заданное направление |
-----------------------------------------------------------------------
Решение:
Собственные функции электрона в атоме водорода 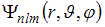 содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Главное квантовое число n определяет энергию стационарного состояния электрона в атоме.
содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Главное квантовое число n определяет энергию стационарного состояния электрона в атоме.
-----------------------------------------------------------------------
7. На рисунке дана схема энергетических уровней атома водорода, а также условно изображены переходы электрона с одного уровня на другой, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой области – серию Бальмера, в инфракрасной области – серию Пашена и т.д.
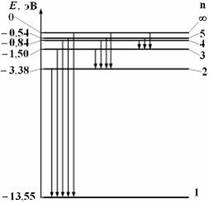
Отношение минимальной частоты линии в серии Бальмера 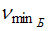 к максимальной частоте линии в серии Лаймана
к максимальной частоте линии в серии Лаймана 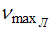 спектра атома водорода равно …
спектра атома водорода равно …

| 5/36 |
| 4/27 | |
| 1/3 | |
| 4/5 |
-----------------------------------------------------------------------
Решение:
Серию Лаймана дают переходы на первый энергетический уровень, серию Бальмера – на второй уровень. Максимальная частота линии в серии Лаймана 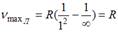 . Минимальная частота линии в серии Бальмера
. Минимальная частота линии в серии Бальмера 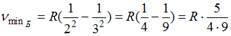 . Тогда
. Тогда 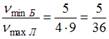 .
.
-----------------------------------------------------------------------
8. На рисунке дана схема энергетических уровней атома водорода.

Наименьшая длина волны спектральной линии (в нм) серии Пашена равна _____.
(h = 6,63·10-34 Дж·с)

| |
-----------------------------------------------------------------------
Решение:
Серию Пашена дают переходы в состояние с n = 3. Учитывая связь длины волны и частоты 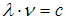 и правило частот Бора
и правило частот Бора 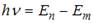 , можно сделать вывод о том, что линии с наименьшей длиной волны (то есть с наибольшей частотой) в серии Пашена соответствует переход с энергетического уровня Е = 0. Тогда
, можно сделать вывод о том, что линии с наименьшей длиной волны (то есть с наибольшей частотой) в серии Пашена соответствует переход с энергетического уровня Е = 0. Тогда 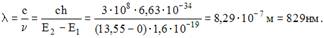
-----------------------------------------------------------------------
9. Спиновое квантовое число s определяет …

| собственный механический момент электрона в атоме |
| орбитальный механический момент электрона в атоме | |
| энергию стационарного состояния электрона в атоме | |
| проекцию орбитального момента импульса электрона на заданное направление |
-----------------------------------------------------------------------
Решение:
Собственные функции электрона в атоме водорода 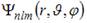 содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Четвертое квантовое число s называется спином и определяет собственный механический момент электрона в атоме.
содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Четвертое квантовое число s называется спином и определяет собственный механический момент электрона в атоме.
-----------------------------------------------------------------------
10. На рисунке схематически изображены стационарные орбиты электрона в атоме водорода согласно модели Бора, а также показаны переходы электрона с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, в инфракрасной – серию Пашена.
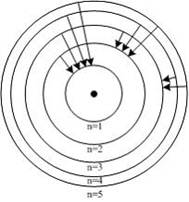
Наибольшей длине волны кванта в серии Лаймана (для переходов, представленных на рисунке) соответствует переход …

| 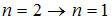
|
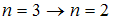
| |
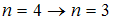
| |
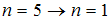
|
-----------------------------------------------------------------------
Решение:
Серию Лаймана дают переходы на первый энергетический уровень; при этом энергия испускаемого кванта, а, следовательно, и его частота зависят от разности энергий электрона в начальном и конечном состояниях. Длина волны излучения связана с его частотой соотношением 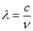 . Поэтому наибольшей длине волны (а следовательно, наименьшей частоте) кванта в серии Лаймана соответствует переход
. Поэтому наибольшей длине волны (а следовательно, наименьшей частоте) кванта в серии Лаймана соответствует переход 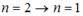 .
.
-----------------------------------------------------------------------
11. На рисунке представлена диаграмма энергетических уровней атома водорода:
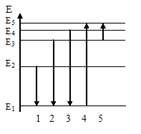
Излучение фотона с наименьшей длиной волны происходит при переходе, обозначенном стрелкой под номером …

| |
-----------------------------------------------------------------------
Решение:
Излучение фотона происходит при переходе электрона с более высокого энергетического уровня на более низкий. Учитывая связь длины волны и частоты 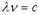 и правило частот Бора
и правило частот Бора 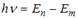 , получаем
, получаем  . Отсюда можно сделать вывод о том, что излучение фотона с наименьшей длиной волны (то есть с наибольшей частотой) происходит при переходе электрона с энергетического уровня Е4 на уровень Е1, что соответствует переходу, обозначенному стрелкой под номером 3.
. Отсюда можно сделать вывод о том, что излучение фотона с наименьшей длиной волны (то есть с наибольшей частотой) происходит при переходе электрона с энергетического уровня Е4 на уровень Е1, что соответствует переходу, обозначенному стрелкой под номером 3.
-----------------------------------------------------------------------
Date: 2015-05-19; view: 6038; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |