
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Распределение Максвелла
Распределение Максвелла — это распределение молекул по модулю, по величине скорости. Так как по величине скорость определяется тремя ее проекциями, а проекции могут иметь независимые значения, то согласно правилу перемножения вероятностей (см. п. 3.3) имеем:
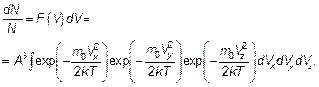 (3.24)
(3.24)
Конечно, при записи этой формулы использован и принцип (распределение) Больцмана. Распределение по направлениям может быть «уничтожено» интегрированием по углам θ и φ, определяющим направление вектора скорости. Очевидно, что
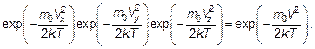 (3.25)
(3.25)
Этот результат можно было предвидеть в соответствии с законом Больцмана. Ведь W к = m 0 V 2/2.
Теперь выразим dVxdVydVz через модуль скорости и углы, задающие ее направление. Для этого используем, что произведение dxdydz — это элемент объема («малый объем»). Также и dVxdVydVz — малый объем в пространстве скоростей.
Переход от Vx; Vy; Vz — проекций скоростей в декартовых координатах (см. рис. 3.5 и 3.9) к модулю скорости 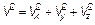 и углам θ и φ совершенно аналогичен переходу от декартовых координат х; у; z к сферическим координатам с расстоянием r 2 = х 2 + у 2 + z 2и теми же углами θ и φ (рис. 3.10).
и углам θ и φ совершенно аналогичен переходу от декартовых координат х; у; z к сферическим координатам с расстоянием r 2 = х 2 + у 2 + z 2и теми же углами θ и φ (рис. 3.10).
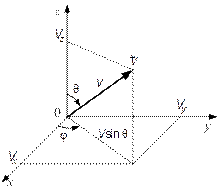
Рис. 3.9. Переход от проекций скоростей Vx; Vy; Vz к модулю скорости V
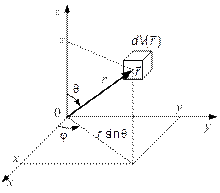
Рис. 3.10. Переход от декартовых координат x, y, z к сферическим r, θ, φ
Сравнивая рис. 3.9 и 3.10, видим, что переход от элемента объема в пространстве скоростей в декартовых координатах dVxdVydVz, к элементу объема также в пространстве скоростей, 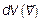 , но выраженному через модуль скорости V и углы θ и φ, полностью аналогичен (совпадает!) с переходом от элемента объема в декартовых координатах dxdydz (рис. 3.11) к элементу объема
, но выраженному через модуль скорости V и углы θ и φ, полностью аналогичен (совпадает!) с переходом от элемента объема в декартовых координатах dxdydz (рис. 3.11) к элементу объема 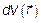 в сферических координатах (рис. 3.12)
в сферических координатах (рис. 3.12)
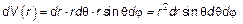 (3.26)
(3.26)
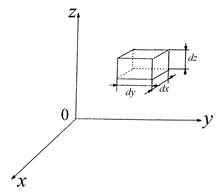
Рис. 3.11. Элемент объема dxdуdz в декартовой системе координат. В пространстве скоростей ему соответствуют dVxdVydVz
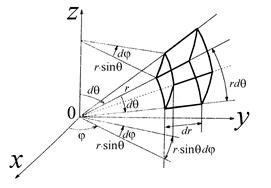
Рис. 3.12. Элемент объема dr ⋅ rd θ ⋅ r sinθ d φ в сферических координатах.
В пространстве скоростей ему соответствует dV ⋅ Vd θ ⋅ V sinq d φ
Очевидно, что для перехода от «пространства координат» к «пространству скоростей» (см. рис. 3.12) нужно заменить х на Vх, у на Vу, z на Vz, радиус-вектор 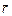 на вектор скорости
на вектор скорости 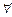 , а радикальную координату
, а радикальную координату 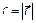 на модуль скорости
на модуль скорости 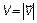 . Тогда элемент объема в пространстве скоростей dVxdVydVz преобразуется в
. Тогда элемент объема в пространстве скоростей dVxdVydVz преобразуется в
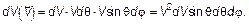 (3.27)
(3.27)
Легко провести интегрирование по углам.
Интегрируем
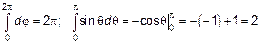 (3.28)
(3.28)
и записываем формулу, позволяющую вычислить вероятность, что молекула имеет скорость с величиной, лежащей в интервале между V и V + dV.
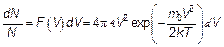 (3.29)
(3.29)
Распределение вероятности имеет вид (рис. 3.13):
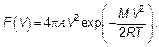 (3.30)
(3.30)
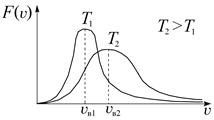
Рис. 3.13. Распределение Максвелла
Именно это распределение и называется распределением Максвелла. Количество молекул, имеющих скорость, лежащую между V и V + dV, будет:
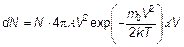 (3.31)
(3.31)
а функция распределения количества молекул, соответственно,
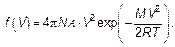 (3.32)
(3.32)
Как видно из формулы (3.30), вид кривой распределения зависит от природы молекул (в формулу входит молярная масса М) и от температуры. На рис. 3.14 приведены кривые распределения молекул азота по скоростям при различных температурах. При повышении температуры вся кривая смещается в сторону больших скоростей (положение максимума, т. е. V нвпропорционально 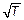 ). Площади под этими кривыми остаются, конечно, неизменными и равными единице, ведь это сумма всех вероятностей того, что молекулы имеют хоть какую-нибудь скорость. Вследствие этого максимум кривой при повышении температуры уменьшается.
). Площади под этими кривыми остаются, конечно, неизменными и равными единице, ведь это сумма всех вероятностей того, что молекулы имеют хоть какую-нибудь скорость. Вследствие этого максимум кривой при повышении температуры уменьшается.
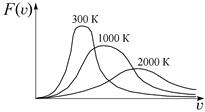
Рис. 3.14. Распределение Максвелла для данного газа при нескольких температурах
Date: 2015-05-08; view: 821; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |