
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Термохимические расчеты
Тепловые эффекты химических реакций определяют как экспериментально, так и с помощью термохимических расчетов.
В основе термохимических расчетов лежит закон Гесса (1841 г):
Тепловой эффект реакции не зависит от пути, по которому протекает реакция (т.е. от числа промежуточных стадий), а определяется начальным и конечным состоянием системы.
Например, реакция горения метана может протекать по уравнению:
СН4 +2О2 = СО2 + 2Н2О(Г) ΔН01 = —802,34 кДж
Эту же реакцию можно провести через стадию образования СО:
СН4 +3/2О2 = СО + 2Н2О(Г) ΔН02 = —519,33 кДж
СО +1/2О2 = СО2 ΔН03 = —283,01 кДж
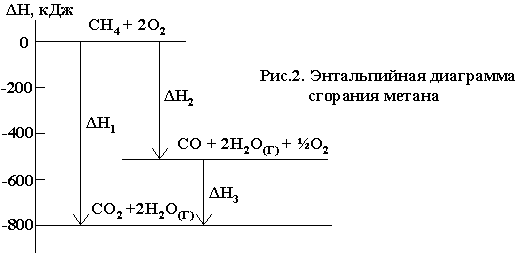
При этом оказывается, что ΔН01 = ΔН02 + ΔН03 . Следовательно, тепловой эффект реакции, протекающей по двум путям, одинаков. Закон Гесса хорошо иллюстрируется с помощью энтальпийных диаграмм (рис.2)
 |
Из закона Гесса вытекает ряд следствий:
1. Тепловой эффект прямой реакции равен тепловому эффекту обратной реакции с противоположным знаком.
2. Если в результате ряда последовательных химических реакций система приходит в состояние, полностью совпадающее с исходным, то сумма тепловых эффектов этих реакций равна нулю (ΔН = 0). Процессы, в которых система после последовательных превращений возвращается в исходное состояние, называются круговыми процессами или циклами. Метод циклов широко используется в термохимических расчетах..
3. Энтальпия химической реакции равна сумме энтальпий образования продуктов реакций за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов.
Здесь встречаемся с понятием ''энтальпия образования''.
Энтальпией (теплотой) образования химического соединения называется тепловой эффект реакции образования 1 моля этого соединения из простых веществ, взятых в их устойчивом состоянии при данных условиях. Обычно теплоты образования относят к стандартному состоянию, т.е. 250С (298 К) и 100 кПа. Стандартные энтальпии образования химических веществ обозначаются ΔН0298 (или ΔН0), измеряются в кДж/моль и приводятся в справочниках. Энтальпию образования простых веществ, устойчивых при 298 К и давлении 100 кПа, принимают равной нулю.
В таком случае следствие из закона Гесса для теплового эффекта химической реакции (ΔН(Х.Р.)) имеет вид:
ΔН(Х.Р.) = ∑ΔН0продуктов реакции — ∑ΔН0исходных веществ
Используя закон Гесса, можно рассчитывать энергию химической связи, энергию кристаллических решеток, теплоты сгорания топлив, калорийность пищи и т.д.
Наиболее распространенные расчеты – вычисление тепловых эффектов (энтальпий) реакций, что необходимо для технологических и научных целей.
Пример 1. Напишите термохимическое уравнение реакции между СО2(Г) и водородом, в результате которой образуются СН4(Г) и Н2О(Г), вычислив ее тепловой эффект на основе данных, приведенных в приложении. Сколько теплоты выделится в этой реакции при получении 67,2 л метана в пересчете на стандартные условия?
Решение. Составляем и уравниваем химическую часть требующегося термохимического уравнения:
СО2(Г) + 3Н2(Г) = СН4(Г) + 2Н2О(Г)
Находим в справочнике (приложение) стандартные теплоты образования соединений, участвующих в процессе:
ΔН0 (СО2(Г)) = —393,51 кДж/моль ΔН0 (СН4(Г)) = —74,85 кДж/моль ΔН0 (Н2(Г)) = 0 кДж/моль ΔН0 (Н2О(Г)) = ―241,83 кДж/моль
Обратите внимание, что теплота образования водорода, как и всех простых веществ в их устойчивом при данных условиях состоянии, равна нулю. Рассчитываем тепловой эффект реакции:
ΔН(Х.Р.) = ∑ΔН0(прод.) — ∑ΔН0(исх.) =
ΔН0(СН4(Г)) + 2ΔН0(Н2О(Г)) — ΔН0(СО2(Г)) —3ΔН0 (Н2(Г))) =
—74,85 + 2(—241,83) — (—393,51) — 3·0 = —165,00 кДж/моль.
Термохимическое уравнение имеет вид:
СО2(Г) + 3Н2(Г) = СН4(Г) + 2Н2О(Г); ΔН = —165,00 кДж
Согласно этому термохимическому уравнению, 165,00 кДж теплоты выделится при получении 1 моль, т.е. 22,4 л метана. Количество теплоты, выделившейся при получении 67,2 л метана, находим из пропорции:
22,4 л —— 165,00 кДж 67,2·165,00
67,2 л —— Q кДж Q = —————— = 495,00кДж
22,4
Пример 2. При сгорании 1л этилена С2Н4(Г) (стандартные условия) с образованием газообразного оксида углерода (IV) и жидкой воды выделяется 63,00 кДж теплоты. Рассчитайте по этим данным мольную энтальпию горения этилена и запишите термохимическое уравнение реакции. Вычислите энтальпию образования С2Н4(Г) и сравните полученное значение с литературными данными (приложение).
Решение. Составляем и уравниваем химическую часть требующегося термохимического уравнения:
С2Н4(Г) + 3О2(Г) = 2СО2(Г) + 2Н2О(Ж); DН =?
Создаваемое термохимическое уравнение описывает горение 1 моль, т.е. 22,4 л этилена. Необходимую для него мольную теплоту горения этилена находим из пропорции:
1л —— 63,00 кДж 22,4·63,00
22,4 л —— Q кДж Q = —————— = 1410,96кДж
DН = -Q, термохимическое уравнение горения этилена имеет вид: С2Н4(Г) + 3О2(Г) = 2СО2(Г) + 2Н2О(Ж); DН = -1410,96 кДж
Для расчета энтальпии образования С2Н4(Г) привлекаем следствие из закона Гесса: ΔН(Х.Р.) = ∑ΔН0(прод.) — ∑ΔН0(исх.).
Используем найденную нами энтальпию горения этилена и приведенные в приложении энтальпии образования всех (кроме этилена) участников процесса.
—1410,96 = 2·(—393,51) + 2·(—285,84) — ΔН0(С2Н4(Г)) — 3·0
Отсюда ΔН0(С2Н4(Г)) = 52,26 кДж/моль. Это совпадает со значением, приведенным в приложении и доказывает правильность наших вычислений.
Пример 3. Напишите термохимическое уравнение образования метана из простых веществ, вычислив энтальпию этого процесса из следующих термохимических уравнений:
СН4(Г) + 2О2(Г) = СО2(Г)+ 2Н2О(Ж) ΔН1 = -890,31 кДж (1)
С(ГРАФИТ) + О2(Г) = СО2(Г) DН2 = -393,51 кДж (2)
Н2(Г) + ½О2(Г) = Н2О(Ж) DН3 = -285,84 кДж (3)
Сравните полученное значение с табличными данными (приложение).
Решение. Составляем и уравниваем химическую часть требующегося термохимического уравнения:
С(ГРАФИТ) + 2Н2(Г) = СН4(Г) DН4 = DН0(СН4(Г))) =? (4)
С термохимическими уравнениями можно оперировать так же, как и с алгебраическими. Мы должны в результате алгебраических действий с уравнениями 1, 2 и 3 получить уравнение 4. Для этого следует уравнение 3 умножить на 2, результат сложить с уравнением 2 и вычесть уравнение 1.
2Н2(Г) + О2(Г) = 2Н2О(Ж) DН0(СН4(Г)) = 2DН3 + DН2 - DН1
+ С(ГРАФИТ) + О2(Г) + СО2(Г) DН0(СН4(Г)) = 2(—285,84)
— СН4(Г) — 2О2(Г) —СО2(Г)— 2Н2О(Ж) + (—393,51)
― (—890,31).
С(ГРАФИТ) + 2Н2(Г) = СН4(Г) DН0(СН4(Г)) = —74,88 кДж
Это совпадает со значением, приведенным в приложении, что доказывает правильность наших вычислений.
Date: 2015-05-05; view: 2078; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |